Аденокарцинома поджелудочной железы патанатомия
Среди предраковых изменений ПЖ наиболее значима дисплазия. Чаще её обнаруживают в экзокринной части ПЖ (в эпителии протоков), реже — в ацинарных клетках. Термин «диеплазия» характеризует нарушение нормального клеточного роста с потерей единообразия клеток и возникновением так называемой «архитектурной анархии». При морфологическом исследовании ПЖ с диспластическими изменениями её экзокринной части обнаруживают участки хаотичного расположения протоковых эпителиальных или ацинарных клеток с признаками клеточного полиморфизма: вариабельностью в размерах и форме, наличием в некоторых клетках крупных гиперхромных ядер.
Помимо дисплазии могут присутствовать гиперплазия и плоскокчеточная метаплазия протокового эпителия, участки междолькового и межацинарного склероза, поли фиброза с «замурованными» в них протоками и ацинусами, кчеточными инфильтратами и липоматозом. Это подтверждает, что диеплазия предракового эпителия и ацинарных клеток часто возникает на фоне ХП, особенно сопровождающегося вторичным сахарным диабетом.
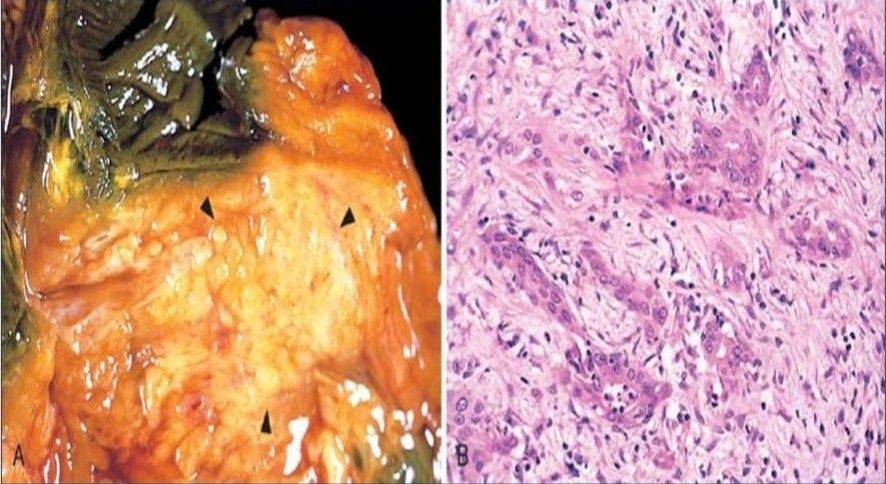
Рак ПЖ может развиваться в любом её отделе, но чаще в головке, где имеет вид плотного сероватого узла (см. рис. 5-14 a). Опухоли тела и хвоста нередко достигают значительных размеров, так как длительное время могут протекать скрыто, не сдавливая проток ПЖ и общий жёлчный проток (см. рис. 5-14 б).

Рис. 5-14. Рак поджелудочной железы (макропрепарат): а — рак головки поджелудочной железы; б — рак хвоста поджелудочной железы
Самая частая злокачественная опухоль ПЖ — протоковая аденокарцинома (см. рис. 5-15). Такой морфологический вариант обнаруживают у 75—90% больных раком ПЖ, несмотря на то, что протоковый эпителий составляют только 10—30% от общего удельного веса нормальной паренхимы ПЖ. У одной четверти больных присутствуют, кроме основного очага, участки с карциномой in situ. Таким образом, возможно полифокальное возникновение очагов озлокачествления. Средний размер опухоли на момент обнаружения — 5 см. Средняя выживаемость— 16 нед от момента установления диагноза; 1 год живут 17% больных, 5 лет — 1%. В 61% случаев опухоль растёт в головке, в 18% — в теле и в 21 % — в хвосте.

Рис. 5-15. Протоковая аденокарцинома поджелудочной железы при разном увеличении (окраска гематоксилином и эозином)
В 6% случаев обнаруживают гигантоклеточные аденокарциномы, представляющие собой скопление кистозных полостей геморрагического характера. Встречаются чаще у мужчин (соотношение мужчин и женщин 1,5:1). При первичной диагностике такие опухоли имеют крупные размеры — примерно 11 см в диаметре. Средняя выживаемость составляет 8 нед, практически ни один из больных этим вариантом рака не живет более 1 года после установления диагноза. Половина гигантоклеточных аденокарцином располагается в головке.
Железисто-плоскоклеточный рак представляет собой смешанную опухоль, состоящую из двух неопластических компонента — железистого и сквамозного. Частота встречаемости составляет 3—4% от всех опухолей, у мужчин встречается в 3 раза чаще. В структуре опухоли чаще преобладает железистый компонент, что объясняет высокий уровень метастазирования данного гистологического варианта опухоли. Более чем в 60% случаев железисто-плоскоклеточный рак распологается в головке ПЖ, значительно реже — в хвосте; зачастую очаги множественные. Средняя выживаемость достигает 24 нед, более 1 года живут 5% больных, до 3—5 лет, как правило, никто не доживает.
Некоторые авторы ставят под сомнение существование изолированного плоскоктеточного рака ПЖ, поскольку для объективного суждения об отсутствии железистого компонента необходимо радикально удалить опухоль ПЖ, что, к сожалению, не всегда осуществимо. В то же время есть публикации о таком варианте рака (см. рис. 5-16). Частота их встречаемости составляет менее 0,005% от всех злокачественных опухолей ПЖ.

Рис. 5-16. Плоскоклеточный рак поджелудочной железы
Муцинозная аденокарцинома составляет 1—3% всех случаев злокачественных опухолей ПЖ. Размер опухоли при первичной диагностике составляет, в среднем, 6 см; у 78% больных она локализуется в головке. Средняя продолжительность жизни после установления диагноза достигает 44 нед, около 33% больных живут- более I года. В целом прогноз несколько более благоприятный, чем при протоковой карциноме.
Муцинозная цистаденокарцинома составляет 1% всех случаев рака ПЖ. Чаще болеют женщины. В 60% случаев опухоль локализуется в теле, в 20% — в головке и в 20% — хвосте, железы. Во время первичной диагностики опухоль достигает 16 см в диаметре. Примерно 50% больных можно излечить хирургическим путем (больные живут до 5 лет). От доброкачественных кист опухоль отличается присутствием стенок и перегородок.
Ацинарный рак (гроздевидный, ацинарноклеточная карцинома) составляет 1,0—1,5% всех больных раком ПЖ различных возрастных групп; у мужчин встречается в 2,5 раза чаще. Характеризуется ацинарноподобным строением опухоли (см. рис. 5-17). Клиническая картина: длительное бессимптомное течение, прогрессирующая потеря веса и болевой абдоминальный синдром наблюдают у половины больных, симптомы диспепсии встречаются реже — в 20% случаев, повышение липазы в сыворотке крови — у 16% больных.

Рис. 5-17. Ацинарноклеточная карцинома: а — ацинарная архитектоника опухоли (окраска гематоксилином и эозином, ×400), чередующиеся ацинарные и трабекулярные клетки с цитоплазматическими гранулами; б — ацинарноклеточная карцинома поджелудочной железы при малом увеличении, хорошо видно ацинарноподобное строение опухоли
У больных ацинарноклеточной карциномой с высокими сывороточными уровнями панкреатической липазы нередко развиваются системные осложнения в виде очаговых некрозов подкожной жировой клетчатки и полиартрита, Опухоль наиболее часто обнаруживают в головке и теле ПЖ — в 56 и 36% случаев, соответственно. Средний размер опухоли во время первичной диагностики составляет 5,0—10,8 см. Средняя выживаемость — 28 нед; 1 год живут 14% больных, до 5-ти лет не доживает никто.
В целом рак ПЖ метастазирует рано и даёт обширные распространённые метастазы, сначала лимфогенные (в парапанкреатические и другие лимфатические узлы), а затем и гематогенные (в печень, лёгкие, костную систему и другие органы).
Маев И.В., Кучерявый Ю.А.
Источник
В соответствии с анатомическим строением поджелудочной железы рак локализуется в головке в 73,4-56%, в теле – 18,2-9,8%, в хвосте – 7,4-6%, тотальное поражение 28,2-5,9%. Основная характерная черта – мультицентричность роста, что обусловливает высокую частоту рецидивов. Прорастание опухоли в соседние органы и структуры наблюдается в 50-60%случаев. Лимфогенным путем в 40-50% случаев поражаются сначала регионарные, а затем отдаленные лимфатические узлы: мезентериальные, забрюшинные, ворот печени, желудка, сальника, брыжейки поперечно-ободочной кишки. Изредка поражаются медиастинальные и паратрахеальные, надключичные лимфатические узлы. Метастазы в яичники, параректальные и паховые лимфатические узлы отмечается при обратном токе лимфы в результате «блока» отводящих лимфатический путей.
Регионарный лимфатический аппарат головки и крючковидного отростка поджелудочной железы представлен З коллекторами: чревными, верхнебрыжеечными, воротнопеченочными. В каждом из них имеется 4 последовательных этапа в виде скопления регионарных лимфатических узлов.
Первый этап – панкреатодуоденальные лимфоузлы, второй этап – ретропилорические и гепатодуоденальные лимфоузлы, третий этап – чревные и верхнебрыжеечные лимфоузлы, четвертый этап – парааортальные и паракавальные лимфоузлы. Гематогенное метастазирование отмечается в 50-55% случаев, из них – по системе воротной вены в 25% случаев поражается печень, а в остальных – лёгкие, надпочечники, почки, кости, иногда кожа.
Интраоперационное изучение состояния срезов замороженных парапанкреатических, воротнопеченочных лимфоузлов формируют основные критерии целесообразности выполнения радикальной или симптоматической операции. Выявление микрометастазов в указанных лимфоузлах является основанием к отказу от радикальной операции в пользу симптоматической, поскольку существенной разницы в 5-ти летней выживаемости не наблюдается.
Гистологическая классификация:
1. Аденокарцинома — папиллярная, скиррозная, тубулярная, муцинозная;
2. Железисто-плоскоклеточный рак;
3. Плоскоклеточный рак;
4. Недифференцированный рак;
5. Неклассифицированный рак.
95% случаев рака поджелудочной железы – аденокарцинома из протокового эпителия.
ТNМ клиническая классификация:
Т – первичная опухоль
ТХ – не достаточно данных для оценки первичной опухоли
Т0 – первичная опухоль не определяется
Тis – carcinoma in situ
Т1 – опухоль ограничена поджелудочной железой, 2 см или меньше в наибольшем измерении
Т2 – опухоль ограничена поджелудочной железой, более 2 см в наибольшем измерении
Т3 – опухоль распространяется за границы поджелудочной железы, но без поражения брюшного ствола или верхней брыжеечной артерии
Т4 – опухоль распространяется на брюшной ствол или верхнюю брыжеечную артерию (нерезектабельная первичная опухоль)
N – регионарные лимфатические узлы
Регионарными лимфатическими узлами являются:
Верхние – выше головки и тела поджелудочной железы
Нижние – ниже головки и тела поджелудочной железы
Передние – передние панкреато-дуоденальные, пилорические и проксимальные брыжеечные
Задние – задние панкреато-дуоденальные, общего желчного протока и проксимальные брыжеечные
Селезеночные – ворот селезенки и хвоста поджелудочной железы (только для опухолей тела и хвоста)
Брюшные – (только для опухолей тела поджелудочной железы)
NХ – не достаточно данных для оценки состояния регионарных лимфатических узлов
N0 – нет признаков поражения регионарных лимфатических узлов
N1 – наличие метастазов в регионарных лимфатических узлах
М – отдаленные метастазы
МХ – не достаточно данных для определения отдаленных метастазов
М0 – отдаленные метастазы не определяются
М1 – присутствуют отдаленные метастазы
рТNМ патоморфологическая классификация:
Категории рТ, рN, рМ соответствуют категориям Т, N, М.
рN0 — Материал для гистологического исследования после регионарной лимфаденэктомии должен включать не менее 10 лимфатических узлов.
G – гистопатологическая градация
G1 – высокий уровень дифференциации
G2 – средний уровень дифференциации
G3 – низкий уровень дифференциации
G4 – недифференцированная опухоль
Группировка по стадиям:
| Стадия 0 | Тis | N0 | М0 |
| Стадия ІА | Т1 | N0 | М0 |
| Стадия ІВ | Т2 | N0 | М0 |
| Стадия ІІА | Т3 | N0 | М0 |
| Стадия ІІВ | Т1, Т2, Т3 | N1 | М0 |
| Стадия ІІІ | Т4 | любое N | М0 |
| Стадия ІV | любое Т | любое N | М1 |
Клинические признаки:
1. Дожелтушные проявления:
· боль носит неспецифический и вариабельный характер, преимущественно сосредоточена в эпигастральной области с иррадиацией в пояснично-крестцовую зону, не связанна с приемом пищи;
· стремительно прогрессирующая потеря массы тела;
· выраженная анорексия (anorecsia pancreatica) у 64% больных;
· тошнота;
· функциональные кишечные расстройства;
· общая слабость, повышенная утомляемость, апатия у 70% больных;
· лихорадка у 26% больных;
· паранеопластические состояния («необъяснимые» мигрирующие периферические флебиты, симптом Труссо).
2. Желтушные проявления:
· зависят от локализации опухоли в поджелудочной железе, при локализации опухоли в ее головке желтуха развивается в 89% случаев;
· кожный зуд;
· брадикардия;
· явления холангита – ознобы;
· бессонница;
· кожные эскориации;
· холемический геморрагический синдром;
· иктеричность кожи и склер в зависимости от цифр гипербилирубинемии.
3. Физикальные признаки рака поджелудочной железы:
· пальпируемая опухоль у 20% больных;
· положительный симптом Курвуазье у 50- 60% больных с локализацией опухоли в головке поджелудочной железы;
· асцит на поздних стадиях заболевания.
Диагностика:
1. Неинвазивные методы:
· прямые методы контрастирования – релаксационная зондовая дуоденография;
· непрямые методы контрастирования – выделительная инфузионно-капельная холангиография. Последняя невозможна при гипербилирубинемии больше 34 мкмоль/л;
· ультрасонография + доплерография;
· компьютерная томография с контрастным усилением;
· ядерно-магнитно-резонансная томография.
2. Инвазивные прямые методы:
· пункционная черезкожная черезпеченочная холангиография. При билиарной гипертензии может быть завершена наружной холангиостомией;
· эндоскопическая ретроградная панкреатохолангиография ;
· ультрасонография + пункционная аспирационная тонкоигольная биопсия.
3. Лабораторная диагностика:
· Повышение уровня α-фетопротеина, щелочной фосфатазы, раково-эмбрионального антигена, СА-19 (специфичность СА-19 достигает до 90%), трансаминаз, амилазы сыворотки, билирубина, мочевины, глюкозы.
· Проба со стимуляцией секретином выявляет снижение объема панкреатической секреции при нормальном содержании ферментов и бикарбоната.
· Признаки гиперкоагуляции.
4. Ангиография – используется редко, в основном, для выявления вовлечения в опухоль верхней брыжеечной и селезеночной вены. Позволяет определить смещение и/или сдавление панкреатодуоденальной артерии.
5. Мероприятия направленные на исключение метастазов в отдаленные органы – рентгенография легких, компьютерная томография грудной клетки, лапароскопия, остеосцинтиграфия по показаниям.
Дифференциальная диагностика:
· кисты поджелудочной железы,
· хронический индуративный панкреатит,
· калькулезный панкреатит,
· рак желудка,
· рак толстой кишки,
· поражение поджелудочной железы при лимфопролиферативных заболеваниях.
Источник
Протоковая аденокарцинома — опухоль эпителиального происхождения, развивающаяся из клеток, выстилающих протоки поджелудочной железы. Процесс может затрагивать любую часть железы, но наиболее частой локализацией служит ее головка. Это одно из наиболее распространенных онкологических заболеваний поджелудочной железы. Опухоль чрезвычайно злокачественна и в большинстве случаев приводит к летальному исходу. Ежегодно в США заболевает 44 000 человек, 38 000 погибает. Тенденция такова, что протоковая аденокарцинома в своей летальности вскоре может опередить смертность от рака груди и толстой кишки.
Чаще всего данное заболевание встречается в промежутке между 55 и 84 годами. Особую роль играет наследственная предрасположенность: риск заболеть возрастает на 40% у людей, имеющих трех и более родственников первой линии, двух — на 10% и на 6% при наличии одного такого родственника. Табакокурение, частое употребление алкоголя, хронический панкреатит, ожирение так же предрасполагают к этому заболеванию. Имеются данные о связи с сахарным диабетом II типа и инфицированием Helicobacter pylori.
Считается, что аденокарцинома в своем развитии имеет некоторую стадийность. Всё начинается с преинвазивной стадии — панкреатической интраэпителиальной неоплазии. Это поражение эпителия стимулируется накоплением генетических мутаций. Наиболее распространенной является мутация в онкогене K-ras (встречается в 90% случаев). Другими часто встречающимися нарушениями служат мутация в Her-2 и потеря антионкогенных свойств p16, p53 и SMAD4.
Макроскопически опухоль выглядит как неоднородная, склерозированная, грубая бело-желтая масса. Границы карциномы нечеткие, опухоль инфильтрирует окружающие ткани. Микроскопически практически во всех случаях определяется периневральная инвазия. Присутствуют сосудистые и лимфатические микрометастазы; часто обнаруживается некроз опухоли. Даже в тех случаях, когда аденокарцинома локализована, она имеет низкую степень дифференцировки, и ее очень сложно обнаружить на ранних, курабельных стадиях.
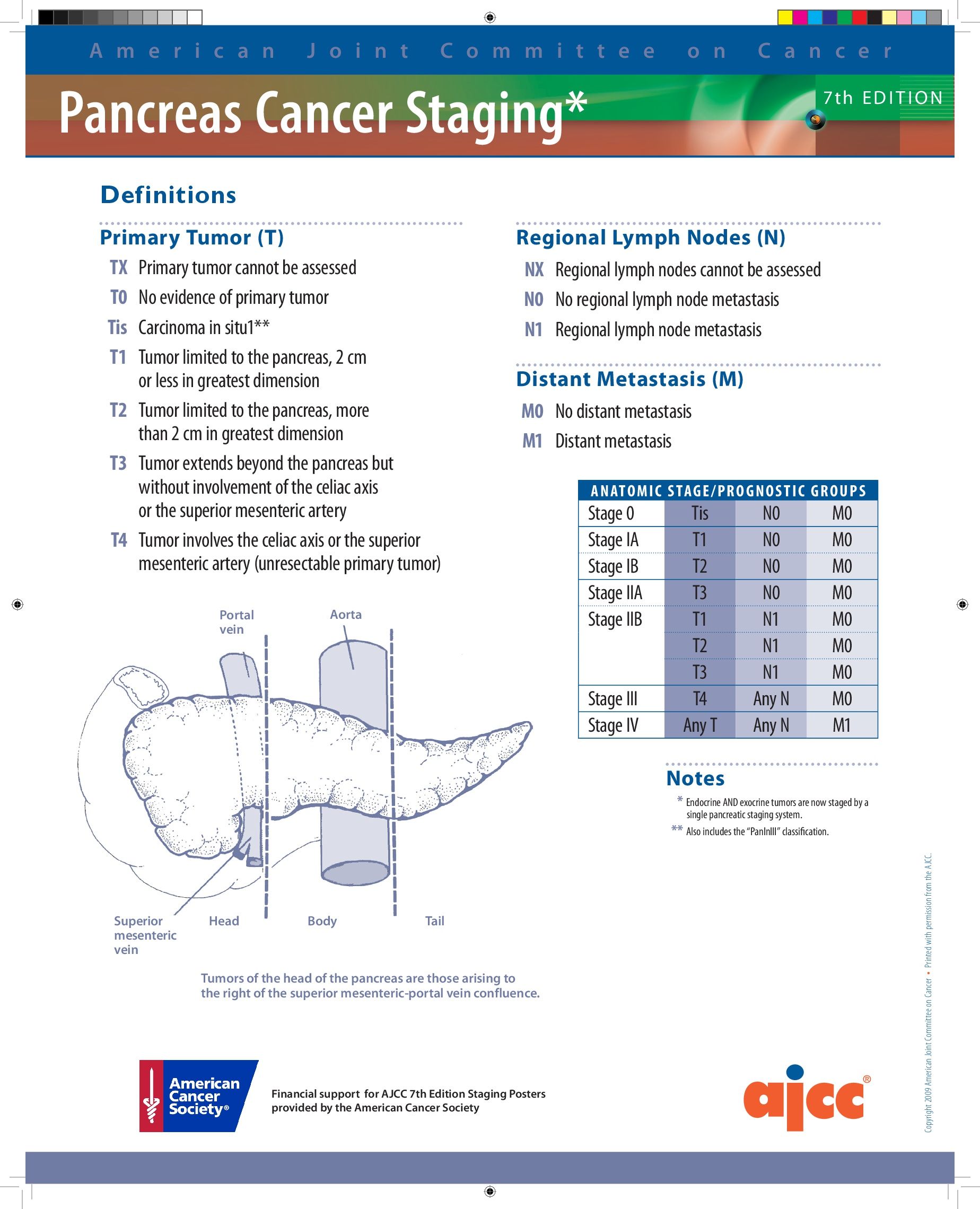
Рисунок 1 | Классификация рака поджелудочной железы по TNM.
TX: Невозможно оценить состояние первичной опухоли
T0: Отсутствуют признаки рака в поджелудочной железе
Tis: Самые начальные проявления рака без распространения опухоли — карцинома in situ
T1: Диаметр опухоли 2 см и менее, находится в пределах поджелудочной железы
T2: Диаметр опухоли более 2 см, находится в пределах поджелудочной железы
T3: Опухоль выходит за пределы поджелудочной железы, но в крупные артерии или вены рядом с органом не проникает
T4: Опухоль выходит за пределы поджелудочной железы и проникает в крупные артерии или вены рядом с органом. Опухоль категории T4 неоперабельна.
NX: Невозможно оценить cостояние регионарных лимфатических узлов.
N0: Отсутствуют признаки рака в регионарных лимфатических узлах.
N1: Опухоль распространяется на регионарные лимфатические узлы.
MX: Невозможно обнаружить отдаленные метастазы.
M0: Опухоль не метастазирует.
M1: В отдаленных органах выявляются метастазы. Рак поджелудочной железы метастазирует преимущественно в печень, легкие и на брюшину.
Стромальный компонент — опухолевое микроокружение — занимает около 70% всей массы опухоли. Строма слабо васкуляризована и обладает высоким интерстициальным давлением. Тем самым данные условия ведут к доминированию наиболее устойчивых, наиболее агрессивных субклонов. Эти субклоны резистентны к химиотерапии и хорошо адаптированы к экстремальным условиям. Таким образом, строма создает мощный барьер для эффективной лекарственной доставки и обеспечивает опухолевым клеткам стимулирующую среду.
Манифестация клинических симптомов происходит на более поздних стадиях, когда вероятность эффективного хирургического лечения составляет лишь 20%. Характер проявлений зависит от локализации патологического процесса. Как говорилось выше, наиболее часто поражается головка поджелудочной железы — в 60-70% случаев. Этой локализации присущи симптомы обтурации общего желчного протока: механическая желтуха, сопровождающаяся кожным зудом; ахоличный кал, темная моча. Присутствует и болевой синдром. В остальных случаях, при поражении тела и хвоста патогномоничным симптомом является наличие болей и потеря веса. Иногда аденокарцинома дебютирует как острый панкреатит. Среди общих симптомов также встречаются астения, анорексия, тошнота, рвота, диарея.
При подозрении на аденокарциному поджелудочной железы всем пациентам назначают исследование печеночного профиля. Маркером аденокарциномы служит CA 19-9, который повышается в 75-85% случаев, однако он недостаточно специфичен и не дает основания для постановки точного диагноза. Тем не менее, повышение данного маркера свидетельствует о рецидиве заболевания после оперативного лечения.
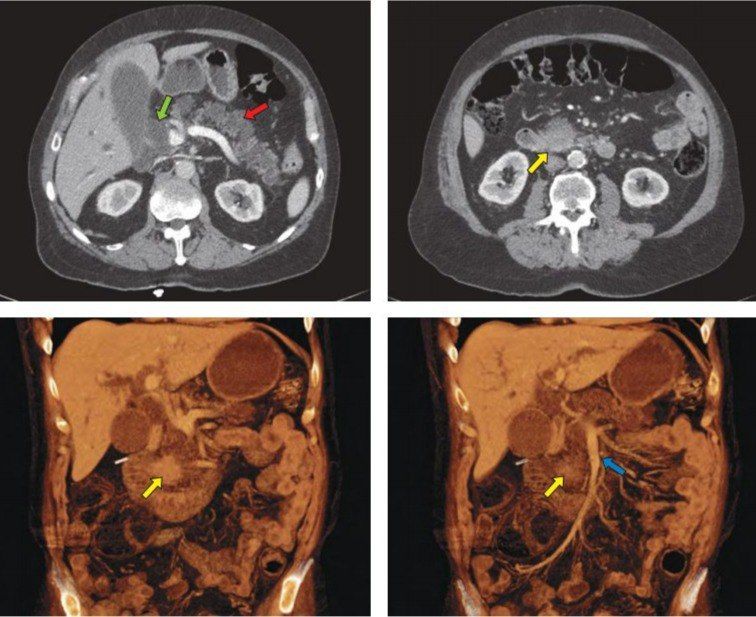
Золотым стандартом среди инструментальных методов исследования является компьютерная томография. Помимо этого диагностической ценностью обладают магнитно-резонансная холангиопанкреатография, эндоскопическая ретроградная холангиопанкреатография, абдоминальное УЗИ, чрескожная чреспечёночная холангиография, эзофагогастродуоденоскопия. Целью исследований является выяснение степени распространения опухоли, инвазии в окружающие ткани, наличия метастазов. По поводу биопсии ведутся споры: считается, что вмешиваться нужно, если возникла обтурационная желтуха, либо в том случае, когда опухоль достигла существенных размеров или дала распространенные метастазы. В таком случае биопсия нужна для определения тактики химиотерапии.
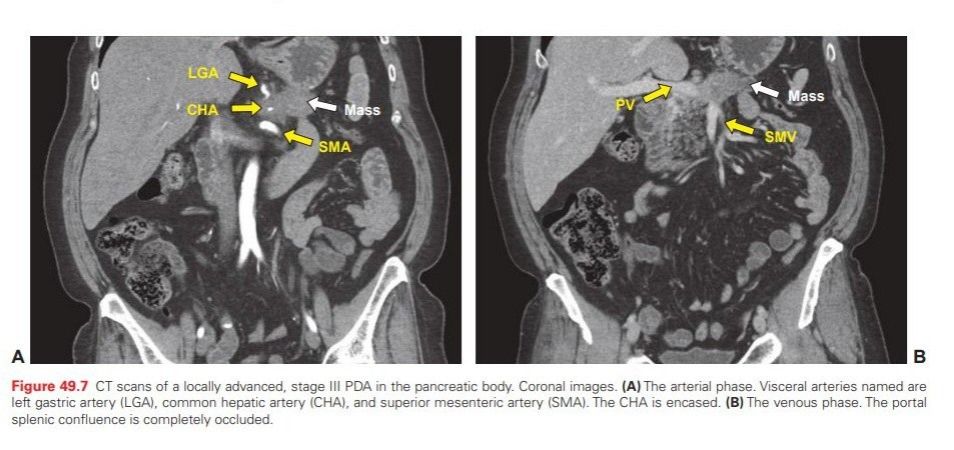
Терапия аденокарциномы поджелудочной железы проводится комплексно. Наиболее обнадеживающим является хирургическое лечение. К сожалению, на момент выявления опухоль чаще всего достигает значительных размеров, прорастая в рядом расположенные сосуды, и радикальная операция становится невозможна. Исходя из этого, предлагают следующие критерии, наличие которых допускает возможность резектабельности: отсутствие метастазов; отсутствие или небольшое вовлечение в опухолевый процесс крупных сосудов; при вовлечении вен должна иметься возможность их реконструкции; пациент должен быть в состоянии перенести оперативное вмешательство. При поражении головки поджелудочной железы производят процедуру Whipple — панкреатодуоденэктомию. В случае поражения тела и хвоста проводят дистальную панкреатэктомию.
Химиотерапия проводится в двух вариантах: адъювантном и неоадъювантном. Неоадъювантная терапия позволяет уменьшить размеры опухоли, более четко разграничить здоровые и пораженные ткани, для того чтобы хирургическая операция имела больше шансов на успех. Адъювантная химиотерапия, согласно рекомендациям Национальной всеобщей онкологической сети, рекомендована пациентам, хорошо перенесшим резекцию. При нерезектабельной опухоли и отдаленных метастазах проводят паллиативную химиотерапию. Лучевая терапия — довольно неоднозначный метод лечения. Существуют различные данные об ее эффективности. В некоторых случаях вред, причиняемый здоровым тканям поджелудочной железы и окружающим органам превышает и без того незначительную эффективность. Однако иногда неоадъювантная лучевая терапия достаточно успешно уменьшает размеры опухоли, обеспечивая ее резектабельность.
Возлагаются большие надежды на таргетную и иммунную терапию. Активно изучаются методы воздействия на онкоген K-ras. Таргетное уменьшение размеров стромы снизит злокачественность и позволит с большей эффективностью проводить лечение аденокарциномы поджелудочной железы.
Разрабатываются вакцины, эффективность которых уже начали испытывать. Прогноз при протоковой аденокарциноме поджелудочной железы неблагоприятный. Пятилетняя выживаемость достигает 7,2%. У прооперированных пациентов она может возрастать до 22%.
Источники
Devita Jr V. T., Lawrence T., Rosenberg S. A. Cancer: Principles & Practice of Oncology: Annual Advances in Oncology. – Lippincott Williams & Wilkins, 2012.
Pancreatic Ductal Adenocarcinoma [Электронный ресурс]. – Режим доступа: https://www.pancreapedia.org/reviews/pancreatic-ductal-adenocarcinoma, свободный. – Загл. с экрана.
Pancreatic Cancer Treatment (PDQ®)–Patient Version [Электронный ресурс]. – Режим доступа: https://www.cancer.gov/types/pancreatic/patient/pancreatic-treatment-pdq#section/_162, свободный. – Загл. с экрана.
Stark A. P. et al. Long-term survival in patients with pancreatic ductal adenocarcinoma //Surgery. – 2016. – Т. 159. – №. 6. – С. 1520-1527.
Источник



