Гуморальная регуляции поджелудочной железы
Опубликовано: 15 октября 2014 в 10:28
 Регуляция работы поджелудочной железы – важный процесс, который позволяет контролировать реализацию основных функций и задач данного органа. В чем же заключаются особенности этого механизма, и почему его роль столь значительна?
Регуляция работы поджелудочной железы – важный процесс, который позволяет контролировать реализацию основных функций и задач данного органа. В чем же заключаются особенности этого механизма, и почему его роль столь значительна?
Гуморальная регуляция осуществляется за счет желез внутренней секреции, выделяющих соответствующие гормоны: соматостатин, глюкагон, и, конечно же, инсулин. При этом именно последний является одним из основных предназначений поджелудочной железы, а регуляция его количества актуальна для обеспечения полноценной жизнедеятельности человека. Благодаря данной функции регулируется обмен веществ в организме и обеспечивается его полноценное функционирование.
Стоит отметить, что также основная задача регуляции работы железы заключается в выделении панкреатического сока, предназначенного для последующего расщепления и переваривания пищи. При этом очень важно, дабы поджелудочный сок выделялся в том количестве, которое требуется для последующего пищеварительного процесса. Если же его объемы будут превышать нормальные показатели, то соответственно, будет нанесен вред и непосредственно поджелудочной, а также всему пищеварительному тракту, доставляя его обладателю серьезный дискомфорт.
Важно понимать, что гуморальная регуляция необходима организму в первую очередь еще и потому, что именно за счет её полноценной работы обеспечивается реализация тех функций, которые она выполняет и для которых предназначена, в полном объеме.
Если же функции, реализуемые поджелудочной железой, не выполняются в полно объеме, то велика вероятность, что в итоге это отразиться не только на органах желудочно-кишечного тракта. Нередко в организме увеличивается количество глюкозы, снижается количество гормонов, столь важных для человеческой жизнедеятельности, а в некоторых случаях расстройство процесса гуморальной регуляции может повлиять даже на органы дыхания, обернувшись возникновением серьезных заболеваний и недугов.
Что и говорить, регуляция работы поджелудочной железы важный механизм, без которого невозможно представить себе полноценное функционирование организма. Именно поэтому столь важно, дабы данная функция исправно выполнялась и в работе не только отдельных органов, но и всего желудочно-кишечного тракта не возникало, ни малейших сбоев или сложностей.
Нейрогуморальная регуляция поджелудочной железы
Нейрогуморальный механизм регуляции — это комплекс факторов, изменяющих внешне- и внутрисекреторную функцию поджелудочной железы (ПЖ). Блуждающий нерв, усиливающий секрецию, парасимпатическая стимуляция в основном отвечают за нервный механизм регуляции. Тормозят выработку сока ПЖ симпатические нервы, угнетается секреторная функция при болях, уменьшении кровоснабжения железы, вызванном сужением сосудов. Такой же эффект наблюдается во время сна, при значительных физических усилиях и умственной работе.
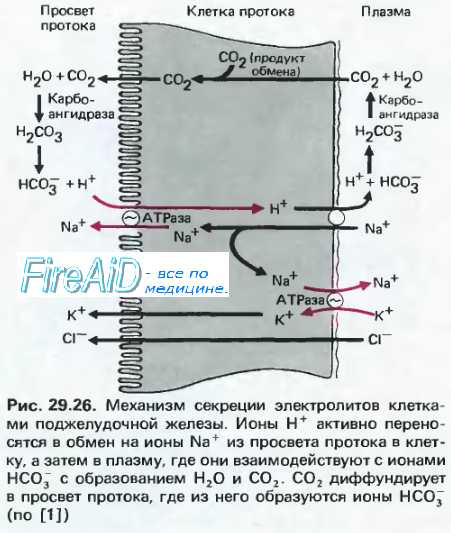
Гуморальная регуляция связана с выработкой стимулирующих секрецию гормонов – секретина и холецистокинина (ХЦК). Под влиянием ХЦК выделяемый сок обогащается ферментами, а секретин повышает количество бикарбонатов, нейтрализующих кислую реакцию. Внешнесекреторная функция железы усиливается под воздействием гастрина, серотонина, солей желчных кислот, инсулина. Состав потребляемых человеком продуктов питания тоже влияет на количество ферментов, присутствующих в соке поджелудочной железы.
 Напомним, что внутрисекреторная функция ПЖ заключается в выработке большой группы важнейших эндогормонов, в том числе инсулина, гастрина, серотонина, глюкагона, панкреатического полипептидаи других активных соединений. При заболеваниях поджелудочной железы проявляется взаимозависимость основных процессов нейрогуморальной регуляции. Например, хронический панкреатит ведет к ее нарушению, формированию внешнесекреторной недостаточности.
Напомним, что внутрисекреторная функция ПЖ заключается в выработке большой группы важнейших эндогормонов, в том числе инсулина, гастрина, серотонина, глюкагона, панкреатического полипептидаи других активных соединений. При заболеваниях поджелудочной железы проявляется взаимозависимость основных процессов нейрогуморальной регуляции. Например, хронический панкреатит ведет к ее нарушению, формированию внешнесекреторной недостаточности.
Патология, связанная с выработкой сока для улучшения пищеварения, одновременно вызывает изменение внутрисекреторной активности. Причина в том, что гормоны, регулирующие экзокринную функцию ПЖ, стимулируют выработку инсулина. Среди болезней ПЖ, вызывающих развитие сахарного диабета, 76 % приходится на хронический панкреатит.
Большое количество гормонов, наличие нервной и гуморальной регуляций функций поджелудочной железы усложняют работу этого важного органа. Только понимание взаимосвязи происходящих явлений позволит успешно лечить панкреатит, диабет и ожирение.
Источник
Оглавление темы «Сокращение желудка. Пищеварительные функции поджелудочной железы. Функции печени.»: Нервная регуляция секреторной функции поджелудочной железы. Гуморальная ( гормональная ) регуляция секреции поджелудочной железы.Слабое сокоотделение натощак резко усиливается во время (через 2— 3 мин) и после приема пищи. В привычных условиях приема пищи панкреатическое сокоотделение начинается уже на вид, запах пищи и другие раздражители, сопутствующие приему пищи, что свидетельствует об условно-рефлекторном механизме секреции. При раздражении пищевыми веществами рецепторов слизистой оболочки ротовой полости, глотки и пищевода возникает безусловно-рефлекторное отделение панкреатического сока. Нервные импульсы от раздражаемых рецепторов по афферентным путям достигают бульбарного центра панкреатической секреции, где они переключаются на преганглионарные нейроны ядер блуждающего нерва, по эфферентным волокнам которого достигают постганглионарных нейронов. Их аксоны образуют синаптические окончания на базальных мембранах панкреацитов. Выделяющийся при возбуждении этих окончаний ацетилхо-лин активирует М-холинорецепторы постсинаптической мембраны. При этом освобождаются вторичные посредники (Са++ и ГЦ-цГМФ), которые и вызывают секреторную деятельность панкреоцитов и эпителиальных клеток протоков. При раздражении чревных нервов, осуществляющих симпатическую иннервацию поджелудочной железы, ее сокоотделение тормозится (за счет активации р-адренорецепторов медиатором норадреналином). Но торможение секреции сопровождается накоплением секреторного материала в панкреацитах.
Поступление пищи в желудок во время приема пищи вызывает раздражение хемо- и механорецепторов желудка, что приводит к продолжению безусловно-рефлекторного сокоотделения поджелудочной железой, вызванного стимуляцией рецепторов ротовой полости. Поступление в двенадцатиперстную кишку желудочного содержимого вызывает наряду с дуоденопанкреатическим секреторным рефлексом (с рецепторов слизистой оболочки) выделение из эндокринных клеток гастро-интестинальных гормонов, стимулирующих или тормозящих сокоотделение поджелудочной железой. Роль основных гуморальных регуляторов выполняют секретин и ХЦК, которые вырабатываются S- и ССК-клетками слизистой оболочки двенадцатиперстной кишки. Секретин и ХЦК усиливают влияние друг друга на панкреоциты, особенно на фоне выделения ацетилхолина в синаптических окончаниях холинергических нервных волокон, иннервирующих железу. Важным гуморальным возбудителем панкреатической секреции является гастрин, выделяемый У-клетками слизистой оболочки антрального отдела желудка. Возбуждающее влияние этих гормонов подкрепляется бомбезином, серотонином и инсулином. Тормозят выделение сока соматостатин, глюкагон, энкефалины, вещество Р, ТИП, ПП, а также кальцитонн и АКТГ. Но их роль в комплексной гуморальной регуляции поджелудочной железы изучена недостаточно. — Также рекомендуем «Секреция сока поджелудочной железы. Фазы ( этапы ) секреции сока поджелудочной железы.» |
Источник
Слабое сокоотделение натощак резко
усиливается во время (через 2— 3 мин) и
после приема пищи. Панкреатическое
сокоотделение начинается уже на вид,
запах пищи как условно-рефлекторный
механизме секреции. При раздражении
пищевыми веществами рецепторов слизистой
оболочки ротовой полости, глотки и
пищевода возникает безусловно-рефлекторное
отделение панкреатического сока. Нервные
импульсы от раздражаемых рецепторов
по афферентным путям достигают бульбарного
центра панкреатической секреции, где
они переключаются на преганглионарные
нейроны ядер блуждающего нерва, по
эфферентным волокнам которого достигают
постганглионарных нейронов. Их аксоны
образуют синаптические окончания на
базальных мембранах панкреацитов.
Выделяющийся при возбуждении этих
окончаний ацетилхолин активирует
М-холинорецепторы постсинаптической
мембраны.
При раздражении чревных нервов,
осуществляющих симпатическую иннервацию
поджелудочной железы, ее сокоотделение
тормозится (за счет активации
р-адренорецепторов медиатором
норадреналином). Но торможение секреции
сопровождается накоплением секреторного
материала в панкреацитах.
Поступление пищи в желудок во время
приема пищи вызывает раздражение хемо-
и механорецепторов желудка.
Поступление в двенадцатиперстную кишку
желудочного содержимого вызывает вместе
с дуоденопанкреатическим секреторным
рефлексом (с рецепторов слизистой
оболочки) выделение из эндокринных
клеток гастро-интестинальных гормонов,
стимулирующих или тормозящих сокоотделение
поджелудочной железой.
Роль основных гуморальных регуляторов
выполняют секретин и ХЦК, которые
вырабатываются S- и ССК-клетками слизистой
оболочки двенадцатиперстной кишки.
Секретин и ХЦК усиливают влияние друг
друга на панкреоциты, особенно на фоне
выделения ацетилхолина в синаптических
окончаниях холинергических нервных
волокон, иннервирующих железу. Важным
гуморальным возбудителем панкреатической
секреции является гастрин.
4) Изменится ли амплитула потенциала действия нервной клетки, если на нее воздейсвовать стимулами сверхпороговой силы
это возбудимые ткани, амплитуда не
измен: так как действует закон «Все или
ничего»
Билет № 5
1.потенциал действия,с графиком,
возбудимость,мера возбудимости,
Потенциал
действия (ПД) – быстрое изменение
мембранного потенциала в ответ на
действия раздражителя пороговой силы.
ПД имеет стандартные амплитуду и
временные параметры, не зависящие от
силы стимула — правило «ВСЕ ИЛИ НИЧЕГО».
Начальная деполяризация мембраны под
действием раздражителя:

Если сила раздражителя достаточна,
чтобы деполяризовать мембрану до КУД,
открываются быстрые потенциал-зависимые
натриевые каналы. Клетка возбуждена –
возник нервный импульс.

Восстановление мембранного потенциала
покоя — реполяризация мембраны.

Следующий этап – восстановление
мембранного потенциала покоя —
реполяризация, обусловлена активным
ионным транспортом. Наиболее важен
процесс активного транспорта — это
работа Na/K- насоса, который выкачивает ионы натрия
из клетки, одновременно закачивая ионы
калия внутрь клетки. Восстановление
мембранного потенциала происходит
благодаря току ионов калия из клетки –
калиевые каналы активируются и пропускают
ионы калия до достижения равновесного
калиевого потенциала. Это процесс важен
потому, что до тех пор, пока не восстановлен
МПП, клетка не способна воспринимать
новый импульс возбуждения.
ГИПЕРПОЛЯРИЗАЦИЯ — кратковременное
увеличение МП после его восстановления,
которое обусловлено повышением
проницаемости мембраны для ионов калия
и хлора. Гиперполяризация бывает только
после ПД.
Деполяризация мембраны до КУД – могут
открыться любые натриевые каналы,
иногда кальциевые, и быстрые, и медленные,
и потенциал-зависимые, и рецептор-управляемые.
Это зависит от вида раздражителя и типа
клетокБыстрое поступление натрия в клетку —
открываются быстрые, потенциал-зависимые
натриевые каналы, и деполяризация
достигает точки реверса потенциала –
происходит перезарядка мембраны, знак
заряда меняется на положительный.Восстановление градиента концентрации
по калию – работа насоса. Калиевые
каналы активированы, калий переходит
из клетки во внеклеточную среду –
реполяризация, начинается восстановление
МППСледовая деполяризация, или отрицательный
следовой потенциал — мембрана еще
деполяризована относительно МПП.Следовая гиперполяризация. Калиевые
каналы остаются открытыми и дополнительный
ток калия гиперполяризует мембрану.
После этого клетка возвращается к
исходному уровню МПП. Длительность ПД
составляет для разных клеток от 1 до
3-4 мс.

Обратите внимание на три величины
потенциала, важные и постоянные для
каждой клетки ее электрические
характеристики.
МПП — электроотрицательность мембраны
клетки в покое, обеспечивающая способность
к возбуждению — возбудимость.КУД — критический уровень, величина
мембранного потенциала, при достижении
которой открываются быстрые, потенциал
зависимые натриевые каналы и происходит
перезарядка мембраны за счет поступления
в клетку положительных ионов натрия.
Чем выше электроотрицательность
мембраны, тем труднее деполяризовать
ее до КУД, тем менее возбудима такая
клетка.Точка реверса потенциала (овершут) —
такая величина положительного мембранного
потенциала, при которой положительно
заряженные ионы уже не проникают в
клетку — кратковременный равновесный
натриевый потенциал.
При действии раздражителя
подпороговой силы возникает неполная
деполяризация — ЛОКАЛЬНЫЙ ОТВЕТ (ЛО).
Неполная, или частичная деполяризация
– это такое изменение заряда мембраны,
которое не достигает критического
уровня деполяризации (КУД).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Регуляция
секреции поджелудочного сока осуществляется
в 3 фазы:
1.
Мозговая (сложнорефлекторная) фаза.
Осуществляется через комплекс условных
и безусловных рефлексов. Вид, запах и
вкус пищи активируют нейронывагусав центре регуляции панкреатической
секреции. Окончания вагуса в поджелудочной
железе выделяютацетилхолин,
который стимулирует синтез панкреатического
сока.
2.
Желудочная (нейро-гуморальная) фаза.
Возникает при нахождении пищи в желудке.
За счетвагуса, гастрина,
серотонинастимулируется секреция
поджелудочного сока.
3.
Кишечная фаза.Кислый
химус вызывает в кишечнике
выделение S-клетками секретина
(белковый гормон). Секретин
поступают
в кровь и
стимулирует выделение из поджелудочной
железы в тонкий кишечник панкреатического
сока, содержащего много НСО3-,
что нейтрализует
НС1 желудочного сока и ингибирует пепсин.
В результате рН возрастает
от 1,5-2,0 до 7,0.
Поступление
пептидов в тонкий кишечник вызывает
секрецию холецистокинина
(белкового гормона) в I-клетках,
который стимулирует
выделение панкреатического сока с
большим содержанием ферментов.
Регуляция кишечной секреции
Регуляция
деятельности желез тонкой кишки
осуществляется местными нервно-рефлекторными
механизмами, а также гуморальными
влияниями и ингредиентами химуса.
Механическое раздражение слизистой
оболочки тонкой кишки вызывает выделение
жидкого секрета с малым содержанием
ферментов. Местное раздражение слизистой
кишки продуктами переваривания белков,
жиров, соляной кислотой, панкреатическим
соком вызывает отделение кишечного
сока, богатого ферментами. Усиливают
кишечное сокоотделение ГИП, ВИП, мотилин.
Гормоны энтерокринин и дуокринин,
выделяемые слизистой оболочкой тонкой
кишки, стимулируют соответственно
секрецию либеркюновых и бруннеровых
желез. Тормозное действие оказывает
соматостатин.
Мотилин
(в Мо-клетках) — стимулирует активность
гладко-мышечной клеток кишечника.
6. Всасывание аминокислот в кишечнике
Всасывание
L-аминокислот
(но не D)
— активный
процесс, в результате которого аминокислоты
переносятся через кишечную стенку
от слизистой её поверхности в кровь.
Известно
пять
специфических транспортных
систем, каждая из которых функционирует
для переноса определённой группы близких
по
строению аминокислот:
нейтральных,
короткой боковой цепью (аланин,
серии, треонин);нейтральных,
с длинной или разветвлённой боковой
цепью (валин, лейцин, изолейцин);с
катионными радикалами (лизин, аргинин);с
анионными радикалами (глутаминовая и
аспарагиновая кислоты);иминокислот
(пролин, оксипролин).
Существуют
2 основных механизма переноса аминокислот:
симпорт с натрием и γ-глутамильный
цикл.
1.
Симпорт аминокислот с Na+.
Симпортом
с Nа+
переносятся аминокислоты из первой и
пятой группы, а также метионин.
L-аминокислота
поступает в энтероцит путём симпорта
с ионом Na+.
Далее специфическая транслоказа
переносит аминокислоту
через мембрану в кровь. Обмен ионов
натрия между
клетками осуществляется путём
первично-активного транспорта
с помощью Na+,
К+-АТФ-азы.
2.
γ-Глутамильный цикл.
γ-глутамильный
цикл переносит некоторые
нейтральные аминокислоты (фенилаланин,
лейцин) и аминокислоты с катионными
радикалами (лизин)
в кишечнике, почках и, по-видимому,
мозге.
В
этой системе участвуют 6 ферментов, один
из
которых находится в клеточной мембране,
а остальные
— в цитозоле.
Мембранно-связанный
фермент γ-глутамилтрансфераза
(гликопротеин)
катализирует перенос
γ-глутамильной группы от глутатиона на
транспортируемую
аминокислоту и последующий
перенос комплекса в клетку. Амнокислота
отщепляется
от у-глутамильного
остатка под действием фермента
у-глутамилциклотрансферазы.
Дипептид
цистеинилглицин расщепляется под
действием
пептидазы на 2 аминокислоты — цистеин
и глицин. В результате этих 3 реакций
происходит перенос одной молекулы
аминокислоты в
клетку (или внутриклеточную структуру).
Следующие
3 реакции обеспечивают регенерацию
глутатиона,
благодаря чему цикл повторяется
многократно.
Для транспорта в клетку одной молекулы
аминокислоты с участием у-глутамильного
цикла затрачиваются 3 молекулы АТФ.
Поступление
аминокислот в организм осуществляется
двумя путями:
через воротную систему печени, ведущую
прямо
в печень, и по лимфатическим сосудам,
сообщающимся
с кровью через грудной лимфатический
проток. Максимальная концентрация
аминокислот в крови
достигается через 30—50 мин
после приёма белковой пищи (углеводы и
жиры
замедляют всасывание аминокислот).
Аминокислоты
при всасывании конкурируют друг с другом
за специфические
участки связывания. Например, всасывание
лейцина (если концентрация его достаточно
высока) уменьшает всасывание изолейцина
и валина.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник