Эндокринный рак поджелудочной железы
- Определение патологии
- Типы опухолей
- Причины развития
- Основные проявления
- Методы диагностирования
- Тактика и стратегия лечения
- Современное лечение нейроэндокринных опухолей в Бельгии
- Возможные осложнения
- Критерии прогноза
- Меры профилактики
Что такое нейроэндокринная опухоль поджелудочной железы
Панкреатические нейроэндокринные новообразования (ПНЭН) представляют собой группу разных по происхождению, строению и клиническим проявлениям неоплазий (опухолей). В зависимости от того, могут ли эти опухоли секретировать гормоны и амины, вызывая карциноидный и другие клинические синдромы, их можно отнести к функциональным (Ф-НЭН) и нефункциональным (НФ-НЕН).
Нейроэндокринные новообразования поджелудочной железы — наиболее распространенные нейроэндокринные опухоли.
Большинство ПНЭН имеют низкую степень злокачественности, но обладают злокачественным потенциалом. Они растут медленно и остаются стабильными в течение многих лет, по крайней мере, когда они небольшого размера. Однако без лечения, большинство таких опухолей растет и в конечном итоге метастазирует в печень
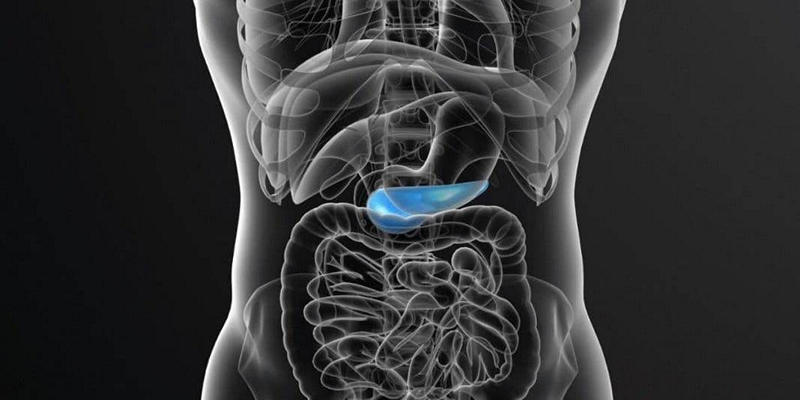
Новообразования поджелудочной железы в целом встречаются редко:<2% всех опухолей поджелудочной железы. Их диагностика и локализация часто требуют серьезных технологий, а их успешное лечение требует тщательного междисциплинарного подхода.
По этим причинам пациент с возможной или подтвержденной эндокринной опухолью поджелудочной железы лучше всего лечится в большом многопрофильном центре, где есть эндокринологи, гастроэнтерологи, хирурги поджелудочной железы и медицинские онкологи.
Классификация
Под термином нейроэндокринная опухоль поджелудочной железы обычно понимают инсулиному, гастриному или глюкагоному. Иногда к этой тройке добавляются более редкие VIPомы и соматостаниомы.
ПНЭН определяются как функциональные или нефункциональные в зависимости от того, вызывают ли они синдром гормональной гиперсекреции — избыточной продукции гормонов.
Из всех функциональных ПНЭН гастриномы и инсулиномы самые распространенные. Другие неоплазии обычно рассматриваются вместе как группа, называемая «редкими функциональными ПНЭН».
Несколько таких редких клинических синдромов были предложены в качестве возможных функциональных ПНЭН. К ним относятся следующие:
- кальцитонинома;
- паратиринома;
- опухоль, секретирующая гормон роста, секретирующая неоплазия (GRFoma);
- адренокортикотропин-гормон-секретирующая неоплазия (ACTHoma);
- нейротензинома.
По данным европейских и американских онкологов нефункциональные ПНЭН встречаются чаще, чем функциональные. Первые обычно диагностируются в четвертом или пятом десятилетиях жизни и часто уже метастазируют в печень на момент постановки диагноза.

Причины появления
10% функциональных НЭН становятся проявлением наследственных семейных эндокринных опухолей:
- синдром множественной эндокринной неоплазии 1 типа (MEN1);
- болезнь фон Гиппеля-Линдау (VHL);
- нейрофиброматоз типа 1 (NF-1);
- туберозный склероз (TSC).
Причина развития этих пакнкреатических нейроэндокринных новообразований — наследственное выключение в соответствующего гена-супрессора опухоли в ходе внутриутробного развития.
Хотя устаревший термин «опухоль островковых клеток» часто используется и сейчас для идентификации новообразований эндокринной поджелудочной железы — это неправильное название. Многие нейроэндокринные опухоли поджелудочной железы не развиваются непосредственно из островковых клеток.
Большинство таких новообразований возникают из стволовых клеток APUD. Это клетки-предшественники из которых впоследствии образуются все типы тканей поджелудочной железы. Они находятся в эпителии протоков этого органа.
Тот факт, что многие гастриномы и соматостатиномы находятся вблизи железистой ткани поджелудочной железы, но не внутри нее, подтверждает мнение о возможном внепанкреатическом развитии этих новообразований.
Симтомы болезни
Функциональные опухоли приводят к синдромам гормональной гиперсекреции.
Неоплазия | Симптом (ы) |
Инсулинома | Гипогликемия — снижение уровня глюкозы в крови. Потливость, слабость, тремор, чувство голода и т.д. |
Гастринома (ульцерогенная аденома поджелудочной железы) | Проявляется как затяжная язвенная болезнь желудка, плохо поддающаяся лечению — боли в животе, тошнота, рвота и т.д. |
VIPома | Неукротимый понос, снижение уровня калия в крови, снижение кислотности желудочного сока, обезвоживание, похудение. |
Глюкагонома | Непереносимость глюкозы, дерматит, стоматит, глоссит, тромбоз глубоких вен, депрессия, сердечная недостаточность. |
Соматостатинома | Симптомы сахарного диабета и желчнокаменной болезни, стеаторея, ахлоргидрия. |
Нефункциональные новообразования вызывают неспецифические симптомы, такие как неопределенная боль в животе, и обычно выявляются случайно.
Различия между функциональными и нефункциональными ПНЭН основано на клинических проявлениях, и нет абсолютной разницы в выражении гормонов между функциональными и нефункциональными ПНЭН.
Например, опухолевые клетки в небольшом ПНЭН могут экспрессировать глюкагон, что приводит к пограничному повышению уровней глюкагона. Клинически, однако, эта ПНЭН определяется как нефункциональная, потому что небольшого повышения глюкагона недостаточно, чтобы вызвать синдром глюкагономы.
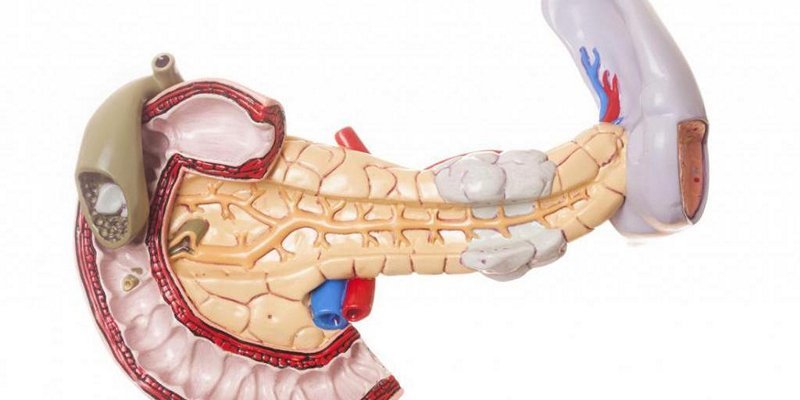
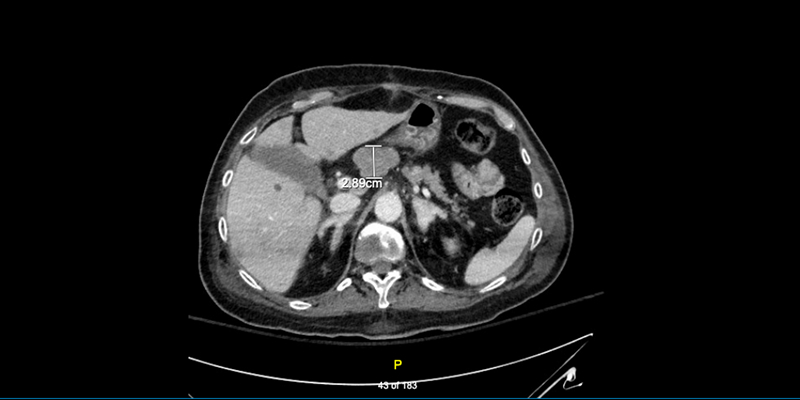
Диагностика
Поскольку для распознавания синдрома гормональной гиперсекреции требуется значительный клинический опыт, а симптомы нефункциональных опухолей неспецифические, диагностика ПНЭН часто происходит довольно поздно.
Эндокринное тестирование, визуализация и гистологические данные необходимы для точной диагностики ПНЭН.
Полная диагностика должна установить природу ПНЭН, оценить степень опухоли, определить первичные и метастатические очаги и определить, функционирует ли опухоль. Если подозревается синдром гормональной гиперсекреции, проводится соответствующее биохимическое исследование для его определения, а затем уже визуализация, эндоскопия и биопсия.
Если опухоль в поджелудочной железе или печени случайно идентифицируются с помощью визуализации, они обычно подвергаются биопсии для подтверждения наличия ПНЭН. Биохимическое тестирование в идеале проводится, даже если синдром гормональной гиперсекреции не очевиден, поскольку он может быть на субклинической стадии, а гиперсекретированные гормоны могут использоваться в качестве маркеров опухоли во время последующих оценок.
Лечение
Лечение у пациентов с нейроэндокринными новообразованиями поджелудочной железы проводят индивидуально, чтобы сбалансировать эффекты гиперсекреции гормонов. Многие эндокринные опухолевые синдромы поджелудочной железы потенциально опасны для жизни. Поэтому, первоначальная медикаментозная терапия направлена на стабилизацию состояния пациента, чтобы обеспечить полную предоперационную оценку.
Все резектабельные функциональные или нефункциональные ПНЭН рекомендуется лечить хирургическим путем. Используются разные типы оперативного вмешательства:
- энуклеация опухоли (удаление видимой части новообразования с сохранением здоровой ткани органа);
- энуклеация в сочетании с резекцией ПЖ;
- дистальная резекция поджелудочной железы;
- панкреатодуоденэктомия (удаление ПЖ и части кищечника);
- и т.д.
Тип хирургического вмешательства определяется индивидуально, исходя из особенностей конкретного заболевания у конкретного пациента. В то же время нейроэндокринный рак поджелудочной железы требует обязательного иссечения лимфатических узлов.
Все резектабельные инсулиномы должны быть удалены хирургическим путем, несмотря на размер опухоли. 85–90% пациентов с этим типом ПНЭН могут быть вылечены полностью таким способом. Инсулиномы составляют примерно 35–40% функциональных ПНЭН. Из них злокачественные инсулиномы составляют только около 5–10% от общего количества.
Системная терапия необходима пациентам с остаточным заболеванием после операции и для лечения неоперабельных опухолей.
Против функциональных ПНЭН эффективны синтетические аналоги гормона соматостатина (гормон роста). Особенно хорошо выражено их действие при VIPомах и глюкагономах.
Нет четких доказательств того, что аналоги соматостатина лечат нефункциональные ПНЭН, но, скорее всего, они способны сдерживать рост опухоли.
В настоящее время доступны два аналога соматостатина, октреотид и ланреотид, и их формы пролонгированного действия, а новый аналог, пасиреотид, пока находится в фазе клинических испытаний с обнадеживающими предварительными результатами.
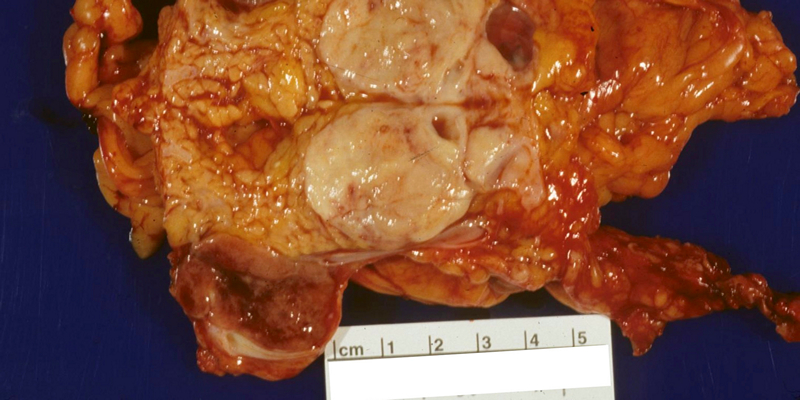
Прогрессивные методы лечения нейроэндокринных панкреатических неоплазий в Бельгии
В клиниках Бельгии используются при лечении ПНЭН современные методы малоинвазивной хирургии, лучевой терапии, биологической терапии и химиотерапии.
В числе микроинвазивных хирургических и радиологических методов:
- радиоактивные полимерные микросферы;
- химиоэмболизация;
- мягкая эмболизация;
- радиочастотная абляция (RFA);
- чрескожная алкогольная абляция;
- микроволновая абляция.
Системный интерферон-α2A применяется в клиниках Бельгии для лечения ПНЭН, которые нечувствительны к аналогам соматостатина.
Ингибитор mTOR эверолимус (RAD001) и ингибитор тирозинкиназы сунитиниб эффективно используются в бельгийских клиниках для замедления прогрессирования неоплазий.
Химиотерапия доступна для неоплазий среднего и высокого уровня злокачественности. Темозоломид и капецитабин — препараты выбора, которые могут применяться у пациентов с быстро прогрессирующими ПНЭН.
Успешно внедряется в практику и разработанный Бельгийскими учеными в сотрудничестве с коллегами из Нидерландов метод Радионуклидной терапии пептидными рецепторами (PRRT) Lutetium Lu 177-dota-tate. Он эффективен против хорошо дифференцированных ПНЭН. Но этот метод пока не получил широкого распространения, поэтому она лучше всего подходит для неоплазий с большим потенциалом злокачественности, которые устойчивы к другим системным методам лечения
Осложнения
У пациентов с эндокринными неоплазиями поджелудочной железы может наблюдаться заболеваемость, связанная с ростом опухоли.
- Пациенты с опухолями в головке поджелудочной железы иногда имеют закупорку желчных путей, закупорку поджелудочной железы или и то, и другое.
- Хроническая боль в животе может возникать из-за сжимающего воздействия большой внутрибрюшной опухоли или обструктивного панкреатита.
Заболеваемость, вызванная эффектами избыточной гормональной продукции функциональными новообразованиями поджелудочной железы, наступает раньше, чем опухолевые эффекты в ходе заболевания.
- При отсутствии лечения у пациентов с инсулиномой могут наблюдаться гипогликемические судороги и даже открытая кома.
- До разработки эффективных антисекреторных препаратов (например, Н2-блокаторов и ингибиторов протонной помпы) у пациентов с гастриномой часто было опасное для жизни желудочно-кишечное кровотечение при язвенной болезни.
- Пациенты с VIPомами рискуют быть обезвожены от диареи. У них также могут развиться фатальные сердечные аритмии могут ввиду связанной гипокалиемии.
- Заболеваемость, связанная с гормональными эффектами глюкагономы, может быть полиморфной. У пациентов может быть диабет, истощение, стоматит и другие признаки, сходные с тяжелым дефицитом питательных веществ.
Прогноз
Прогноз при большинстве типов ПНЭН — благоприятный. Но даже та нейроэндокринная опухоль поджелудочной железы, прогноз при которой считается хорошим, требует постоянного наблюдения. Поскольку усиление скорости роста может стать тревожным фактором, ухудшающим выживаемость.
Поскольку эти опухоли обычно растут медленно и имеют относительно низкий метастатический потенциал, а также потому, что не было определено каких-либо конкретных критериев для прогнозирования их поведения, различия между доброкачественными и злокачественными новообразованиями основано на наличии метастатического заболевания.
Пятилетняя выживаемость при ПНЭН без проведения лечения составляет:
- 80% для всех стадий;
- 90–100% для локализованной болезни;
- 40% для регионарной болезни;
- 29% для отдаленных метастазов.
Долгосрочная специфическая выживаемость (DSS) хирургически резецированных опухолей превышает 50% через 20 лет.
Поскольку даже метастатические эндокринные новообразования поджелудочной железы обычно растут медленно, прогноз у пациентов с этими опухолями является относительно хорошим по сравнению с таковым у пациентов с неэндокринным раком.
Более 90% пациентов с инсулиномами имеют доброкачественные новообразования без признаков метастазов, и до 97% этих пациентов полностью излечиваются хирургической резекцией.
Пациенты с гастриномами имеют худший прогноз. 60% этих опухолей злокачественные. Тем не менее, показатели выживаемости разительно отличаются между пациентами, у которых метастазирование гастриномы ограничено лимфатическими узлами, и пациентами с метастазами в печень, следующим образом:
- пациенты, у которых метастазирование гастриномы включает только лимфатические узлы, могут проживать 25 лет или дольше, и их продолжительность жизни неотличима от таковой у людей без гастриномы.
- пациенты с метастазами в печени имеют 5-летнюю выживаемость 20-30%, по сравнению с 90% у пациентов без метастазов в печени.
Приблизительно половина всех VIPом имеют метастазы на момент постановки диагноза или операции и примерно треть пациентов полностью излечивается хирургическим путем.
Большинство соматостатином (84%) уже метастазируют на момент презентации, но ряд пациентов выживают через 5 лет после комбинированной операции и химиотерапии.
Среди эндокринных неоплазий глюкагономы имеют тенденцию быть относительно большими (5-10 см) при постановке диагноза. Кроме того, до 80% таких неоплазий показывают инвазивный или метастатический рост. Синдром глюкагономы у большинства пациентов распознается относительно поздно, и хирургическое лечение возможно менее чем у 20% всех пациентов. В связи с этим такая нейроэндокринная опухоль поджелудочной имеет самый серьезный прогноз.
Профилактика
Специфических мер профилактики для нейроэндокринных неоплазий поджелудочной железы не существует.
Получите больше информации о перспективных технологиях лечениях нейроэндокринных неоплазий в Бельгии. Закажите обратный звонок или напишите нам через форму обратной связи.
Источник
Эндокринный рак поджелудочной железы абсолютно преобладает среди злокачественных опухолей органов БПДЗ. В Южной Европе, в большинстве стран Азиатско-Тихоокеанского региона заболеваемость составляет 2,2-6,0 на 100 тыс. населения. В странах Северной Европы и среди небелого населения США заболеваемость достигает 11,0-12,5 на 100 000 населения. Среди белого населения США заболеваемость существенно ниже. Средний возраст заболевших мужчин — 63-65 лет, женщин — 68-69 лет. У мужчин заболеваемость в среднем в 1,5-2 раза выше, чем у женщин. В России абсолютное число заболевших раком поджелудочной железы в 2000 г. составило 13 146 человек, или 2,9% из всех заболевших в этом году злокачественными новообразованиями. И структуре заболеваемости населения России злокачественными новообразованиями в 2000 г. частота рака поджелудочной железы и у мужчин, и у женщин занимала 11-е место.
Рак поджелудочной железы — заболевание с крайне высоким потенциалом злокачественности, поэтому показатель, характеризующий отношение числа впервые заболевших к числу умерших за год практически равен единице. Рак поджелудочной железы крайне редко встречается в возрасте до 30 лет. Рост выявляемости рака поджелудочной железы в какой-то мере можно объяснить повышенным вниманием к этой проблеме в последние десятилетия, а также улучшением медицинского обслуживания населения, появлением надежных методов диагностики, в последние годы как среди европейского населения (Великобритания, Швеция и т.д.), так и в Азиатском регионе, в частности в Японии, отмечается значительный рост смертности от рака поджелудочной железы.
Подавляющее большинство исследований продемонстрировало явную связь между курением и риском заболевания раком поджелудочной железы. Ряд исследований демонстрирует дозозависимое влияние, т.е. риск увеличивается пропорционально числу выкуренных сигарет. Канцерогенность табачного дыма давно доказана, однако конкретные события в панкреатическом канцерогенезе до конца не известны. Предполагается, что основное значение имеют нитрозосоединения. В последние годы наметился повышенный интерес к установлению связи отдельных факторов питания с увеличением заболеваемости раком поджелудочной железы. Выявлен ряд факторов питания, способных влиять на заболеваемость раком поджелудочной железы, но эта связь основана больше на эмпирических наблюдениях, чем подтверждена какими-либо специфическими биологическими механизмами.
Еще одним пищевым продуктом, который привлекает внимание шидемиологов, является мясо. Большинство авторов подобную связь объясняет наличием жира в мясных продуктах. Другим возможным объяснением стало обнаружение появляющихся при кулинарной обработке мяса N-нитрозосоединений и ароматических белков, которые обладают канцерогенными свойствами.
Итак, представляется, что потребление фруктов и овощей приводит к снижению риска возникновения рака поджелудочной железы, а избыточное потребление мяса, возможно, увеличивает этот риск. Влияние употребления кофе и алкоголя на повышение заболеваемости раком поджелудочной железы не доказано.
Некоторые профессиональные вредности могут увеличить риск возникновения рака поджелудочной железы на 26%. К ним относятся: алюминиевое производство, ионизирующее излучение, ряд химических производств, связанных со стиролом, и некоторые виды пестицидов.
Многие хирурги склонны считать, что диабет — один из симптомов рака поджелудочной железы, а не фактор риска его развития. Подобный взгляд на взаимоотношения диабета и рака поджелудочной железы базируется на простых исследованиях, когда зачастую у больных раком поджелудочной железы диабет выявлялся незадолго до обнаружения рака. Возникновение диабета вряд ли можно объяснить прямым опухолевым поражением эндокринной части поджелудочной железы, но можно представить, что рост опухоли может вызвать нарушение метаболизма глюкозы и, определенно, в ряде случаев при раке поджелудочной железы может возникнуть диабет. Когда же речь идет о длительно существующем диабете (> 5 лет), имеются неопровержимые доказательства того, что диабет увеличивает риск возникновения рака поджелудочной железы. У больных хроническим панкреатитом также повышен риск заболевания раком поджелудочной железы.
Классификация опухолей поджелудочной железы
Последняя патологоанатомическая классификация опухолей поджелудочной железы, предложенная патологами США (Solcia Е. et al. 1997), основана на современной патологоанатомической диагностике опухолей и в значительной степени отражает клиническое течение и прогноз заболевания. Классификация, по сути, является клинико-патологоанатомической, чем выгодно отличается от любых гистологических классификаций опухолей поджелудочной железы.
1. Первичные опухоли поджелудочной железы
1.1. Опухоли экзокринной ткани поджелудочной железы
1.1.1. Доброкачественные опухоли поджелудочной железы (серозная цистаденома, муцинозная цистаденома, внутрипротоковая папиллярная муцинозная аденома, зрелая кистозная тератома)
1.1.2. Пограничные опухоли поджелудочной железы (муцинозная кистозная опухоль с умеренно выраженной дисплазией, внутрипротоковая папиллярно-муцинозная опухоль с умеренно выраженной дисплазией, солидная псевдопапиллярная опухоль)
1.1.3. Злокачественные опухоли поджелудочной железы
1.1.3.1. Протоковая аденокарцинома; редкие микроскопические формы протоковой аденокарциномы: муцинозная некистозная аденокарцинома, перстневидно-клеточная аденокарцинома, железисто-плоскоклеточный, недифференцированный (анапластический) рак, смешанный протоково-эндокринный рак
1.1.3.2. Гигантоклеточная опухоль
1.1.3.3. Серозная цистаденокарцинома
1.1.3.4. Муцинозная цистаденокарцинома (неинвазивная, инвазивная). Внутрипротоковая папиллярно-муцинозная карцинома (неинвазивная, инвазивная)
1.1.3.5. Ацинарно-клеточный рак; другие варианты ацинарно-клеточного рака: ацинарно-клеточная цистаденокарцинома, смешанный ацинарно-эндокринный рак
1.1.3.6. Панкреатобластома
1.1.3.7. Солидная псевдопапиллярная карцинома
1.1.3.8. Смешанные карциномы
1.2. Эндокринные опухоли поджелудочной железы
1.2.1. Доброкачественные эндокринные опухоли поджелудочной железы
1.2.1.1. Высокодифференцированная аденома (инсулинома, нефункционирующая аденома)
1.2.2. Пограничные (с неопределенным злокачественным потенциалом) эндокринные опухоли поджелудочной железы (высокодифференцированная опухоль без инвазии сосудов, инсулинома, гастринома, випома, глюкагонома, соматостатинома, другие опухоли, нефункционирующая опухоль)
1.2.3. Эндокринные опухоли поджелудочной железы с низкой степенью злокачественности
1.2.3.1. Высоко- и умеренно дифференцированные эндокринные карциномы (инсулинома, гастринома, випома, глюкагонома, соматостатинома, другие опухоли, нефункционирующие карциномы)
1.2.4. Эндокринные опухоли поджелудочной железы с высокой степенью злокачественности
1.2.4.1. Низкодифференцированный эндокринный рак поджелудочной железы (мелкоклеточный рак функционально-активный или нефункционирующий)
1.3. Неэпителиальные опухоли поджелудочной железы
1.3.1. Доброкачественные мягкотканные опухоли
1.3.2. Злокачественные мягкотканные опухоли
1.3.3. Лимфомы с поражением поджелудочной железы
Протоковая аденокарцинома — абсолютно преобладающая опухоль поджелудочной железы. Другие пять микроскопических вариантов протокового рака встречаются крайне редко. На экзокринный рак поджелудочной железы приходится 75% ее опухолей. В структуре экзокринного рака поджелудочной железы протоковая аденокарцинома составляет почти 97%, другие микроскопические формы — 3%. Наиболее часто экзокринный рак развивается в головке поджелудочной железы (59,1-87%), реже — и се теле и хвосте.
Раку поджелудочной железы нередко сопутствует хронический панкреатит, что делает точное определение границ опухоли практически невозможным без микроскопического исследования.
Опухоль распространяется на общий желчный проток, двенадцатиперстную кишку, паравазальные соединительнотканные структуры, нервные волокна, лимфатические сосуды и узлы вокруг общей печеночной артерии, верхних брыжеечных сосудов, чревного ствола, селезеночных сосудов. В большинстве случаев протоковый рак диагностируется на стадии внеорганного распространения опухоли и отдаленных метастазов. Локорегионарный рецидив у подавляющего большинства больных, перенесших хирургическое лечение, обусловлен ранним лимфогенным метастазированием, распространением опухоли по межтканевым, внутритканевым щелям, периневрально, инвазией крупных сосудов в области опухоли. Периневральная внеорганная инвазия обнаруживается у 81-100% больных протоковым раком поджелудочной железы.
Главный лимфогенный путь опухолевой диссеминации при раке головки поджелудочной железы — поражение лимфатических узлов вокруг головки поджелудочной железы (регионарные лимфатические узлы). Далее лимфогенное метастазирование может осуществляться прямо в парааортальные лимфатические узлы или в лимфоузлы вокруг верхних брыжеечных сосудов, а затем — в парааортальные лимфатические узлы. Это антеградный путь лимфогенного метастазирования. При локализации протокового рака в головке поджелудочной железы метастазы в регионарных лимфатических узлах в момент операции обнаруживаются у 41-86%, юкстарегионарные лимфатические узлы, по данным зарубежных авторов, поражаются метастазами у 18-57% оперированных больных.
Периневральный путь распространения рака поджелудочной железы рассматривается как важнейший наряду с лимфогенным и гематогенным.
Клинико-анатомическая классификация неэндокринного рака поджелудочной железы по TNM, предложенная Международным противораковым союзом (6-е издание, 2002)
Tis — преинвазивная карцинома (рак in situ)
T1 — опухоль ограничена поджелудочной железы и менее2 см в наибольшем измерении
Т2 — опухоль ограничена поджелудочной железы и более2 см в наибольшем измерении ТЗ — распространяется за пределы поджелудочной железы, но не вовлекает чревный ствол или верхнюю брыжеечную артерию
Т4 — распространяется на чревный ствол или верхнюю брыжеечную артерию
N1 — метастазы в регионарные лимфатические узлы
Ml — отдаленные метастазы
Группировка по стадиям
Стадия 0: TisNOMO Стадия IA: T1N0M0 Стадия IB: T2N0M0 Стадия ПА: T3N0M0 Стадия IIB: Т1-3N1M0 Стадия III: T4N0-1M0 Стадия IV: Т1-4N0-1М I
Клиническая картина и диагностика рака поджелудочной железы
Клиническая картина зависит от локализации опухоли. При локализации опухоли в головке поджелудочной железы у 47-90% пациентов диагноз установливается после появления механической желтухи. Наличие желтухи не является ранним симптомом заболевания, так как опухоль распространилась на внепеченочные желчные протоки. Для рака тела и хвоста поджелудочной железы характерно Iтигельное бессимптомное течение. Основные клинические симптомы при раке поджелудочной железы дистальных локализаций: постоянные боли в нигастральной области с иррадиацией в спину и потеря массы тела. Появление асцита или стеноза ДПК свидетельствует о распространении опухолевого процесса и делает маловероятной возможность хирургического лечения. Появление болевого синдрома с иррадиацией в спину коррелирует с местным распространением опухолевого процесса.
Диагностика основывается на комплексном обследовании с использованием УЗКТ, КТ, МРТ, ангиографии, РХПГ. Для диагностики рака поджелудочной железы применяются два иммунохимических теста — СА19-9 и РЭА. С целью дифференциальной диагностики используется чрескожная пункционная цитобиопсия объемных образований поджелудочной железы. В некоторых случаях дифференциальный диагноз рака головки поджелудочной железы и хронического индуративного панкреатита представляет значительную трудность.
Лечение рака поджелудочной железы
Основными видами хирургического пособия при раке поджелудочной железы являются стандартная и расширенная гастропанкреатодуоденальная резекция, дистальная резекция поджелудочной железы, панкреатэктомия. Применение комбинированных подходов при лечении протоковой аденокарциномы поджелудочной железы улучшает отдаленную выживаемость. Хирургическое лечение проводится в комбинации с дистанционной лучевой терапией (СОД 50-70 Гр) или химиотерапией с использованием препарата гемзар. Возможно применение интраоперационного облучения быстрыми электронами первичной опухоли (СОД до 30 Гр). Дистанционная лучевая терапия применяется при местно-распространенном раке поджелудочной железы. Лечение осуществляется мелким фракционированием до СОД 60-90 Гр. Лекарственное лечение применяется при диссеминированном раке поджелудочной железы, эффект отмечен у 7-24% больных.
Источник



