Механизм действия поджелудочной железы
Местоположение, размер и структура поджелудочной железы.
Поджелудочная железа является органом и внешней и внутренней секреции. Эндокринная часть железы представлена отдельными клеточными группами, образующими небольшие островки в массе всей остальной ее ткани.
Эти группы клеток называют островками Лангерганса. Число островков наибольшее в хвостовой части железы. Размер одного островка составляет 0,1-0,3 мм, число их от 200 тыс до 1,8 млн. Некоторые островки отделены от окружающих их тканей тонкой соединительнотканной оболочкой. В островках Лангерганса различают четыре группы клеток: альфа, бета, игрек и гамма. Они неодинаково окрашиваются и выполняют разные функции. Больше всего встречается бета-клеток (70%), примерно 20% от числа всех клеток приходится на альфа-клетки и примерно по 5% составляют игрек и гамма-клетки.
Гормоны поджелудочной железы.
В островках Лангерганса образуются три гормона: инсулин, глюкагон и липокаин.
Значение инсулина было выявлено еще в 1889 году, когда исследователи Меринг и Минковский, удалив у собаки поджелудочную железу, обнаружили в ее моче сахар. Отсюда ими был сделан вывод, что поджелудочная железа регулирует количество сахара в организме. Русский ученый Л.В.Соболев в 1902 году показал, что поджелудочная железа наряду с экзокринной выполняет и эндокринную функцию. Он перевязал выводной проток поджелудочной железы, после чего отмечал гибель клеток, в которых образуется секрет, выделяющийся в двенадцатиперстную кишку, в то время как островковая ткань не подвергалась изменению и нарушения обмена углеводов не отмечалось. В 1921 году ученые Бантиг и Бест выделили из островков гормон, названный ими инсулином (insula — островок).
В настоящее время полностью изучена структура инсулина и он искусственно синтезирован. Молекула инсулина состоит из двух цепей: А и В. Цепь А включает 21 аминокислотный остаток, а цепь В — 13-30. Установлено, что инсулин образуется в бета-клетках. Для его связывания с белком гранул и последующего освобождения необходим цинк. Инсулин стимулирует синтез гликогена в печени, мышцах, тормозит его превращение в сахар и способствует окислению сахара в мышцах. Поэтому после выключения функции островков Лангерганса (есть лекарственные препараты, которые избирательно их повреждают), в крови резко увеличивается содержание сахара, что называется гипергликемией, и он начинает появляться в моче. Наличие сахара в моче называют глюкозурией. При введении инсулина резко уменьшается количество сахара в крови с 80-120 до 30-45 мг%. Уменьшение количества сахара в крови называют гипогликемией.
Глюкагон образуется в альфа-клетках, состоит из 29 аминокислотных остатков и действует противоположно инсулину. Он вызывает гипергликемию и уменьшает содержание гликогена в печени.
Липокаин способствует выходу жиров из печени, окислению их в ней и тормозит превращение углеводов в жиры. Секреция гормонов островками Лангерганса регулируется содержанием сахара в крови. Альфа- и бета-клетки воспринимают изменения концентрации сахара в крови, и по принципу отрицательной обратной связи меняется активность этих клеток. Гипергликемия активирует бета-клетки и тормозит альфа-клетки, а гипогликемия активирует альфа-клетки и тормозит бета-клетки.
Механизм действия гормонов поджелудочной железы.
Считают, что имеется несколько путей воздействия гормонов поджелудочной железы на углеводный обмен. Инсулин способствует проникновению глюкозы через мембрану клетки и ее внутриклеточному накоплению. Кроме того, инсулин индуцирует синтез ферментов, способствующих синтезу гликогена и окислению глюкозы. Глюкагон увеличивает содержание фермента, вызывающего расщепление гликогена.
Гипер- и гипофункция поджелудочной железы.
Гиперфункция поджелудочной железы — очень редкое заболевание. Оно проявляется в гипогликемии и в связанном с этим нарушении деятельности центральной нервной системы, которая чрезвычайно чувствительна к недостатку глюкозы. Возникают слабость, судороги, потеря сознания. Введение глюкозы снимает все эти явления.
При гипофункции поджелудочной железы возникает сахарный диабет. Она характеризуется целым рядом симптомов, возникновение которых связано с увеличением содержания сахара в крови. Количество его может повышаться до 200-500 мг%. При этом в кровь переходит жидкость из тканей, что приводит к их обезвоживанию. Больной постоянно испытывает жажду. Он выпивает около 10 л воды, большая часть которой поступает в кровь и выделяется почками. За сутки у таких больных выделяется от 3 до 12, а в редких случаях до 25 л. Ослабление процессов окисления глюкозы приводит к нарушению обмена жиров. Образуются продукты неполного окисления жиров — кетоновые тела, что приводит к сдвигу реакции крови в кислую сторону — к ацидозу.
Инсулин — эффективное средство лечения диабет. Он дает возможность в течение десятилетий сохранять трудоспособность больных.
Источник
Гормонами поджелудочной железы являются инсулин и глюкагон.
Глюкагон
Строение
Представляет собой полипептид, включающий 29 аминокислот с молекулярной массой 3,5 кДа и периодом полураспада 3-6 мин.
Синтез
Осуществляется в клетках поджелудочной железы и в клетках тонкого кишечника.
Регуляция синтеза и секреции
Активируют: гипогликемия, адреналин.
Уменьшают: глюкоза, жирные кислоты.
Механизм действия
Аденилатциклазный активирующий.
Мишени и эффекты
Конечным эффектом является повышение концентрации глюкозы и жирных кислот в крови.
Жировая ткань
- повышает активность внутриклеточной гормон-чувствительной ТАГ-липазы и, соответственно, стимулирует липолиз.
Печень
- активация глюконеогенеза и гликогенолиза,
- за счет повышенного поступления жирных кислот из жировой ткани усиливает кетогенез.
Патология
Гиперфункция
Глюкагонома – редко встречающееся новообразование из группы нейроэндокринных опухолей. У больных отмечается гипергликемия и поражение кожи и слизистых оболочек.
Инсулин
Дополнительная, более подробная информация, об инсулине находится на следующей странице.
Строение
Представляет собой полипептид из 51 аминокислоты, массой 5,7 кД, состоящий из двух цепей А и В, связанных между собой дисульфидными мостиками.
Синтез
Синтезируется в клетках поджелудочной железы в виде проинсулина, в этом виде он упаковывается в секреторные гранулы и уже здесь образуется инсулин и С-пептид.
Регуляция синтеза и секреции
Активируют синтез и секрецию:
- глюкоза крови – главный регулятор, пороговая концентрация для секреции инсулина – 5,5 ммоль/л,
- жирные кислоты и аминокислоты,
- влияния n.vagus – находится под контролем гипоталамуса, активность которого определяется концентрацией глюкозы крови,
- гормоны ЖКТ: холецистокинин, секретин, гастрин, энтероглюкагон, желудочный ингибирующий полипептид,
- хроническое воздействие гормона роста, глюкокортикоидов, эстрогенов, прогестинов.
Уменьшают: влияние симпато-адреналовой системы.
Механизм действия
Осуществляется через рецепторы с тирозинкиназной активностью (подробно).
Мишени и эффекты
Основным эффектом является снижение концентрации глюкозы в крови благодаря усилению транспорта глюкозы внутрь миоцитов и адипоцитов и активации внутриклеточных реакций утилизации глюкозы:
- активируя фосфодиэстеразу, которая разрушает вторичный мессенджер цАМФ, инсулин прерывает эффекты адреналина и глюкагона на печень и жировую ткань.
- в мышцах и жировой ткани стимулирует транспорт глюкозы в клетки (активация Глют-4),
- в печени и мышцах ускоряет синтез гликогена (активация гликогенсинтазы).
- в печени, мышцах и адипоцитах инсулин стимулирует гликолиз, активируя фосфофруктокиназу и пируваткиназу.
- полученный в гликолизе пируват превращается в ацетил-SКоА под влиянием активированного инсулином пируватдегидрогеназного комплекса, и далее используется для синтеза жирных кислот. Превращение ацетил-SКоА в малонил-SКоА, первый субстрат синтеза жирных кислот, также стимулируется инсулином (ацетил-SКоА-карбоксилаза).
- в мышцах усиливает транспорт нейтральных аминокислот в миоциты и стимулирует трансляцию (рибосомальный синтез белков).
Ряд эффектов инсулина заключается в изменении транскрипции генов и скорости трансляции ферментов, отвечающих за обмен веществ, за рост и деление клеток.
Благодаря этому индуцируется синтез ферментов метаболизма
- углеводов в печени (глюкокиназа, пируваткиназа, глюкозо-6-фосфатдегидрогеназа),
- липидов в печени (АТФ-цитрат-лиаза, ацетил-SКоА-карбоксилаза, синтаза жирных кислот, цитозольная малатдегидрогеназа) и адипоцитах (ГАФ-дегидрогеназа, пальмитатсинтаза, липопротеинлипаза).
и происходит репрессия фосфоенолпируват-карбоксикиназы (подавление глюконеогенеза).
Инактивация инсулина
Инактивация инсулина начинается после интернализации инсулин-рецепторного комплекса и образования эндосомы, в которой и происходит деградация инсулина. Участвуют две ферментные системы:
- Глутатион-инсулин-трансгидрогеназа, которая восстанавливает дисульфидные связи между цепями А и В, в результате чего гормон распадается.
- Инсулиназа (инсулин-протеиназа), гидролизующая инсулин до аминокислот.
Период полужизни инсулина не превышает 5-6 минут. Происходит деградация в основном в печени и почках, но и другие ткани принимают в этом участие. Также в почках инсулин может фильтроваться, захватываться эпителиоцитами проксимальных канальцев и разрушаться до аминокислот.
Патология
Гипофункция
Инсулинзависимый и инсулиннезависимый сахарный диабет. Для диагностики этих патологий в клинике активно используют нагрузочные пробы и определение концентрации инсулина и С-пептида.
Источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Общие сведения
Одним из наиболее многофункциональных органов пищеварительной системы является поджелудочная железа. Можно сказать, что это ключевой орган пищеварения и обменных процессов организма. К сожалению, о ней мы вспоминаем, лишь когда слышим о таких диагнозах как «панкреатит» или «сахарный диабет», при которых этот орган перестает работать нормально. В этой статье мы уделим внимание анатомии и физиологии поджелудочной железы. Это поможет Вам лучше узнать собственный организм и быть ответственными по отношению к своему здоровью.
Анатомия поджелудочной железы
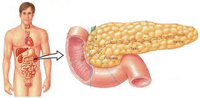 С точки зрения анатомии поджелудочная железа несложна. Условно ее можно разделить на железистую ткань и систему протоков, по которым синтезируемый поджелудочный сок продвигается по направлению к просвету двенадцатиперстной кишки.
С точки зрения анатомии поджелудочная железа несложна. Условно ее можно разделить на железистую ткань и систему протоков, по которым синтезируемый поджелудочный сок продвигается по направлению к просвету двенадцатиперстной кишки.
Железа расположена за брюшиной, на уровне поясничных и нижних грудных позвонков. При этом в поджелудочной железе различают несколько анатомических частей – головка, тело и хвост. Головка железы расположена в области двенадцатиперстной кишки, которая ее огибает. Именно на уровне этой части органа происходит слияние общего протока поджелудочной железы с желчным протоком. Объединившиеся желчевыводящий и проток поджелудочной железы открываются в просвет двенадцатиперстной кишки. В теле железы проходит общий проток, в который на всем протяжении впадают множество дополнительных протоков более мелкого калибра. В хвосте поджелудочной расположено наибольшее число железистых клеток, причем количество клеток, синтезирующих гормоны тут наибольшее.
Участие поджелудочной железы в пищеварении
 На самом деле анатомическая простота строения железы не соответствует сложной функции, которая на нее возложена. Ведь панкреатический сок – это концентрированный коктейль различных пищеварительных ферментов. Рассмотрим различные виды ферментов и их функцию по отдельности:
На самом деле анатомическая простота строения железы не соответствует сложной функции, которая на нее возложена. Ведь панкреатический сок – это концентрированный коктейль различных пищеварительных ферментов. Рассмотрим различные виды ферментов и их функцию по отдельности:
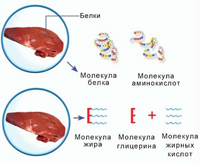
Амилаза — фермент, который участвует во фрагментации углеводных цепочек. Именно благодаря данному ферменту длинные цепочки углеводов укорачиваются и распадаются до уровня единичных молекул сахаров, которые могут быть усвоены слизистой кишечника. Этот фермент уже в просвете протоки поджелудочной железы находится в активном состоянии.
Липаза – этот фермент активно воздействует на жиры. Оказывает расщепляющее воздействие на сложную структуру простых жиров, расщепляя их на жирные кислоты и глицерин. В таком виде структурные единицы жиров усваиваются в пищеварительном тракте.
Нуклеаза – участвует во фрагментации цепочек ДНК, РНК поступившей пищи. Именно данный фермент разрывает связи между нуклеиновыми кислотами, высвобождая из цепи свободные нуклеиновые кислоты, которые могут быть усвоены организмом и в дальнейшем использоваться для построения информационных генетических структур самого организма.
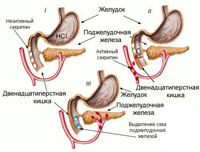
 Трипсиноген и химотрипсиноген – эти вещества синтезируются железами поджелудочной железы в неактивной форме. Лишь в просвете двенадцатиперстной кишки происходит их активация под воздействием активного трипсина, кишечного фермента энтерокиназы при кислотности равной pH 6 — 8. Активация данного фермента осуществляется лишь в просвете кишечника для того, чтобы предотвратить повреждение самой поджелудочной железы.
Трипсиноген и химотрипсиноген – эти вещества синтезируются железами поджелудочной железы в неактивной форме. Лишь в просвете двенадцатиперстной кишки происходит их активация под воздействием активного трипсина, кишечного фермента энтерокиназы при кислотности равной pH 6 — 8. Активация данного фермента осуществляется лишь в просвете кишечника для того, чтобы предотвратить повреждение самой поджелудочной железы.
В просвете кишечника под воздействием вспомогательных факторов приходит отщепление от белковой молекулы трипсиногена и химотрипсиногена концевого участка цепочки аминокислот. Благодаря этому происходит активация фермента, который приступает к процессу активного расщепления белковых молекул поступивших с пищей. Эти ферменты разрушают длинную аминокислотную цепочку белков. Благодаря этому процессу происходит развертывание белковых молекул, вытягивание цепочек, что делает возможным в дальнейшем отщепление концевых аминокислот, расположенных в начале и конце цепи.
Профосфолипазы – ферменты, которые активно воздействуют на сложные жиры – фосфолипиды. Так же как и трипсин, фосфолипаза в просвете кишечника должна быть активирована путем отщепления небольшой аминокислотной цепи. Благодаря этому механизму активации, фермент не воздействует на клеточные стенки тканей поджелудочной, которые в большом количестве содержат фосфолипиды.
В отношении расщепления жиров важно отметить важную роль, которую играет желчь. Дело в том, что жиры в просвет двенадцатиперстной кишки поступают в виде крупных жировых капель. Но для активного их расщепления необходимо формирование эмульсии состоящей из капель диаметром не более 5 мкм. Благодаря этому многократно увеличивается площадь контакта между жировыми капельками и ферментами, которые в состоянии их расщепить. Именно благодаря желчи удается достичь максимального измельчения жировых капель.
Как регулируется работа поджелудочной железы?
 Регуляция работы этой железы – это многоуровневый процесс. Большое влияние на активность работы секретирующих клеток оказывает центральная нервная система. Доказано, что вид пищи, упоминание о ней, обонятельные или вкусовые ощущения приводят к резкому повышению активности поджелудочной. Это воздействие производится посредством вегетативной нервной системы. Парасимпатическая часть нервной системы через блуждающий нерв повышает активность железы. В то же время, симпатическая система снижает ее активность.
Регуляция работы этой железы – это многоуровневый процесс. Большое влияние на активность работы секретирующих клеток оказывает центральная нервная система. Доказано, что вид пищи, упоминание о ней, обонятельные или вкусовые ощущения приводят к резкому повышению активности поджелудочной. Это воздействие производится посредством вегетативной нервной системы. Парасимпатическая часть нервной системы через блуждающий нерв повышает активность железы. В то же время, симпатическая система снижает ее активность.
Большое значение в регуляции активности поджелудочной железы имеют свойства желудочного сока. Повышение кислотности желудка, его механическое растяжение приводят к повышению секреции поджелудочной. Так же механическое растяжение двенадцатиперстной кишки, повышение кислотности в ее просвете приводят к секреции гормоноподобных веществ (секретин, холецистокинин), которые стимулируют работу поджелудочной.
Однако на поджелудочную железу оказывается не только стимулирующее влияние, но и тормозящее. Реализуется оно посредством работы симпатической нервной системы и благодаря таким гормонам как глюкагон, соматостатин.
Важным является так же способность поджелудочной железы подстраиваться под ежедневный рацион. В том случае, если в пище преобладает углеводный компонент, то вырабатываемый железой секрет будет содержать преимущественно амилазу, при преобладании белковой пищи – трипсин, жирная пища будет способствовать выработке липаз.
Эндокринная функция поджелудочной железы
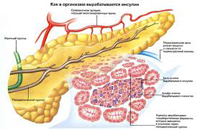 В отличие от клеток, которые секретируют в просвет канальцев, эндокринные клетки поджелудочной секретируют гормоны непосредственно в циркулирующую в тканях кровь. И, благодаря активному кровотоку в большом и малом кругу кровообращения, гормоны разносятся по всему организму в поисках специфических клеточных рецепторов.
В отличие от клеток, которые секретируют в просвет канальцев, эндокринные клетки поджелудочной секретируют гормоны непосредственно в циркулирующую в тканях кровь. И, благодаря активному кровотоку в большом и малом кругу кровообращения, гормоны разносятся по всему организму в поисках специфических клеточных рецепторов.
Основные участки, в которых сконцентрированы эндокринные клетки поджелудочной железы, называются островками Лангерганса. Причем разные клетки специализируется на синтезе различных гормонов. Бета клетки синтезируют и секретируют инсулин, за секрецию гормона глюкагон отвечают альфа клетки.
Функции гормонов поджелудочной железы
Инсулин – этот гормон активно участвует в обменных процессах, причем его функция не ограничивается лишь регуляцией метаболизма углеводов. Уровень инсулина влияет на обменные процессы аминокислот, углеводов, жиров. При этом инсулин способствует усваиванию расщепленных в процессе пищеварения веществ, их распределению в организме после попадания в кровь. Именно благодаря инсулину углеводы, аминокислоты и некоторые компоненты жиров могут проникать через клеточную стенку из крови внутрь каждой клетки организма. Без инсулина, при дефекте молекулы гормона или рецептора клетки, растворенные в крови питательные вещества остаются в ее составе и оказывают на организм токсическое действие. Наиболее распространенной патологией, связанной с нарушением работы инсулина является такое известное всем заболевание как сахарный диабет.
Глюкагон – во многом этот гормон оказывает противоположное инсулину действие. Основной функцией данного гормона является мобилизация внутриклеточных резервов углеводов и их использование в энергетических целях. Благодаря этому гормону поддерживается нормальный уровень глюкозы в крови даже в период строгих диет и голодовок.
Уровень гормонов поджелудочной железы регулируется по принципу обратной связи. При повышении уровня глюкозы в крови происходит высвобождение инсулина, при его снижении повышается уровень глюкагона.
 В заключение, хотелось бы обратить Ваше внимание, на тот факт, что поджелудочная железа, массой в 70 — 80 грамм в течение суток вырабатывает около 2 — 2,5 литров панкреатического сока. Вырабатываемый ею секрет нейтрализует кислотность желудочного сока, который, попадая в двенадцатиперстную кишку, может повредить слизистую кишечника.
В заключение, хотелось бы обратить Ваше внимание, на тот факт, что поджелудочная железа, массой в 70 — 80 грамм в течение суток вырабатывает около 2 — 2,5 литров панкреатического сока. Вырабатываемый ею секрет нейтрализует кислотность желудочного сока, который, попадая в двенадцатиперстную кишку, может повредить слизистую кишечника.
Несмотря на свои малые размеры, простоту анатомического устройства поджелудочная железа является ключевым органом пищеварения и обменных процессов в организме. Вырабатываемый ею секрет является концентрированной смесью пищеварительных ферментов. Важным является механизм активации вырабатываемых железой ферментов именно в просвете двенадцатиперстной кишки. Этот механизм позволяет предотвращать ферментные повреждения самой поджелудочной железы, при этом, не изменяя активности пищеварения в просвете тонкой кишки.
Перед применением необходимо проконсультироваться со специалистом.
Источник



