Нарушение внутренней секреции поджелудочной железы симптомы
Поджелудочная железа – многофункционный орган системы пищеварения. Можно сказать, что она предстает главным органом пищеварения, принимает участие в процессах обмена в организме человека.
Обладает диффузным функционалом – внешний и внутренний. Внешнесекреторная задача обусловлена выработкой панкреатического сока, который включает в себя ферменты пищеварения, нужные для нормального переваривания пищи.
Внутрисекреторный (эндокринный) функционал заключается в продуцировании определенных гормональных составляющих, обеспечивает регуляцию процессов обмена – жировой, углеводный и белковый обмен.
Расстройство функциональности поджелудочной железы провоцирует возникновение патологий – сахарный диабет, панкреатит и др. Рассмотрим анатомию и физиологию внутреннего органа, что позволит лучше узнать собственный организм.
Расположение и строение поджелудочной железы
ПЖ локализуется в брюшной области, находится сзади желудка, вплотную прилегает к 12-перстной кишке на уровне верхних позвонков поясницы. В проекции на брюшную стенку она располагается на 5-10 сантиметров выше пупка. Орган характеризуется трубчатым строением, состоит из трех сегментов – головка, тело и хвост.
Головка органа размещается в области изгиба 12-перстной кишки, последний орган охватывает головку в виде подковы. От тела она отделяется бороздой, по которой происходит воротная вена внутри организма.
Снабжение железы кровью происходит через артерии, отток биологической жидкости осуществляется посредством воротниковой вены.
Особенности строения тела ПЖ:
- Тело подразделяется на несколько частей – передняя, нижняя и задняя части, аналогично выделяют края.
- Передняя часть соприкасается со стенками желудка.
- Задняя часть примыкает к брюшной аорте и позвоночнику, по ней проходят кровеносные сосуды селезенки.
- Нижняя часть располагается пониже корня поперечной ободочной кишки.
Хвост ПЖ доходит до ворот селезенки, направлен и вверх и вниз. Структура внутреннего органа состоит из двух типов ткани, которые выполняют внешнюю и внутреннюю функцию. Основа ткани – мелкие дольки, которые разделяются между собой посредством прослоек соединительной ткани.
У каждой дольки имеются свои протоки на вывод. Они соединяются между собой, вследствие чего образуется общий выводной проток, который проходит по всему органу. У правого края головки он открывается в 12-перстную кишку, соединяется с желчными протоками. Вот так секрет поджелудочной железы проникает в кишку.
Между дольками локализуются группы клеток, называемые островками Лангерганса. Они не имеют выводных протоков, однако обладают сетью сосудов крови, что позволяет выделять инсулин и глюкагон сразу в кровь.
Как регулируется работа железы?
Уровень сахара
Мужчина
Женщина
Укажите Ваш сахар или выберите пол для получения рекомендаций
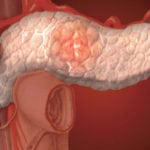 Регуляция панкреатической секреции предстает многоуровневым процессом. Большое влияние на активность функциональности клеток, которые способны секретировать нужные ферменты, оказывает состояние центральной нервной системы.
Регуляция панкреатической секреции предстает многоуровневым процессом. Большое влияние на активность функциональности клеток, которые способны секретировать нужные ферменты, оказывает состояние центральной нервной системы.
Исследования показывают, что вид пищи, запах еды или просто упоминание о ней приводят к резкому увеличению активности ПЖ. Это воздействие базируется на работе вегетативного отдела нервной системы.
Парасимпатический отдел нервной системы посредством блуждающего нерва способствует повышению активности внутреннего органа. При этом симпатическая система ориентирована на снижение.
В регуляции деятельности органа большое значение придается свойствам желудочного сока. Если увеличивается кислотность его в желудке, наблюдается его механическое растяжение, это приводит к тому, что возрастает секреция поджелудочной железы.
Одновременно с этим механическое растяжение 12-перстной кишки и увеличение кислотности в ее просвете приводит к выработке веществ, которые стимулируют работу ПЖ. К этим веществам относят:
- Секретин.
- Холецистокинин.
Железу системы в организме могут не только стимулировать, но и тормозить ее работу. Это влияние оказывается под воздействием симпатической нервной системы и гормонов – глюкагон, соматостатин.
Железа может подстраиваться под ежедневное меню. Если в еде превалируют углеводы, то синтезируемый секрет содержит преимущественно амилазу; если в пище больше белковых веществ, то вырабатывается трипсин; на фоне потребления только жирных продуктов питания продуцируется липаза.
Функции органа пищеварительной системы
Внешнесекреторная деятельность поджелудочной железы подразумевает выработку панкреатического сока. В сутки она синтезирует 500-1000 мл оного. Он состоит из ферментных соединений, соли и обычной воды.
Ферменты, которые синтезируются посредством железы, называют проферменты. Они продуцируются в неактивной форме. Когда попадает еда в 12-перстную кишку, начинают выделяться гормоны, посредством которых запускаются биохимические цепочки в организме, что приводит к активизации ферментов.
Мощным стимулятором выступает соляная кислота, которая при попадании в кишку способствует выведению секретина и панкреозимина – они оказывают воздействие на синтезирование ферментов:
- Амилаза обеспечивает расщепление углеводов.
- Трипсин принимает участие в процессе переваривания белковых веществ, который берет свое начало в желудке.
- Липаза помогает расщеплять жиры, которые уже подверглись влиянию желчи, поступившей из желчного пузыря.
Также панкреатический сок включает в свой состав минеральные вещества в виде кислой соли, которые способствуют щелочной реакции. Это нужно для того чтобы нивелировать кислые составляющие продуктов питания, которые поступили из желудка, и создать благоприятную среду для усвоения углеводов.
Внутрисекреторная функция органа обеспечивает выделение в организм таких гормонов как инсулин и глюкагон. Они продуцируются посредством группы клеток, которые вкраплены между дольками, не обладают протоками – островками Лангерганса. Функции гормонов:
- Выделение инсулина наблюдается из бета-клеток. Этот гормон отвечает за регулирование углеводных и жировых процессов в организме. Под воздействием компонента глюкоза проникает в ткань и клетки, вследствие чего концентрация сахара снижается.
- Глюкагон продуцируется посредством альфа-клеток. Если кратко, то гормон – это антагонист инсулина, то есть, ориентирован на повышение содержания сахара в организме человека. Также альфа-клетки участвуют в синтезировании липокаина, который предупреждает жировое перерождение печени.
Выделение адреналина из надпочечников также регулируется концентрацией сахара. На фоне гипогликемического состояния (низкая глюкоза) наблюдается рефлекторная выработка адреналина, что способствует повышению содержания сахара.
Поджелудочная железа находится в тесной связи с остальными органами пищеварительной системы. Любые ее нарушения или сбои в работе пагубным образом отражаются на всем процессе пищеварения.
Клинические проявления дефицита ферментов ПЖ
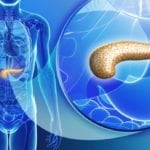
Расстройство выработки ферментов, снижение их функциональности и дефицит – это последствия хронической формы панкреатита. Заболевание сопровождается постепенными изменениями железистой ткани, вследствие чего она замещается соединительной тканью.
К панкреатиту приводит множество причин. Однако чаще всего патологический процесс в организме обусловлен чрезмерным потреблением алкогольных напитков. Среди другой этиологии выделяют нерациональное питание, сопутствующие недуги (холецистит), инфекционные заболевания, прием некоторых лекарственных средств.
Дефицит трипсина, амилазы и липазы приводит к серьезным сбоям в работе пищеварительного процесса.
Общие симптомы сбоя в работе ПЖ:
- Болевой синдром в левой области живота в подреберье, который часто развивается после приема пищи. Иногда боли не связаны с едой.
- Понижение или полная потеря аппетита.
- Пищеварительные расстройства в виде тошноты, поноса, многократной рвоты.
- Урчание в животе, метеоризм.
- Изменяется окраска и консистенция кала.
Выраженность и интенсивность клинических проявлений обусловлены степенью поражения. Из-за плохого переваривания наблюдается дефицит питательных компонентов, а в некоторых картинах расстройства метаболических процессов приводит к др. патологиям – остеохондроз, остеоартроз, атеросклероз кровеносных сосудов.
Если выявляется нехватка именно липазы, то признаки следующие:
- В каловых массах присутствует избыточное наличие жира.
- Жидкий кал оранжевого либо желтого цвета.
- Стул маслянистый.
В некоторых случаях происходит выделение только жидкого жира без наличия каловых масс. Если не хватает амилазы, то у больного обнаруживается непереносимость еды, обогащенной моносахаридами и дисахаридами. Также присутствует жидкий стол, недостаточность всасывания компонентов в тонком кишечнике, что сопровождается постоянным поносом, понижением массы тела.
При дефиците трипсина просматривается умеренная либо выраженная креаторея – в фекалиях выявляется большое содержание азота и мышечных волокон. Стул характеризуется зловонным запахом, не исключается возникновение малокровия.
Поскольку механизм расщепления продуктов нарушен, то даже при усиленном питании у пациентов понижается вес, диагностируется дефицит витаминов и минеральных компонентов, чрезмерная сухость кожного покрова, ломкость ногтевых пластин, волос.
При низкой выработке ферментов железой рекомендуется заместительное лечение. Но вещества растительной природы не могут полностью компенсировать внешнесекреторную недостаточность органа.
Как лечат железу?
 Лечение обусловлено конкретным заболеваниям. Острый приступ на фоне уточненных и неуточненных причин лечится посредством голодания. Поскольку это помогает снизить продуцирование сока, как результат, разгружается внутренний орган.
Лечение обусловлено конкретным заболеваниям. Острый приступ на фоне уточненных и неуточненных причин лечится посредством голодания. Поскольку это помогает снизить продуцирование сока, как результат, разгружается внутренний орган.
Обычно голодание при панкреатите пациенты легко переносят, так как значительно ухудшается общее самочувствие, присутствует постоянный болевой синдром. Разрешается пить минеральную воду без газа либо слабоконцентрированный отвар шиповника.
Основная цель терапии острого заболевания – предупредить осложнения и его перерождение в вялотекущий процесс. Рекомендуются таблетки для снятия болевого синдрома и ферментативные лекарства, которые способствуют снижению секреции ферментов.
Изначально они вводятся в организм человека через вену. Когда у пациента выявляется улучшение самочувствия, то он уже может принимать медикаменты в виде таблеток. Чтобы снизить болезненные ощущения в острой фазе можно к ПЖ прикладывать грелку со льдом.
Препараты для терапии поджелудочной железы:
- Спазмолитики для снятия болевого синдрома. Медицинские специалисты в большинстве назначают Папаверин, Но-шпу, Дротаверин. Если боль умеренная, то применяют Ибупрофен. Последнее лекарство одновременно обладает противовоспалительным и обезболивающим свойством.
- Антацидные медикаменты помогают унять боль, предупреждают раздражение и изъязвление слизистой оболочки. Используют в виде растворов и гелей, которые помогают нейтрализовать соляную кислоту. Представители группы – Зоран, Ранитидин.
Чтобы снизить выработку пищеварительных ферментов применяют Контрикал. Для терапии хронического панкреатита нужно ферментное лечение, чтобы поддерживать работу внутреннего органа, улучшить процесс переваривания пищи. Назначают Мезим, Панкреатин, Креон.
Поджелудочная железа является очень нежным и чувствительным органом, поэтому требует бережного отношения к себе. Злоупотребление алкоголем и вредные пищевые привычки могут привести к панкреатиту – острому и хроническому заболеванию, камням в выводных протоках, сахарному диабету, некрозу либо аденокарциноме ПЖ и др. заболеваниям.
Строение и функции поджелудочной железы рассмотрены в видео в этой статье.
Уровень сахара
Мужчина
Женщина
Укажите Ваш сахар или выберите пол для получения рекомендаций
Последние обсуждения:
Источник
Реферат
на тему
Нарушение внутренней секреции
и экспериментальная патология поджелудочной железы
Нарушение внутренней секреции
. Поджелудочная железа участвует в регуляции углеводного и липоидного обмена. Опытами Минковского и Меринга было доказано, что удаление поджелудочных желез у собак ведет к развитию гипергликемии и глюкозурии. Но особенно ценными были экспериментальные исследования А.В. Соболева, который на животных путем перевязки панкреатических протоков показал, что внутрисекреторная деятельность железы принадлежит островкам Лангерганса и что гибель их ведет к появлению сахарного диабета. Бантннгу и Бесту удалось получить из островков Лангерганса инсулин— гормон, участвующий в регуляции углеводного обмена. Исследованиями ряда авторов было установлено, что последний образуется в А-клетках островков Лангерганса и что разрушение их путем введения аллоксана, избирательно действующего на них, вызывает у животных картину сахарного диабета. Механизм действия инсулина сложен. Под влиянием его происходит фиксация гликогена в печени и поглощение сахара тканями организма. В островках Лангерганса образуется и другой гормон — глюкагон, который обладает противоположными инсулину свойствами и введение которого вызывает повышение сахара в крови.Оба эти гормона являются антагонистами и участвуют в регуляции углеводного обмена. Недостаточная выработкаинсулина островками Лангерганса и темсамым недостаточное поступление его в кровь ведет к появлению целого ряда симптомов, свойственных состоянию, носящему название гипоинсулинизма, которое илежит в основе клинической картины сахарного диабета. Это заболевание обычно проявляется следующими симптомами: обильной жаждой, повышенным аппетитом, полиурией, и их удалением, общей слабостью, пониженной трудоспособностью Возможно появление кожного зуда, фурункулеза, выпадение зубов и как осложнение развитие туберкулеза легких, атеросклероза, невритов, диабетической глаукомы и других осложнений. Все эти клинические проявления сопровождаются гипергликемией, гликозуриейи нередко появлением в моче ацетоновых тел.
В тяжелых случаях нарушения углеводного обмена течение сахарного диабета может осложниться развитием гипергликемической, диабетической комы.
В противоположность этому состоянию в клинике наблюдаются случаи повышенного содержания инсулина в крови (гиперинсулинизм), которыеведут к развитию своеобразной клинической картины. Явления гиперинсулинизма могут развиться у больных сахарным диабетом после передозировки инсулина, при аденомах островков Лангерганса (инсулинома), других эндокринных нарушениях (гипофункция гипофиза, коры надпочечников, Гипофункция щитовидной железы и др.) и функциональных нарушениях со стороны центральной нервной системы (так наз. функциональный гиперинсулинизм). Во всех этих случаях повышение содержания инсулина в крови ведет к резкому снижению сахара в крови, т. е. к гипогликемии. Гиперинсулинизм проявляется в клинике рядом симптомов: вначале общей слабостью, голодом, затем резким возбуждением, обильным потоотделением, головокружением, выраженной дрожью рук, иногда судорогами. К этим явлениям может присоединиться чувство страха, дезориентация в окружающем, спутанная речь, галлюцинации. В случаях продолжительного приступа гиперинсулинизма и резкого падения сахара в крови может наступить коматозное состояние — гипогликемическая кома. Следствием гиперинсулинизма является гипогликемия, при которой количество сахара в крови значительно снижается и падает до 40—50 мг%
, иногда даже до 15—20 мг%и ниже. Клинические проявления гиперинсулинизма стоят в зависимости не только от уровня содержания сахара в крови, но и от продолжительности гипогликемического состояния. Обычно приступы гиперинсулинизма быстро ликвидируются после дачи сахара внутрь или внутривенного введения его и проходят бесследно. В случаях же тяжелой и длительной гипогликемической комы может наступить смерть. Необходимо отметить, что при частых повторениях и продолжительных приступах гиперинсулинизма наступают стойкие и необратимые изменения со стороны центральной нервной системы, проявляющиеся в различной степени разрушения коры, базальных ганглиев, образовании петехиалъных кровоизлияний в различных участках мозга, вследствие чего могут возникнуть явления гемипареза, атаксии, недержания мочи, паркинсонизм, психические расстройства. В литературе описаны случаи атрофии коры и базальных ганглиев, сопровождавшихся кровоизлияниями и другими изменениями в мозге, развившихся во время приступов гиперинсулинизма на почве аденомы островков Лангерганса. Установлено, что обмен в мозге в основном зависит от содержания глюкозы в крови и что поэтому мозг очень чувствителен к явлениям гипогликемии. Некоторые исследователи высказывают предположение, что при наступлении гипогликемии собственных запасов гликогена в мозге хватает только на один час и что, если гипогликемия затягивается на более длительный срок, то в мозге могут развиться значительные и необратимые изменения. Магнус и др. полагают, что во время гипогликемии в центральной нервной системе создаются условия, которые аналогичны анаксии и асфиксии. Иногда приступы гиперинсулинизма могут сопровождаться диспептическими расстройствами и сильными болями в животе, напоминая клиническую картину язвенной болезни. В некоторых случаях гиперинсулинизма, часто повторяющихся и продолжающихся длительно, у больных могут появиться боли в конечностях и развиться атрофии мышц, видимо, из-за потери ими гликогена. При наличии симптомов гиперинсулинизма важно выявить его этиологию, т. к. это имеет большое практическое значение для клиники и главным образом для лечения его. Причины гиперинсулинизма (соответственно — гипогликемии) различны. Гипогликемии подразделяются на органические и функциональные. В тех случаях гиперинсулинизма, когда он обусловлен аденомой островков Лангерганса,больной должен быть оперирован; функциональный же гиперинсулинизм подлежит терапевтическому лечению. Для выяснения причины различных гипогликемии большое значение имеет клиническая картина, свойственная тому или иному заболеванию, вызвавшему резкое снижение сахара в крови, а также рентгенологический и лабораторный методы исследования. Так, например, для решения вопроса, не вызваны ли явления гипогликемии гипофункцией передней доли гипофиза, необходимо учитывать клиническую картину заболевания, данные рентгенографии турецкого седла, исследования глазного дна и полей зрения. Гипогликемия, обусловленная гипофункцией коры надпочечников, выявляется на основании клиники этого заболевания (адинамия, темная окраска кожи и слизистых оболочек, низкое артериальное давление) и лабораторных данных (низкий уровень сахара, хлоридов в крови и 17-кетостероидов в моче) и т. д. При органическом гиперинсулинизме количество сахара в крови натощак бывает весьма низким — до 50 мг%и ниже. При функциональном гиперинсулинизме количество сахара в крови натощак бывает обычно нормальным, а после нагрузки глюкозой наблюдается значительный подъем кривой в первые часы и резкое падение ее через 2—4 часа после нагрузки.
Предложено для распознавания различных видов гипогликемии проводить исследование сахара в крови при голодании больного. В этих случаях при органическом гиперинсулинизме наблюдается резкое снижение сахара в крови и появление приступов гипогликемии. Для органического гиперинсулпнизма, возникающего на почве аденомы островков Лангерганса, принято считать классическим триаду симптомов, описанную Уиллом:
1. Возникновение приступов гиперинсулинизма натощак или после длительного голодания.
2. Содержание сахара в крови натощак ниже 50 мг%.
3. Быстрое купирование приступа введением глюкозы внутрь или внутривенно. За последнее время некоторые авторы в диагностике этого заболевания придают большое значение энцефалографическому исследованию, которое, по их заключению, показывает в этих случаях снижение нормального альфаритма.
Недостаточно глубокий анализ клинической картины, неясного пароксизмального состояния может повести к ошибке в диагностике. Нередко в случаях гиперинсулинизма ставится диагноз: эпилепсия, психотические состояния, опухоль головного мозга, алкоголизм, язвенная болезнь и другие заболевания.
Как было установлено экспериментально, экстирпация поджелудочной железы вызывает у животного не только гипергликемию, глюкозурию, но и гиперлипемию с последующим жировым перерождением печени. Кормление же подопытных животных сырой поджелудочной железой предупреждает развитие этого процесса. На основании экспериментальных наблюдений Дрегстедт пришел к заключению, что в поджелудочной железе, помимо инсулина и глюкагона, вырабатывается третий гормон, которому он дал название «липокаин». Обладая липотропными свойствами, липокаин предупреждает развитие жировой дистрофии печени.
В клинике отмечена также связь, существующая между печенью и поджелудочной железой, и частота одновременного вовлечения их в патологический процесс (гепатопанкреатический синдром). Так, при целом ряде заболеваний печени и желчных путей (болезнь Боткина, цирроз печени, желчнокаменная болезнь, холециститы и другие заболевания) нередко могут быть наблюдаемы функциональные и морфологические изменения со стороны поджелудочной железы и, наоборот, при заболеваниях поджелудочной железы имеет место вторичное развитие патологического процесса в печени. Отмечено также, что поджелудочная железа участвует в процессах кроветворения и регуляции артериального давления.
Экспериментальная патология
В экспериментах на животных воспроизведены многие существенные стороны клинической патологии поджелудочной железы, в частности различные формы острых и хронических панкреатитов, панкреонекрозы, нарушения внутрисекреторной и внешнесекреторной функций поджелудочной железы. Существенный интерес представляет возможность изолированного повреждения различных функциональных элементов поджелудочной железы посредством специальных химических веществ, обладающих избирательной токсичностью. Деструкция (Б-клеток, продуцирующих инсулин, может быть вызвана аллоксаном,повреждение А-клеток, продуцирующих глюкагон, — введением солей кобальта. Нарушение экзокринного аппарата может быть достигнуто введением ряда веществ, из которых наиболее широко применяется этионин. Такой же результат дает перевязка протоков поджелудочной железы, вызывающая полную атрофию экзокринного аппарата и не влияющая на внутрисекреторную функцию поджелудочной железы. Ниже приведены наиболее употребительные приемы воспроизведения заболеваний поджелудочной железы в эксперименте.
Источник



