Патогенез опухолей поджелудочной железы
Фторурацил
.
Фторурацил (FU) — синтетический аналог естественно встречающегося пиримидина — урацила. Основной мишенью является фермент тимидилат синтетаза, контролирующий синтез нормальных тимидиновых нуклеотидов. При инфузиях раствор Фторурацила должен быть защищен от света. Больным рекомендуется не применять вместе с Фторурацилом аспирин и другие нестероидные противовоспалительные средства.
Препарат применяется в разных режимах:
- 500 мг/м
2
в/в струйно 5 дней подряд, каждые 4 недели или
- 500-600 мг/м
2
в/в, струйно 1 раз в неделю, 6 недель или
- 1000 мг/м
2
в/в, инфузионно 5 дней (120 часов) каждые 4 недели или
- 200-300 мг/м
2
в/в, инфузионно в течение месяца или
- 2,6 г/м
2
в/в, инфузионно в течение 24 часов, 1 раз в неделю, 4-5 недель.
Митомицин С
(ММС).
ММС является антибиотиком по происхождению, по механизму действия относится к алкилирующим агентам, требующим активации in vivo. Среди побочных эффектов ММС — лейкопении и особенно тромбоцитопении. Редко препарат вызывает развитие интерстициальной пневмонии, при применении вместе с антрациклинами усиливает кардиотоксичность последних.
Препарат вводится в/в. Назначается по 10-20 мг/м
2
каждые 6-8 недель, или по 5-6 мг/м
2
каждые 4 недели.
Стрептозоцин
(Szt).
По химическому строению препарат относится к нитрозомочевинам с D-глюкопиранозной связью. По механизму действия Szt — типичный алкилатор ДНК. Он попадает в клетки островкового аппарата и этим объясняется его противоопухолевая активность при новообразованиях эндокринной части поджелудочной железы.
Препарат вводится строго в/в по 500 мг/м
2
в течение 5 дней каждые 6 недель.
Из осложнений наблюдаются почечная токсичность, рвота, умеренная миелосупрессия, гипогликемия, лихорадка, депрессия, летаргия.
Относится к классу нитрозомочевин. Является алкилирующим агентом. При раке поджелудочной железы препарат эффективен в 13% случаев.
Доксорубицин
(ADM).
Антибиотик из группы антрациклинов, состоящий из многокольцевого хромофора и аминосахара. Главным в механизме действия ADM является интеркаляция хромофора между спиралями ДНК. Кроме того, подавляется фермент топоизомераза II, ответственный за топологию ДНК, и генерируются свободные радикалы, которые цитотоксичны для опухолевых и нормальных тканей.
ADM вводится в/в или внутриартериально. Назначается в дозах по 25-30 мг/м
2
2 дня каждые 3-4 недели, или 20 мг/м
2
еженедельно, или 60-75 мг/м
2
1 раз в 3 недели.
Наиболее серьезным осложнением считается кардиотоксичность.
Эпирубицин
(EPI).
Является стереоизомером доксорубицина, отличается от него ориентацией гидроксильной группы в 4 положении в аминосахаре. Противоопухолевый эффект регистрируется в диапазоне 13-37%. Годичная выживаемость составляет 12%.
Применяется в дозах 75-90 мг/м
2
каждые 21 день. Препарат вводится строго в/в. Суммарная доза не должна превышать 700 мг/м
2
.
Среди частых осложнений миелосупрессия, мукозиты, тошнота и рвота. Среди редких побочных эффектов повышение мочевой кислоты, тромбоцитопении, флебосклероз, диарея, темные пятна на коже, изменения ногтей, аллергические реакции.
Относится к хлорэтиламинам, является синтетическим аналогом циклофосфана. Активируется в печени микросомальными ферментами. Его активный метаболит — 4-гидроксиифосфамид алкилирует ДНК вызывая ее разрывы, а также РНК и тормозит синтез белков.
Из осложнений наблюдаются: миелосупрессии, тошнота, рвота, диарея и иногда запоры, алопеция, гепатотоксичность, редко летаргия, галлюцинации; могут возникнуть симптомы цистита — дизурия, частое мочеиспускание.
Наиболее распространенные режимы (в/в):
- 1000 мг/м
2
5 дней подряд каждые 3 недели или
- 1,2-2,4 г/м
2
3 дня подряд каждые 3 недели или
- 5000 мг/м
2
1 раз в 3 недели.
Хиназолиновый антифолат, является прямым и специфическим ингибитором тимидилат синтетазы. После попадания в опухолевую клетку препарат подвергается полиглутаминированию под действием фолиполиглутамат синтетазы. Томудекс проявляет активность в режиме монотерапии в 12-14% случаев. У 29% пациентов отмечается стабилизация роста опухоли.
Вводится по 3 мг/м
2
в/в 1 раз в 3 недели.
Среди осложнений: лейкопения (18%), диарея (10%), мукозиты (3%), астения (18%), рвота (13%), повышение трансаминаз (7%).
UFT — препарат, состоящий из фторафура и урацила. Молярное соотношение этих компонентов 1:4. Эффективность препарата регистрируется в 22,7% случаев.
Это синтетический аналог дезоксиуридина, является метаболитом фторурацила.
Препарат вводится в/в или внутриартериально. При в/в введении доза FUDR составляет 0,1-0,15 мг/кг в день — 14 дней; циклы повторяют каждые 4 недели. При введении внутриартериально доза FUDR составляет 0,2-0,3 мг/кг в день, 14 дней; циклы повторяют каждые 4 недели.
Из осложнений FUDR отмечаются: тошнота, рвота, мукозиты, диарея (29%), гастриты, головная боль, зуд, дерматиты, повышение трансаминаз.
Относится к ингибиторам топоизомеразы I. Является аналогом камптотецина.
Вводится в/в, в дозе 350 мг/м
2
1 раз в 3 недели (5-6 доз).
Среди осложнений — диарея, нейтропения, иногда с лихорадкой, рвота, аллергические реакции, стоматиты.
При раке поджелудочной железы эффективен у 12% больных.
Это сложный дитерпен с таксановым кольцом и углеводной цепочкой (необходимой для противоопухолевой активности). Паклитаксел имеет растительное происхождение, выделен из коры калифорнийского тиса. Тах — (первый активный препарат из группы таксанов) стимулирует хаотичное и неправильное образование из тубулина микротрубочек и затем мешает их распаду. Эти нарушения скелета опухолевых клеток ведут их к гибели. В 20% от Тах отмечена стабилизация опухолевого процесса.
Тах вводится в дозах 175-200 мг/м
2
в/в, инфузионно, в течение 3 часов (иногда 24) 1 раз в 3 недели с предварительной премедикацией.
Из побочных эффектов наблюдаются миелосупрессия, анемия и тромбоцитопения, падение давления (12%), нейротоксичность (60%), анорексия, алопеция, рвота и мукозиты не часты.
Механизм действия препарата заключается в разрушении клеточного скелета из-за стимуляции образования микротрубочек и подавления их деполимеризации.
Применяется Txt в/в в дозах 100 мг/м
2
1 раз в 3 недели (5-6 циклов). Для снижения гиперчувствительности также требуется премедикация дифенгидрамином и стероидами.
Из побочных эффектов наблюдаются: нейтропения (70%), дерматологическая токсичность (60%), задержка жидкости (30-68%), диарея (31%), стоматиты (20%), нейротоксичность (12%), прочие осложнения редки.
Gem является фторзамещенным аналогом дезоксицитидина, по структуре близок к цитозару. Однако, в отличие от последнего, он более липофильный и вследствие этого быстрее проходит через мембраны опухолевых клеток. У него больший аффинитет к мишени — дезоксицидинкиназе, его активный метаболит гемцитабин трифосфат дольше, чем цитозар находится в опухолевой клетке.
Гемзар применяется в/в по 1000 мг/м
2
в 1,8,15 дни, каждые 4 недели. Среди осложнений от применения Gem: лейкопения (19%), тромбоцитопения (22%), астения (12%), периферические отеки (10%).
Эрлотиниб (Тарцева) является обратимым и высокоспецифичным ингибитором тирозинкиназы рецептора эпидермального фактора роста (EGFR). Тирозинкиназа отвечает за процесс внутриклеточного фосфорилирования HER1/EGFR. Экспрессия HER1/EGFR наблюдается на поверхности как нормальных, так и опухолевых клеток. Ингибирование фосфотирозина EGFR тормозит рост линий опухолевых клеток и/или приводит к их гибели.
При раке поджелудочной железы применяется по 100 мг ежедневно, длительно, в комбинации с гемцитабином.
Источник
Инфильтрирующая протоковая аденокарцинома, более известная как рак поджелудочной железы, занимает 4-е место среди причин смерти от злокачественных новообразований в США, уступая лишь раку легкого, толстой кишки и молочной железы. Для рака поджелудочной железы характерен один из самых высоких показателей смертности.
В 2008 г. в США было выявлено 37 тыс. новых случаев рака поджелудочной железы. Уровень 5-летней выживаемости при раке поджелудочной железы крайне низок и составляет менее 5%.
а) Предраковые поражения поджелудочной железы. В толстой кишке существует механизм трансформации обычного эпителия в аденому, а затем в инвазивную карциному. В поджелудочной железе также происходит трансформация протокового эпителия в неинвазивные внутриэпителиальные поражения мелких протоков и проточков, а затем в инвазивную карциному. Неинвазивные внутриэпителиальные поражения обозначают термином «панкреатическая интраэпителиальная неоплазия» (PanIN). Факт трансформации PanIN в инвазивную карциному подтверждают следующие данные:
— распределение в поджелудочной железе участков PanIN аналогично распределению инвазивного рака;
— PanIN часто обнаруживают вблизи участков инфильтрирующей карциномы;
— развитие инвазивного рака поджелудочной железы у пациентов с ранее диагностированной PanIN.
Генетические и эпигенетические нарушения, выявляемые при PanIN, аналогичны тем, которые наблюдают при инвазивном раке. Эпителиальные клетки PanIN характеризуются значительным укорочением теломер, что способствует накоплению хромосомных нарушений и развитию инвазивной карциномы. На основании описанных нарушений была предложена модель опухолевого развития PanIN.
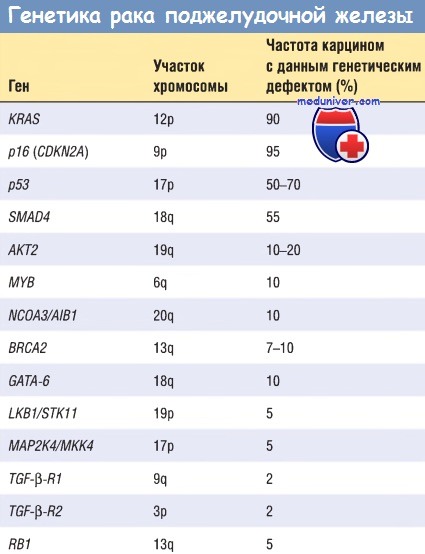
б) Молекулярные основы канцерогенеза. Рак поджелудочной железы характеризуется наличием многочисленных генных дефектов, не присущих другим злокачественным опухолям этого органа. Молекулярные дефекты, характерные для канцерогенеза поджелудочной железы, перечислены в таблице ниже.
— Ген KRAS. При раке поджелудочной железы этот онкоген мутирует чаще остальных. Активирующие точечные мутации KRAS отмечают в 80-90% наблюдений. Такие мутации нарушают внутреннюю гуанозин-трифосфатазную активность белка Kras, и он становится постоянно активным. В свою очередь, Ras активирует несколько внутриклеточных сигнальных путей, что способствует активации факторов транскрипции Fos и Jun.
— Ген р16 (CDKN2A). При раке поджелудочной железы этот ген-супрессор опухолей инактивируется наиболее часто (в 95% наблюдений). Белок р16 играет критическую роль: его инактивация приводит к утрате контроля над клеточным циклом.
— Ген SMAD4. При раке поджелудочной железы этот ген-супрессор опухолей был инактивирован в 55% наблюдений. SMAD4 кодирует синтез белка, играющего важную роль в передаче сигнала от лигандов семейства TGF-b к рецепторам на клеточной мембране. При других злокачественных опухолях инактивация этого гена происходит очень редко.
— Ген р53. При раке поджелудочной железы инактивация этого гена-супрессора опухолей определяется в 50-70% наблюдений. Как указывалось ранее, белок р53 — это ядерный ДНК-связывающий белок, который влияет на старение клетки и контролирует клеточный цикл, запускающий процесс клеточной гибели (апоптоз).
— Другие гены. В последнее время накапливается все больше данных о других, но не менее важных генах, повреждение которых возможно при раке поджелудочной железы. Например, амплификация гена АКТ2 определяется в 10-20% наблюдений рака поджелудочной железы, а амплификация генов MYB, GАТА-6 и NCOA3/AIB1 — в 10% наблюдений. Инактивация таких генов-супрессоров опухолей, как BRCA2, LKB1/STK11, МАР2К4/МКК4, TGF-b-R1, TGF-b-R2 и RB1, отмечается менее чем в 10% наблюдений рака поджелудочной железы.
Нарушение метилирования. При раке поджелудочной железы также нарушается процесс метилирования. Гиперметилирование промоторных участков некоторых генов-супрессоров опухолей приводит к сайленсингу этих генов.
Экспрессия генов. При расширенном анализе экспрессии генов были выявлены гены, гиперэкспрессия которых характерна для злокачественных опухолей поджелудочной железы. Данные гены являются потенциальными мишенями для новой таргетной терапии, а также могут стать основой для создания скрининговых тест-систем. Например, при злокачественных опухолях поджелудочной железы гиперактивирован сигнальный путь Hedgehog, ингибирование этого пути препаратом циклопамином останавливает рост опухоли в эксперименте.
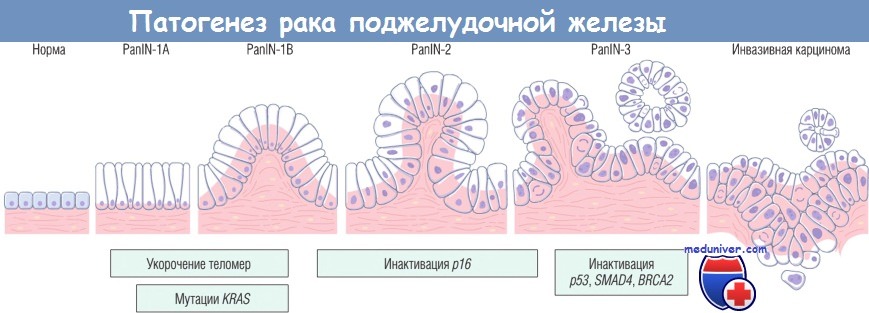
Модель развития рака поджелудочной железы.
Предполагается, что на ранней стадии панкреатической интраэпителиальной неоплазии (PanIN) происходит укорочение теломер и мутации онкогена KRAS,
на промежуточной стадии инактивируется ген-супрессор опухолей р16,
а на поздней стадии происходит инактивация генов-супрессоров опухолей р53, SMAD4 (DPC4) и BRCA2.
Важно отметить, что наиболее значимо накопление множественных мутаций, а не появление их в определенном порядке.
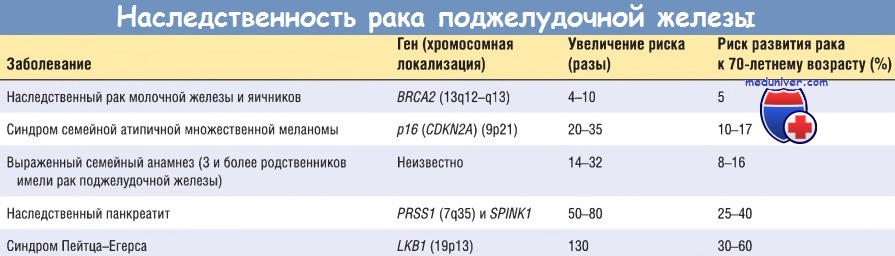
в) Эпидемиология, этиология и патогенез. Рак поджелудочной железы встречается преимущественно у пожилых людей: 80% наблюдений приходятся на возрастную группу 60-80 лет. Это заболевание распространено в США среди лиц с темным цветом кожи, евреи ашкенази также заболевают чаще по сравнению с общей популяцией.
Основным внешним фактором, повышающим риск развития рака поджелудочной железы в 2 раза, является курение. Хотя для отдельного индивида такое повышение риска невелико, роль курения в общей заболеваемости раком поджелудочной железы значительна в связи с широким распространением этой вредной привычки.
Еще один, не менее значимый фактор риска — употребление богатой жирами пищи. Риск развития рака поджелудочной железы также повышают хронический панкреатит и сахарный диабет, но конкретные причины этого (за исключением случаев наследственного панкреатита) неизвестны.
Отягощающими факторами могут быть курение и употребление алкоголя пациентами с хроническим панкреатитом. Однако в конкретном случае трудно установить, является ли хронический панкреатит причиной рака поджелудочной железы или лишь клиническим проявлением новообразования, поскольку опухоли маленьких размеров могут вызвать обструкцию протоков железы с последующим развитием хронического панкреатита.
Также неясна взаимосвязь сахарного диабета и рака поджелудочной железы, т.к. сахарный диабет может быть осложнением злокачественной опухоли, т.е. впервые выявленный сахарный диабет у пожилых пациентов может стать первым симптомом рака поджелудочной железы.
Есть данные о семейных случаях рака поджелудочной железы. Кроме того, выявляют все большее количество наследственных генетических дефектов, повышающих риск развития рака поджелудочной железы. Почти у 10% евреев ашкенази, страдающих раком поджелудочной железы, выявлены мутации гена BRCA2, хотя могут отсутствовать семейные случаи рака молочной железы и яичников. Мутации гена р16 (CDKN2A) при раке поджелудочной железы почти всегда наблюдают у лиц с семейной предрасположенностью к меланоме.
В одной семье с высокой заболеваемостью раком поджелудочной железы была выявлена мутация гена PALLD, кодирующего синтез белка внеклеточного матрикса палладина. В других семьях мутации этого гена не были обнаружены, однако гиперэкспрессия палладина определялась в строме, окружающей опухолевую ткань.
г) Морфология. Около 60% злокачественных опухолей локализуются в области головки, 15% — в области тела и 5% — в области хвоста поджелудочной железы. В 20% наблюдений отмечают диффузное поражение всей железы. Макроскопически опухолевая ткань плотная на ощупь, звездообразной формы и серовато-белого цвета на разрезе.
В большинстве случаев рак поджелудочной железы представляет собой протоковую аденокарциному, которая построена из эпителиальных клеток с формированием железистых структур и секрецией муцина. Протоковая аденокарцинома характеризуется двумя типичными признаками: высокой инвазивностью (даже на ранней стадии аденокарцинома широко прорастает в околопанкреатические ткани) и выраженной десмопластической реакцией (скоплением фибробластов, лимфоцитов и внеклеточного вещества на границе опухоли и здоровой ткани).
В большинстве наблюдений карциномы головки поджелудочной железы отмечается обструкция дистальной части общего желчного протока. Вследствие этого у 50% пациентов выявляют выраженное расширение желчных протоков, а практически у всех возникает желтуха. Напротив, при карциноме тела и хвоста поджелудочной железы отсутствует поражение желчных протоков, поэтому заболевание до определенного момента бессимптомно.
Такие опухоли могут достигать достаточно больших размеров, и к моменту обнаружения большинство из них широко диссеминированы. Рак поджелудочной железы часто распространяется по ходу нервов и прорастает в забрюшинное пространство. Опухоль также может инвазировать селезенку, надпочечники, позвоночник, поперечную ободочную кишку и желудок. Часто отмечаются метастазы в околопанкреатические лимфатические узлы, а также в лимфатические узлы желудка, ворот печени, брыжейки кишки, сальника. Отдаленные метастазы выявляют преимущественно в печени, легких и костях.
Микроскопически карцинома головки, тела и хвоста поджелудочной железы имеет одинаковое строение. Опухоль представляет собой умеренно дифференцированную или низкодифференцированную аденокарциному, формирующую атипическую железистую структуру или представленную группами клеток с агрессивным инфильтрирующим типом роста. Вокруг структур инвазивного рака определяются выраженный фиброз стромы и признаки периневральной инвазии как в ткани железы, так и за ее пределами.
Часто отмечается инвазия в лимфатические или большие кровеносные сосуды. Опухолевые железистые структуры плохо сформированы и обычно выстланы полиморфными кубическими или цилиндрическими эпителиоцитами. Высокодифференцированные карциномы встречаются очень редко.
Относительно редкие типы рака поджелудочной железы — железисто-плоскоклеточная карцинома, коллоидная карцинома, гепатоидная карцинома, медуллярная карцинома, перстневидноклеточная карцинома, недифференцированная карцинома и недифференцированная карцинома с остеокластоподобными гигантскими клетками. При железисто-плоскоклеточной карциноме наряду с участками железистой дифферен-цировки есть очаги плоскоклеточной дифференциров-ки, а недифференцированная карцинома может содержать остеокластоподобные многоядерные гигантские клетки.
Рак поджелудочной железы:
(А) На разрезе в области хвоста поджелудочной железы видны нормальная ткань железы и нормальный панкреатический проток (слева),
а также новообразование без четких границ (в центре), сдавливающее панкреатический проток и приводящее к его расширению дистальнее образования (справа).
(Б) Атипические железы, окруженные плотной фиброзной стромой, и немногочисленные клетки воспаления.
д) Клинические признаки. Карцинома поджелудочной железы протекает бессимптомно до тех пор, пока не прорастет в соседние органы и ткани. Первым симптомом обычно является боль, при этом опухоль часто оказывается уже неоперабельной. Механическая желтуха развивается при локализации карциномы в головке поджелудочной железы, однако этот симптом редко помогает своевременной диагностике злокачественной опухоли.
Снижение массы тела, потеря аппетита, общее недомогание и слабость свидетельствуют, как правило, о запущенном заболевании. У 10% пациентов отмечается мигрирующий тромбофлебит (синдром Труссо). Развитие тромбофлебита связано с высвобождением факторов агрегации тромбоцитов и прокоагулянтов из опухолевой ткани и продуктов ее распада. Арманд Труссо (1801-1867), французский врач, страдавший то появляющимся, то исчезающим тромбозом, считал, что это связано с развитием у него рака (во время аутопсии действительно был обнаружен рак поджелудочной железы).
Для рака поджелудочной железы характерно быстрое и агрессивное течение. На момент постановки диагноза менее 20% злокачественных опухолей поджелудочной железы являются операбельными. В течение длительного времени идет поиск маркеров для раннего выявления рака поджелудочной железы. У пациентов достаточно часто отмечают повышение уровня многих ферментов и антигенов в сыворотке крови (в частности, карциноэмбрионального антигена и СА19.9). Эти маркеры можно применять для оценки эффективности лечения, но они неспецифичны и малочувствительны, что не позволяет использовать их для скрининга. Некоторые методы лучевой диагностики, например эндоскопическое УЗИ и компьютерная томография, доказали свою ценность в подтверждении диагноза, но они также не подходят для скрининга.
е) Ацинарно-клеточная карцинома поджелудочной железы. Ацинарно-клеточная карцинома характеризуется наличием опухолевых клеток с ацинарной дифференцировкой, включая формирование зимогенных гранул и продукцию экзокринных ферментов, в частности трипсина и липазы. У 15% пациентов с ацинарноклеточной карциномой развивается синдром метастатического жирового некроза, обусловленный попаданием липазы в системный кровоток.
ж) Панкреатобластома. Панкреатобластома — редкая опухоль, обычно развивающаяся у детей в возрасте от 1 до 15 лет. Опухоль имеет характерное микроскопическое строение и представлена участками плоскоклеточной дифференцировки, расположенными среди ацинарных клеток. Панкреатобластома — это злокачественная опухоль, однако прогноз при ней значительно лучше, чем при протоковой аденокарциноме.
а — Кахексия и желтуха у пациента с раком поджелудочной железы.
б,в — Рак поджелудочной железы с билиарной обструкцией б). Более каудальный срез (компьютерная томография) позволяет увидеть увеличенную головку поджелудочной железы с неровной зоной опухоли низкого усиления.
Главный панкреатический проток расширен. Опухоль распространяется в жировую клетчатку кпереди от головки поджелудочной железы.
Инвазии в верхнюю брыжеечную артерию или вену не видно (в). Срез краниальный (б) демонстрирует расширение панкреатического протока и атрофию паренхимы тела и хвоста поджелудочной железы.
Общий желчный проток слегка расширен.
— Вернуться в оглавление раздела «Патофизиология»
Оглавление темы «Патогенез болезней ЖКТ»:
- Механизм развития (патогенез) атрезии желчных протоков
- Механизм развития (патогенез) кисты холедоха
- Механизм развития (патогенез) рака желчного пузыря
- Строение и функции поджелудочной железы
- Механизм развития (патогенез) пороков развития поджелудочной железы
- Механизм развития (патогенез) острого панкреатита
- Механизм развития (патогенез) хронического панкреатита
- Механизм развития (патогенез) кисты поджелудочной железы
- Механизм развития (патогенез) кистозных опухолей поджелудочной железы
- Механизм развития (патогенез) рака поджелудочной железы
Источник


