Регуляция инсулина и поджелудочная железа
Для нормального функционирования человеческому организму постоянно нужна глюкоза. Это и есть та жизненная сила, которая обеспечивает клетки энергией. На нужном уровне глюкозу держит гормон поджелудочной железы — инсулин. Только он помогает клеткам впитывать ее для своих энергетических нужд из крови. Инсулин вырабатывается в поджелудочной железе 24 часа в сутки, но наибольшее количество гормона поступает в кровь после еды. Нарушения работы поджелудочной по продуцированию инсулина приводят к диабету.
Гормональная функция поджелудочной железы
Поджелудочная железа вырабатывает инсулин. Без него невозможен обмен веществ в организме. За синтез гормона отвечают бета-клетки. В них содержатся:
- митохондрии — своеобразные энергетические станции;
- рибосомы, где, собственно, и происходит начальное формирование белка инсулина из аминокислот.
Далее «заготовка» поступает в сеть каналов аппарата Гольджи. Там завершается сборка молекул. По такой общей схеме бета-клетки вырабатывают инсулин.
Гормон, который вырабатывает поджелудочная железа, выделяется в кровоток в ответ на повышение уровня глюкозы. Глюкоза, не усвоенная сразу, связывается в молекулы гликогена в мышцах, печени и подкожной жировой клетчатке. Организм расходует эти запасы, если с момента последнего приема пищи прошло много времени, или после активной физической нагрузки.
Гликоген снова расщепляется на молекулы глюкозы, и в клетки поступает необходимая для жизнедеятельности энергия. Когда запасы мышц и печени истощены, организм приступает к использованию жира, который расщепляется на глицерин и жирные кислоты. И наоборот, если энергетические депо мышц и печени заполнены до отказа (при переизбытке простых углеводов), стартует преобразование глюкозы в жир.
Гликоген синтезируется почти во всех тканях организма, но наибольшие его запасы хранятся именно в печени и мышцах. После активной спортивной тренировки или другой сопоставимой с ней нагрузки гликоген в мышечной ткани быстро расходуется. Его запасы восстанавливаются в периоды отдыха и после приема богатой углеводами пищи. Гликоген в печени начинает снова преобразовываться в глюкозу, если организм не получает пищу на протяжении длительного времени.
В обмене веществ участвует также глюкагон, который является антагонистом инсулина. Именно этот гормон дает сигнал клеткам печени из своих запасов поставлять глюкозу в кровь. Он синтезируется альфа-клетками островков Лангерганса, которые содержит поджелудочная железа.
Кроме инсулина, поджелудочная железа вырабатывает ферменты, которые необходимы для нормального пищеварения.
Как происходит регуляция уровня глюкозы
Бета-клетки реагируют на содержание глюкозы в крови. При повышении уровня глюкозы бета-клетки стимулируют выработку инсулина. К количеству глюкозы особенно чувствительны инсулинозависимые мышечная и жировая ткани. На них приходится порядка двух третей клеточной массы в человеческом теле.
Если инсулин — это гормон поджелудочной железы, выполняющий функцию снижения уровня глюкозы в крови, то все остальные гормоны выполняют противоположную функцию, увеличивая его.
Гормональное регулирование также осуществляют:
- глюкагон;
- адреналин;
- глюкокортикоиды;
- соматотропин.
Помимо важнейшей задачи по снижению уровня сахара, действие инсулина на организм следующее:
- Повышает проницаемость клеток для проникновения в них глюкозы.
- Способствует усвоению белков.
- Обеспечивает синтез жирных кислот в печени.
- Помогает регенерационным процессам.
- Помогает усвоению микроэлементов.
- Препятствует попаданию жирных кислот в кровоток.
Норма инсулина в крови
Этот важный для обменных процессов гормон поджелудочная железа продуцирует постоянно. Однако наибольшее его количество выделяется после каждого очередного приема пищи. Нормы инсулина в крови разнятся в зависимости от возраста и пола:
- дети — 3-20 мкЕд/мл;
- люди преклонного возраста — 6-30 мкЕд/мл;
- мужчины и женщины — 3-25 мкЕд/мл;
- беременные женщины — 6-26 мкЕд/мл.
Если поджелудочная железа выделяет недостаточно гормона, это свидетельствует о нарушении ее работы. При определении уровня гормона и сопоставлении его с предельными показатели в первую очередь нужно ориентироваться на референтные значения (точные данные), используемые в конкретной лаборатории, где проводится исследование.
Изменение выработки инсулина — причины, симптомы и последствия
Процесс выработки гормона нарушается при наличии тех или иных заболеваний поджелудочной железы. В частности, панкреатит приводит к изменению тканей органа. В результате воспаления клетки, отвечающие за выработку ферментов и гормонов, гибнут, и их замещает соединительная ткань.
Если вы заметили у себя симптомы изменения уровня инсулина в крови, обязательно посетите врача.
В результате возникает не только внешнесекреторная недостаточность (проблемы с выработкой пищевых ферментов). Поджелудочная железа и инсулин оказывается неспособна вырабатывать в нужном количестве.
Однако не у всех пациентов патология развивается именно в такой последовательности. Бывает так, что пациенты, которым уже поставили диагноз «диабет второго типа», начинают страдать панкреатитом.
Почему появляется избыточная секреция
Повышенную выработку могут провоцировать различные факторы:
- нерегулярное и несбалансированное питание, изобилующее простыми углеводами;
- повышенные физические и психические нагрузки;
- ожирение;
- дефицит витамина Е и хрома.
Уровень гормона может подняться из-за болезней поджелудочной железы (речь идет о нарушении эндокринной функции органа), печени и опухолей в брюшной полости, а также при наступлении беременности. Низкие показатели могут говорить как о банальном физическом истощении (сильной усталости), так и о начале диабета.
Почему поджелудочная железа не вырабатывает инсулин
За нехваткой инсулина стоит гибель синтезирующих его бета-клеток из-за атак собственной иммунной системы. При недостатке гормона поджелудочной железы инсулина клетки не имеют возможности впитывать глюкозу, а уровень сахара в крови продолжает оставаться гораздо выше допустимых норм.
Лечение нарушений
До настоящего времени медицина не имеет однозначного ответа на вопрос, как заставить поджелудочную железу вырабатывать инсулин. Исследования в данной области продолжаются, и одно из перспективных направлений — трансплантация бета-клеток. Широкого распространения процедура пока не получила из-за высокой стоимости и сложностей с получением донорского материала.
Свою версию по этому поводу предложили ученые из Калифорнийского университета в Сан-Франциско. Согласно результатам исследования, некоторые случаи диабета связаны с тем, что бета-клетки начинают испытывать дефицит кислорода и теряют способность вырабатывать инсулин.
На этом принципе может базироваться инновационный метод борьбы с диабетом. Однако достаточных для его использования результатов ученые пока не представили. Поэтому крайне важно строго следовать разработанной лечащим врачом индивидуальной схеме инсулиновой терапии.
Диабет
Если происходит сбой работы поджелудочной железы, однозначно нарушается нормальный процесс выработки инсулина. Стопроцентной защиты от диабета первого типа не существует, поскольку огромное значение в его развитии играет генетическая предрасположенность. А вот профилактике инсулинонезависимого диабета (второго типа) можно и нужно следовать. Развивается заболевание из-за переизбытка углеводов в пищевом рационе и гиподинамии, то есть малоподвижного образа жизни.
По каким причинам происходит дефицит инсулина при диабете
Дефицит инсулина возникает, если речь идет о диабете 1 типа. При втором типе заболевания гормона более, чем достаточно, но клетки слабо реагируют на него и в результате не получают глюкозу в достаточном количестве. Аутоиммунный диабет возникает из-за атак со стороны иммунной системы бета-клеток поджелудочной и связан с наследственным фактором.
Первый тип чаще всего возникает у молодых людей. Редко его диагностируют у пожилых, которые из-за лишнего веса, неправильного питания и сопутствующих заболеваний в основном страдают вторым типом болезни. У этой группы пациентов дефицит инсулина может возникнуть, если заболевание из-за длительного некорректного лечения перейдет в первую форму.
Инсулиновая терапия
Инсулинозависимый диабет предполагает использование индивидуальной схемы приема инсулина, которую расписывает врач-эндокринолог. Когда и сколько инсулина колоть, определяют на основании результатов исследования, проведенного пациентом самостоятельно. Как минимум на протяжении недели он должен фиксировать, как изменяется уровень сахара в крови. Важнейшие показатели — уровни глюкозы перед сном и утром после пробуждения.
Ознакомившись с результатами исследования и сопутствующих обстоятельств (особенности питания пациента, образ жизни и физическая активность), лечащий врач примет решение, потребуется ли использовать продленный инсулин для поддержания уровня глюкозы натощак и следует ли колоть быстрый инсулин перед приемом пищи. Подобранная врачом схема инсулинотерапии дополняется корректно сбалансированной диетой.
Как избежать сахарного диабета при болезнях поджелудочной
При хронических заболеваниях поджелудочной железы высок риск развития сахарного диабета, но он все же не составляет 100%. При адекватном и своевременном лечении основного заболевания осложнений в виде диабета вполне можно избежать. Часто проблема заключается в игнорировании симптомов.
О неблагополучии поджелудочная железа сигнализирует регулярно возникающими болями. Если другие симптомы отсутствуют, боли купируют и считают, что проблема решена. А работа органа уже нарушена, и процесс может медленно прогрессировать. Спустя несколько лет к болевому синдрому добавляются другие неприятные симптомы. Мучает изжога, периодически возникает вздутие живота.
Если патологический процесс зашел слишком далеко, пациент теряет аппетит, его может часто беспокоить диарея. Симптомы являются следствием инсулиновых выбросов бета-клеток. При любых подобных симптомах крайне важно обратиться к врачу и после обследования пройти курс лечения. Только так можно предупредить развитие диабета второго типа.
При игнорировании симптомов клетки поджелудочной железы продолжают гибнуть. При дефиците инсулина уровень глюкозы в крови держится выше нормы. Развивается диабет, поджелудочная продолжает разрушаться. При одновременном лечении панкреатита и сахарного диабета стоят два важные задачи: восстановить углеводный обмен и наладить выработку пищеварительных ферментов.
Источник
Гормонами поджелудочной железы являются инсулин и глюкагон.
Глюкагон
Строение
Представляет собой полипептид, включающий 29 аминокислот с молекулярной массой 3,5 кДа и периодом полураспада 3-6 мин.
Синтез
Осуществляется в клетках поджелудочной железы и в клетках тонкого кишечника.
Регуляция синтеза и секреции
Активируют: гипогликемия, адреналин.
Уменьшают: глюкоза, жирные кислоты.
Механизм действия
Аденилатциклазный активирующий.
Мишени и эффекты
Конечным эффектом является повышение концентрации глюкозы и жирных кислот в крови.
Жировая ткань
- повышает активность внутриклеточной гормон-чувствительной ТАГ-липазы и, соответственно, стимулирует липолиз.
Печень
- активация глюконеогенеза и гликогенолиза,
- за счет повышенного поступления жирных кислот из жировой ткани усиливает кетогенез.
Патология
Гиперфункция
Глюкагонома – редко встречающееся новообразование из группы нейроэндокринных опухолей. У больных отмечается гипергликемия и поражение кожи и слизистых оболочек.
Инсулин
Дополнительная, более подробная информация, об инсулине находится на следующей странице.
Строение
Представляет собой полипептид из 51 аминокислоты, массой 5,7 кД, состоящий из двух цепей А и В, связанных между собой дисульфидными мостиками.
Синтез
Синтезируется в клетках поджелудочной железы в виде проинсулина, в этом виде он упаковывается в секреторные гранулы и уже здесь образуется инсулин и С-пептид.
Регуляция синтеза и секреции
Активируют синтез и секрецию:
- глюкоза крови – главный регулятор, пороговая концентрация для секреции инсулина – 5,5 ммоль/л,
- жирные кислоты и аминокислоты,
- влияния n.vagus – находится под контролем гипоталамуса, активность которого определяется концентрацией глюкозы крови,
- гормоны ЖКТ: холецистокинин, секретин, гастрин, энтероглюкагон, желудочный ингибирующий полипептид,
- хроническое воздействие гормона роста, глюкокортикоидов, эстрогенов, прогестинов.
Уменьшают: влияние симпато-адреналовой системы.
Механизм действия
Осуществляется через рецепторы с тирозинкиназной активностью (подробно).
Мишени и эффекты
Основным эффектом является снижение концентрации глюкозы в крови благодаря усилению транспорта глюкозы внутрь миоцитов и адипоцитов и активации внутриклеточных реакций утилизации глюкозы:
- активируя фосфодиэстеразу, которая разрушает вторичный мессенджер цАМФ, инсулин прерывает эффекты адреналина и глюкагона на печень и жировую ткань.
- в мышцах и жировой ткани стимулирует транспорт глюкозы в клетки (активация Глют-4),
- в печени и мышцах ускоряет синтез гликогена (активация гликогенсинтазы).
- в печени, мышцах и адипоцитах инсулин стимулирует гликолиз, активируя фосфофруктокиназу и пируваткиназу.
- полученный в гликолизе пируват превращается в ацетил-SКоА под влиянием активированного инсулином пируватдегидрогеназного комплекса, и далее используется для синтеза жирных кислот. Превращение ацетил-SКоА в малонил-SКоА, первый субстрат синтеза жирных кислот, также стимулируется инсулином (ацетил-SКоА-карбоксилаза).
- в мышцах усиливает транспорт нейтральных аминокислот в миоциты и стимулирует трансляцию (рибосомальный синтез белков).
Ряд эффектов инсулина заключается в изменении транскрипции генов и скорости трансляции ферментов, отвечающих за обмен веществ, за рост и деление клеток.
Благодаря этому индуцируется синтез ферментов метаболизма
- углеводов в печени (глюкокиназа, пируваткиназа, глюкозо-6-фосфатдегидрогеназа),
- липидов в печени (АТФ-цитрат-лиаза, ацетил-SКоА-карбоксилаза, синтаза жирных кислот, цитозольная малатдегидрогеназа) и адипоцитах (ГАФ-дегидрогеназа, пальмитатсинтаза, липопротеинлипаза).
и происходит репрессия фосфоенолпируват-карбоксикиназы (подавление глюконеогенеза).
Инактивация инсулина
Инактивация инсулина начинается после интернализации инсулин-рецепторного комплекса и образования эндосомы, в которой и происходит деградация инсулина. Участвуют две ферментные системы:
- Глутатион-инсулин-трансгидрогеназа, которая восстанавливает дисульфидные связи между цепями А и В, в результате чего гормон распадается.
- Инсулиназа (инсулин-протеиназа), гидролизующая инсулин до аминокислот.
Период полужизни инсулина не превышает 5-6 минут. Происходит деградация в основном в печени и почках, но и другие ткани принимают в этом участие. Также в почках инсулин может фильтроваться, захватываться эпителиоцитами проксимальных канальцев и разрушаться до аминокислот.
Патология
Гипофункция
Инсулинзависимый и инсулиннезависимый сахарный диабет. Для диагностики этих патологий в клинике активно используют нагрузочные пробы и определение концентрации инсулина и С-пептида.
Источник
Поджелудочная
железа выполняет две функции: экзокринную
(синтез и секреция пищеварительных
ферментов) и эндокринную (синтез и секре
ция гормонов). Эндокринную функцию
выполняют особые участки поджелудочной
железы — островки Л ангерганса, занимающие
около 1% ее объема. Эндокринные клетки
островков Лангерганса секретируют в
кровь:
—
инсулин ( б ет а -клет ки );
—
глюкагон ( а ль ф а -к лет ки );
—
сомат ост ат ин (делы п а -к лет ки ).
По
химической структуре эти гормоны
относятся к белково-пептидным, а их
основная физиологическая роль — регуляция
углеводного обмена.
5.1. Гормоны поджелудочной железы
I.
Инсулин — основной по количеству и
значению гормон остров ков Лангерганса.
Эффекты
дейст вия инсулина:
1)
гипогликем ическое дейст вие: инсулин
— единственный гормон, снижающий
концентрацию глюкозы в крови . В
частности, инсулин:
• повышает
проницаемость клеточных мембран для
глюкозы; инсулин регулирует поступление
глюкозы во все ткани, исключая ЦНС, нейро
ны которой являются инсулиннезависимыми
— могут потреблять глюкозу в отсутствие
инсулина;
• усиливает
утилизацию глюкозы в клетках — ее
превращение в гликоген и жиры;
2)
анаболическое действие : инсулин
стимулирует синтез и тормозит
распад
гликогена, жиров и белков, РНК, ДНК
(анаболический эффект).
2.
Глюкагон — антагонист инсулина —
повышает концентрацию глюкозы в крови,
усиливая глюконеогенез и расщепление
гликогена в печени. Г люкагон также
стимулирует распад белков и жиров.
Регуляция
секреции инсулина и глюкагона
В
основном, осуществляется глюкозой по
принципу отрицательной обратной связи.
Увеличение концентрации глюкозы в крови
приводит к увеличению секреции инсулина
и снижению секреции глюкагона; наоборот,
снижение концентрации глюкозы тормозит
секрецию инсулина и усиливает
секрецию глюкагона. Таким образом
концентрация глюкозы поддерживается
на постоянном уровне (рис. 11).
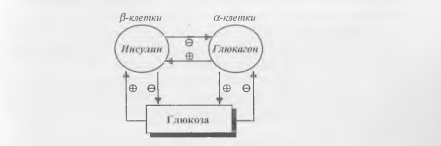
Рис.
11. Регуляция секреции инсулина и
глюкагона.
Дополнительную
петлю отрицательной обратной связи в
этой cистеме образуют инсулин и глюкагон:
глюкагон стимулирует секрецию инсулина,
а инсулин тормозит секрецию глюкагона.
Кроме того, секрецию обоих гормонов
подавляет соматостатин дельта-клеток
островков Лангерганса.
Следует
добавить, что секрецию инсулина усиливают
некоторые гормоны желудочно-кишечного
тракта (гастрин, секретин и др.); 2)
парасимпатические волокна блуждающего
нерва (через Механорецепторы). Наоборот,
секрецию инсулина угнетают 2) симпатические
волокна (через арадренорецепторы).
5.2. Регуляция концентрации глюкозы в крови
Нормальная
концентрация глюкозы в плазме крови
(натощак) составляет 3,5-5,5 ммоль/л. В
регуляции концентрации глюкозы в крови
участвуют несколько гормонов.
Снижает
концент рацию глюкозы единственный
гормон — инсулин. В норме секреция
инсулина повышается после приема пищи,
когда концентрация глюкозы в крови
может возрастать до 8-9 ммоль/л. Инсулин
способствует утилизации глюкозы тканями,
что необходимо для их энергообеспечения
и для создания энергетических запасов
(гликогена и жира).
Повышают
концентрацию глюкозы несколько гормонов
(их называют «контринсулярными»):
глюкагон, глю кокортикоиды, адреналин,
т ироидны е горм оны , соматотропный
гормон. Секреция этих гормонов усиливается
при гипогликемии или при стрессе. В
результате, концентрация глюкозы в
крови повышается за счет гликогенолиза
(распада гликогена) и глюконеогенеза —
синтеза глюкозы из неуглеводных
соединений: жирных кислот (их концентрация
увеличивается вследствие липолиза) и,
в крайнем случае, аминокислот (образуются
при распаде белков). Выходящая в кровь
глюкоза потребляется, в первую очередь,
нейронами ЦНС, которые с одной стороны,
практически не имеют собственных запасов
гликогена и поэтому очень чувствительны
к гипогликемии, а с другой стороны,
способны потреблять глюкозу в отсутствии
инсулина, секреция которого при стрессе
снижена.
Патология.
Нарушение регуляции уровня глюкозы в
крови может приводить к развитию
сахарного диабета, основным признаком
которого является стойкая гипергликемия
(концентрация глюкозы в крови натощак
превышает 7 ммоль/л). Повышается также
концентрация глюкозы в первичной моче,
вследствие чего замедляется реабсорбция
воды в почках, и увеличивается диурез
— количество вторичной мочи может
превышать 5 л/сут.
Механизмы
развития сахарного диабета разнообразны
и могут быть объединены в две группы:
1
) абсолютная недостаточность инсулина
— снижение секреции инсулина вследствие
генетических дефектов, иммунных поражений
(3-клеток островков Лангерганса,
заболеваний и повреждений поджелудочной
железы, недостаточности питания (прежде
всего белкового) и других причин;
2)
относительная недостаточность
инсулина — секреция инсулина в этом
случае не снижается, или даже повышается;
гипергликемия при этом связана со
снижением чувствительности тканей к
инсулину вследствие изменения рецепторов
инсулина, ожирения, гиперсекреции
контринсулярных г ормонов и других
причин. Например, сахарный диабет может
развиваться при акромегалии (гиперсекреция
СТГ), синдроме Иценко-Кушинга (избыток
глюкокортикоидов), гипертирозе
(гиперсекреция Т3, Т4), феохромоцигоме
(опухоль, продуцирующая катехоламины),
глюкагономе (опухоль, продуцирующая
глюкагон).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник