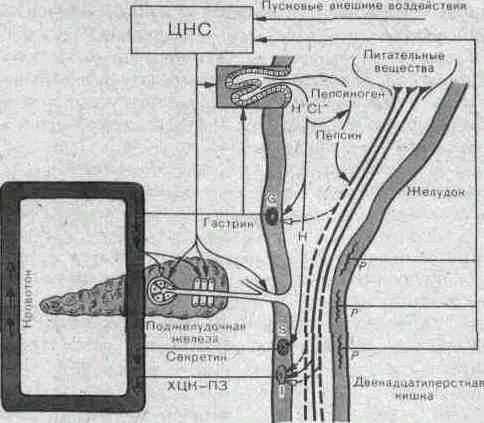
Секреция пищеварительных соков поджелудочной железы регулируется нервным и гуморальным путями
Слабое сокоотделение натощак резко
усиливается во время (через 2— 3 мин) и
после приема пищи. Панкреатическое
сокоотделение начинается уже на вид,
запах пищи как условно-рефлекторный
механизме секреции. При раздражении
пищевыми веществами рецепторов слизистой
оболочки ротовой полости, глотки и
пищевода возникает безусловно-рефлекторное
отделение панкреатического сока. Нервные
импульсы от раздражаемых рецепторов
по афферентным путям достигают бульбарного
центра панкреатической секреции, где
они переключаются на преганглионарные
нейроны ядер блуждающего нерва, по
эфферентным волокнам которого достигают
постганглионарных нейронов. Их аксоны
образуют синаптические окончания на
базальных мембранах панкреацитов.
Выделяющийся при возбуждении этих
окончаний ацетилхолин активирует
М-холинорецепторы постсинаптической
мембраны.
При раздражении чревных нервов,
осуществляющих симпатическую иннервацию
поджелудочной железы, ее сокоотделение
тормозится (за счет активации
р-адренорецепторов медиатором
норадреналином). Но торможение секреции
сопровождается накоплением секреторного
материала в панкреацитах.
Поступление пищи в желудок во время
приема пищи вызывает раздражение хемо-
и механорецепторов желудка.
Поступление в двенадцатиперстную кишку
желудочного содержимого вызывает вместе
с дуоденопанкреатическим секреторным
рефлексом (с рецепторов слизистой
оболочки) выделение из эндокринных
клеток гастро-интестинальных гормонов,
стимулирующих или тормозящих сокоотделение
поджелудочной железой.
Роль основных гуморальных регуляторов
выполняют секретин и ХЦК, которые
вырабатываются S- и ССК-клетками слизистой
оболочки двенадцатиперстной кишки.
Секретин и ХЦК усиливают влияние друг
друга на панкреоциты, особенно на фоне
выделения ацетилхолина в синаптических
окончаниях холинергических нервных
волокон, иннервирующих железу. Важным
гуморальным возбудителем панкреатической
секреции является гастрин.
4) Изменится ли амплитула потенциала действия нервной клетки, если на нее воздейсвовать стимулами сверхпороговой силы
это возбудимые ткани, амплитуда не
измен: так как действует закон «Все или
ничего»
Билет № 5
1.потенциал действия,с графиком,
возбудимость,мера возбудимости,
Потенциал
действия (ПД) – быстрое изменение
мембранного потенциала в ответ на
действия раздражителя пороговой силы.
ПД имеет стандартные амплитуду и
временные параметры, не зависящие от
силы стимула — правило «ВСЕ ИЛИ НИЧЕГО».
Начальная деполяризация мембраны под
действием раздражителя:

Если сила раздражителя достаточна,
чтобы деполяризовать мембрану до КУД,
открываются быстрые потенциал-зависимые
натриевые каналы. Клетка возбуждена –
возник нервный импульс.

Восстановление мембранного потенциала
покоя — реполяризация мембраны.

Следующий этап – восстановление
мембранного потенциала покоя —
реполяризация, обусловлена активным
ионным транспортом. Наиболее важен
процесс активного транспорта — это
работа Na/K- насоса, который выкачивает ионы натрия
из клетки, одновременно закачивая ионы
калия внутрь клетки. Восстановление
мембранного потенциала происходит
благодаря току ионов калия из клетки –
калиевые каналы активируются и пропускают
ионы калия до достижения равновесного
калиевого потенциала. Это процесс важен
потому, что до тех пор, пока не восстановлен
МПП, клетка не способна воспринимать
новый импульс возбуждения.
ГИПЕРПОЛЯРИЗАЦИЯ — кратковременное
увеличение МП после его восстановления,
которое обусловлено повышением
проницаемости мембраны для ионов калия
и хлора. Гиперполяризация бывает только
после ПД.
Деполяризация мембраны до КУД – могут
открыться любые натриевые каналы,
иногда кальциевые, и быстрые, и медленные,
и потенциал-зависимые, и рецептор-управляемые.
Это зависит от вида раздражителя и типа
клетокБыстрое поступление натрия в клетку —
открываются быстрые, потенциал-зависимые
натриевые каналы, и деполяризация
достигает точки реверса потенциала –
происходит перезарядка мембраны, знак
заряда меняется на положительный.Восстановление градиента концентрации
по калию – работа насоса. Калиевые
каналы активированы, калий переходит
из клетки во внеклеточную среду –
реполяризация, начинается восстановление
МППСледовая деполяризация, или отрицательный
следовой потенциал — мембрана еще
деполяризована относительно МПП.Следовая гиперполяризация. Калиевые
каналы остаются открытыми и дополнительный
ток калия гиперполяризует мембрану.
После этого клетка возвращается к
исходному уровню МПП. Длительность ПД
составляет для разных клеток от 1 до
3-4 мс.

Обратите внимание на три величины
потенциала, важные и постоянные для
каждой клетки ее электрические
характеристики.
МПП — электроотрицательность мембраны
клетки в покое, обеспечивающая способность
к возбуждению — возбудимость.КУД — критический уровень, величина
мембранного потенциала, при достижении
которой открываются быстрые, потенциал
зависимые натриевые каналы и происходит
перезарядка мембраны за счет поступления
в клетку положительных ионов натрия.
Чем выше электроотрицательность
мембраны, тем труднее деполяризовать
ее до КУД, тем менее возбудима такая
клетка.Точка реверса потенциала (овершут) —
такая величина положительного мембранного
потенциала, при которой положительно
заряженные ионы уже не проникают в
клетку — кратковременный равновесный
натриевый потенциал.
При действии раздражителя
подпороговой силы возникает неполная
деполяризация — ЛОКАЛЬНЫЙ ОТВЕТ (ЛО).
Неполная, или частичная деполяризация
– это такое изменение заряда мембраны,
которое не достигает критического
уровня деполяризации (КУД).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
пищи
—
трипсина и химотрипсина, а прием жирной
пищи вызывает секрецию сока с более
высокой его липолитической активностью.
Прием
одинаковой по характеру пищи длительное
время оказывает выраженное влияние на
деятельность поджелудочной железы.
Это влияние в основном состоит в
приспособлении количества и ферментного
состава сока к преобладающему
питательному веществу в рационе
питания человека и животного. Так,
преобладание белков повышает выделение
в составе панкреатического сока протеаз,
преимущественно углеводное питание
увеличивает выделение с соком амилазы,
а большое количество жира в рационе
снижает объем поджелудочной-секреции
и увеличивает содержание липазы в соке.
Секреция
поджелудочной железы регулируется
нервными и гуморальными механизмами.
И. П. Павлов в хронических и острых
опытах показал, что раздражение
блуждающего нерва обусловливает
выделение небольшого количества
поджелудочного сока, богатого ферментами.
Начальная
секреция поджелудочной железы вызывается
видом, запахом пищи и другими раздражителями
(условнорефлекторные
сигналы),
а также жеванием и глотанием
(безусловнорефлекторнЫе
сигналы).
При этом нервные сигналы, формирующиеся
в рецепторах полости рта и глотки,
достигают продолговатого мозга и затем
эфферентные влияния по волокнам
блуждающего нерва поступают к железе
и вызывают ее секрецию.
‘
У
человека, с фистулой поджелудочного
протока наблюдали.выделение
панкреатического сока через
2—3
мин после того, как ему говорили о пище,
которую дадут. Возбуждение
панкреатической секреции в данном
случае происходило условнорефлекторным
путём.
Симпатические
волокна, иннервирующие поджелудочную
железу, тормозят ее секреторную
активность. Поэтому после перерезки
чревных нервов у собак поджелудочная
секреция увеличивается. Симпатические
влияния, кроме того, имеют для железы
трофическое значение
—
они изменяют реактивность железы по
отношению к другим воздействиям,
усиливают синтез органических веществ
в ней.
Торможение
панкреатической секреции наблюдается
при раздражении многих центростремительных
нервов, при болевых реакциях, во время
сна, при напряженной физической и
умственной работе.
В
стимуляции панкреатической секреции
прямые нервные влияния имеют меньшее
значение, чем гуморальные.
Ведущее значение в гуморальной регуляции
секреции поджелудочной железы принадлежит
гастроинтестинальным гормонам
(рис.
187).
В
лаборатории И. П. Павлова было установлено,
что введение соляной кислоты в
двенадцатиперстную кишку вызывает
обильную секрецию поджелудочного сока.
В
1902
г. Бейлис и Старлинг показали, что
солянокислая вытяжка слизистой оболочки
двенадцатиперстной кишки, введенная
внутрйвенно, стимулирует поджелудочную
секрецию. Образующееся под влиянием
соляной кислоты в двенадцатиперстной
кишке вещество они назвали гормоном
секретином.
Секретин
вызывает выделение большого количества
поджелудочного сока, богатого
бикарбонатами, но бедного ферментами,
так как почти не действует на клетки
ацинусов, секретирующие ферменты.
Вторым
гормоном, усиливающим секрецию
поджелудочной железы, является
холецистокинин-панкреозимин.
Сначала считали, что это два разных
гормона. Один из них ‘(панкреозимин)
стимулирует секрецию поджелудочной
железы, а другой (холе-цистокин)
—
выход желчи в двенадцатиперстную кишку.
Теперь доказано, что это один гормон,
вызывающий несколько эффектов. В
наибольшей мере стимулируют высвобождение
этого гормона продукты начального
гидролиза пищевого белка и жира, а также
некоторые
аминокислоты. Стимулируют высвобождение
холе-цистокинина-панкреозимина соляная
кислота и углеводы.
Холецистокинин-панкрео-зимин
действует преимущественно на
панкреоциты ацинусов .поджелудочной
железы, поэтому выделяющийся в ответ
на действие этого гормона сок богат
ферментами. Одновременное влияние
на железу секретина и
холе-цистокинина-панкреозимина во время
приема пищи усиливает друг друга.
Рис.
187.
Регуляция секреции поджелудочной
железы.
I3
—
интерорецепторы;
G
—
гастринпродуцирующие клетки;
S
—секретинпродуцирующие
клетки:
1 —
холециетокинин-панкреози-мин (ХЦК-ПЗ)
-продуцирующие клетки;
Секреция
поджелудочной железы, усиливается’
также га-стрином,
серотонином, инсулином, бомбезином,
субстанцией П, солями желчных кислот.
Тормозят выделение поджелудочного
сока глюкагон,
кальцитонин, ЖИП, ПП, соматостатин. ВИП
может
возбуждать и тормозить панкреатическую
секрецию. Эффекты гормонов частично
опосредуются через их влияние на
желудочную секрецию:
с
усилением ее более кислое содержимое
поступает в двенадцатиперстную кишку
и посредством ее гормонов повышает
панкреатическую секрецию.
Нервные
влияния при приеме пищи обеспечивают
лишь пусковые
воздействия на железу,
а в коррекции панкреатической секреции
большую роль играют гуморальные
механизмы. Действие гормонов на железу
более выражено при сохраненной ее
иннервации, что подчеркивает единство
нервных и гуморальных механизмов
регуляции поджелудочной секреции.
Стимуляторы секреции поджелудочной
железы усиливают ее кровоснабжение,
что немаловажно для поддержания функции
железы на высоком уровне достаточно
длительное время.
Фазы
панкреатической секреции при стимуляции
ее приемом пищи те же, что и для желудочной
секреции, однако более выражены
гормональные влияния на поджелудочную
железу, особенно в кишечную фазу.
Источник
Оглавление темы «Функция всасывания кишечника. Пищеварение в ротовой полости и функция глотания.»: Гуморальная регуляция секреции пищеварительных соков и моторики желудка и кишечника. Гормональная регуляция пищеварительного тракта.Центральные, периферические и местные рефлексы осуществляются в тесном взаимодействии с гуморальным механизмом регуляции миоцитов, гландулоцитов и нервных клеток. В слизистой оболочке желудочно-кишечного тракта и в поджелудочной железе имеются эндокринные клетки, которые вырабатывают гастроинте-стинальные гормоны (регуляторные пептиды, энтерины). Эти гормоны через кровоток и местно (паракринно, диффундируя через межклеточную жидкость) оказывают влияние на миоциты, гландулоциты, интрамураль-ные нейроны и эндокринные клетки. Их выработка запускается рефлекторно (через блуждающий нерв) во время приема пищи и длительное время поддерживается за счет раздражающего влияния продуктов гидролиза пищевых веществ и экстрактивных веществ. Таблица 11.1. Гормоны желудочно-кишечного тракта, место их образования и вызываемые ими эффекты
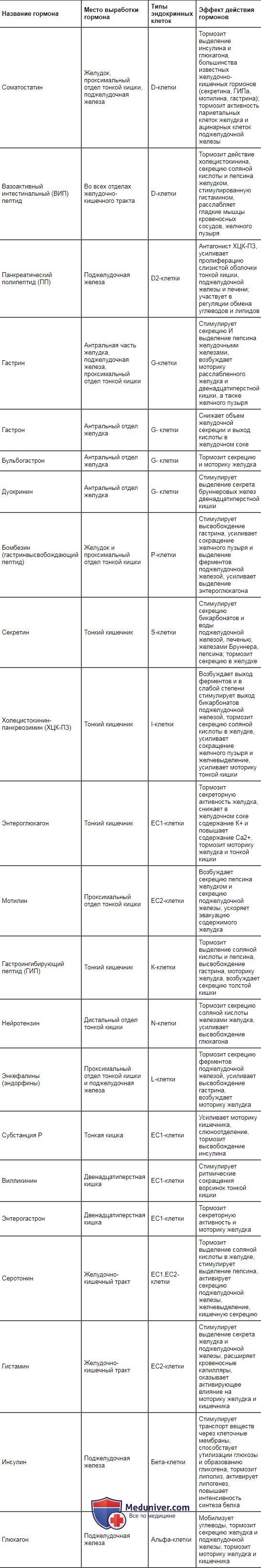 Место выработки основных гастроинтестинальных гормонов, вызываемые ими эффекты и продуцирующие их клетки представлены в табл. 11.1. В настоящее время обнаружено около 30 регуляторных пептидов. Как следует из представленной таблицы, они оказывают стимулирующее, тормозное и модулирующее влияние на секрецию пищеварительных соков, моторику гладкой мускулатуры желудочно-кишечного тракта, всасывание, выделение энтеринов эндокринными элементами слизистой оболочки желудка, кишечника и поджелудочной железы. Выделение гастроинтестинальных гормонов имеет каскадный характер. Например, под влиянием гастрина обкладочные клетки желез желудка увеличивают выработку соляной кислоты, которая в слизистой оболочке тонкой кишки стимулирует выделение S- и J-клетками секретина и холеци-стокинна — панкреозимина. Секретин усиливает секрецию воды и бикарбонатов поджелудочной железой и печенью, а холецистокинин — панкреозимин — возбуждает выделение ферментов поджелудочной железой и тормозит секрецию соляной кислоты обкладочными клетками, усиливает моторику тонкой кишки и желчного пузыря. Регуляторные пептиды, поступая в кровоток, быстро разрушаются в печени и почках и тем самым создают условия для осуществления эффектов других гастроинтестинальных гормонов. Выработка некоторых энтеринов носит циклический характер и может осуществляться и при отсутствии пищевого раздражителя. Например, мо-тилин, вырабатываемый ЕС2-клетками проксимального отдела тонкой кишки, вызывает сокращения мышц желудка и кишечника, совпадающие с периодами «голодной» активности пищеварительного тракта. — Также рекомендуем «Схема механизмов регуляции функций желудочно-кишечного тракта (жкт). Обобщенная схема механизмов регуляции функций пищеварительного тракта.» |
Источник