Анастомоз при раке поджелудочной железы
Оглавление темы «Операции при раке поджелудочной железы.»:
- Показания для панкреатикодуоденэктомии по Уипплу
- Доступ и ход операции панкреатикодуоденэктомии по Уипплу
- Показания для обходных анастомозов при неудалимом раке поджелудочной железы
- Доступ и ход операции обходного анастомоза при раке поджелудочной железы
- Показания для дистальной панкреатэктомии при раке поджелудочной железы
- Доступ и ход операции дистальной панкреатэктомии при раке поджелудочной железы
- Показания для центральной панкреатэктомии с панкреатикогастростомией
- Доступ и ход операции центральной панкреатэктомии с панкреатикогастростомией
Доступ и ход операции обходного анастомоза при раке поджелудочной железы
Вмешательство можно выполнить либо через двусторонний подрёберный доступ, либо через верхнюю срединную лапаротомию. Мы предпочитаем выполнение позадиободочной гастроеюностомии. В прошлом основным обходным желудочным анастомозом при неоперабельном периампулярном раке была впередиободочная гастроеюностомия.
После такой операции нередко возникала задержка опорожнения желудка, вследствие чего больные, не имевшие дуоденальной обструкции или застоя желудочного содержимого до операции, вынуждены были оставаться в стационаре на долгое время для лечения этого осложнения. Позже мы стали выполнять позадиободочную гастроеюностомию. Прооперировав более 200 больных, мы лишь в немногих случаях столкнулись с задержкой опорожнения желудка.
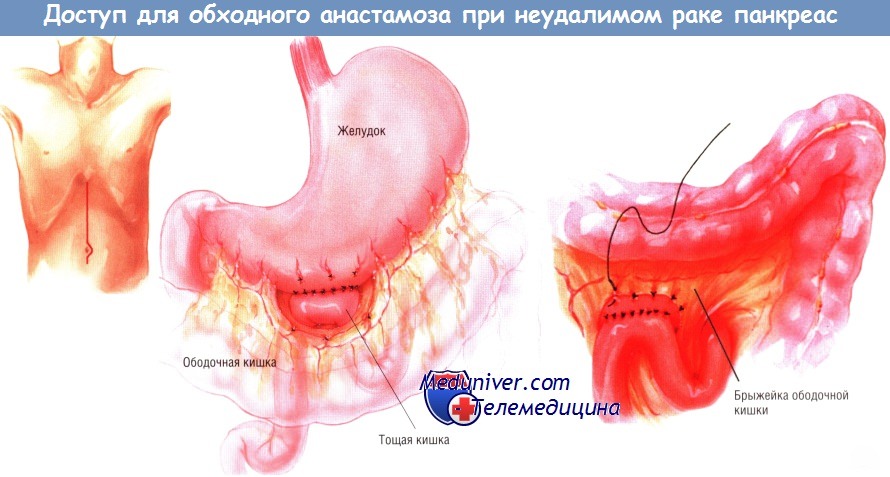
Большую кривизну желудка отделяют от сальника в наиболее свисающей области. После этого проксимальную петлю тощей кишки, расположенную чуть ниже связки Трейтца, протягивают кверху через отверстие в брыжейке поперечной ободочной кишки и накладывают гастроеюноанастомоз «бок в бок».
Внутренний непрерывный ряд швов создают синтетической рассасывающейся нитью № 3/0, тогда как наружный ряд отдельных узловых швов делают шёлком № 3/0. Соустье прикрепляют к отверстию в брыжейке ободочной кишки со стороны желудка, чтобы исключить образование внутренней грыжи, в которой могут ущемиться петли тонкой кишки.
Следующую петлю тощей кишки проводят наверх через отдельное отверстие в брыжейке поперечной ободочной кишки. Выполняют холецистэктомию, если она не была сделана ранее. Пересекают общий желчный проток и прошивают дистальный конец желчного дерева. После этого выполняют гепатикоеюностомию «конец в бок» одним рядом одиночных узловых швов синтетической рассасывающейся нитью № 4/0. Эта петля должна быть не меньше 45 см длиной.
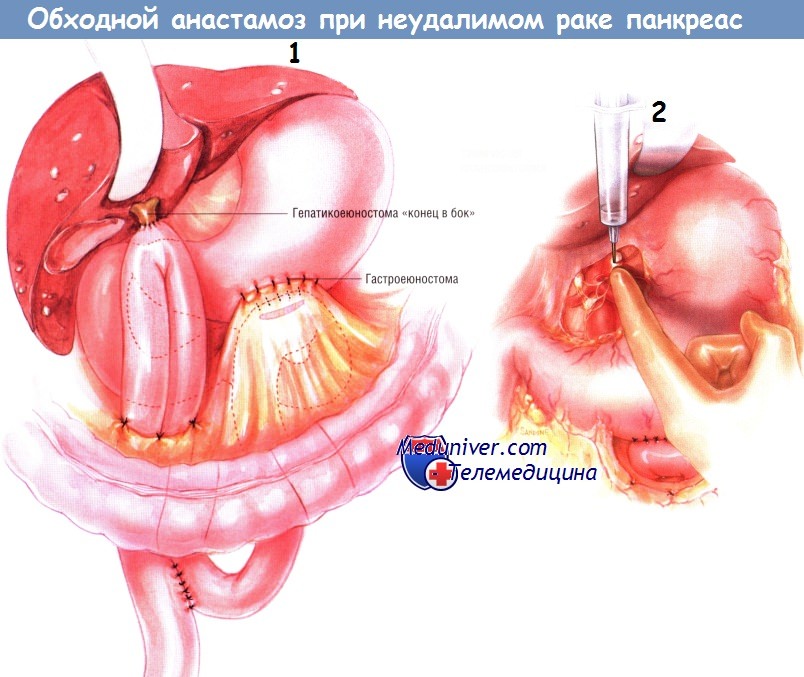
В её основании, между приводящей и отводящей кишками, делают анастомоз «бок в бок», расположенный ниже отверстия в брыжейке ободочной кишки. Внутреннюю линию швов этого соустья делают рассасывающейся синтетической нитью № 3/0, а наружную — одиночными узловыми шёлковыми швами № 3/0. Обе (приводящую и отводящую) ветви кишечника прикрепляют к отверстию в брыжейке поперечной ободочной кишки и друг к другу серией одиночных узловых швов шёлком № 4/0.
Химическая спланхнэктомия — рутинный этап данной операции. Её выполняют, инъецируя 20 мл 50% спирта по бокам от аорты на уровне чревного ствола. В результате происходит перерыв чревных нервов, идущих к чревному сплетению. Результаты химической спланхнэктомии были оценены в проспективном рандомизированном двойном слепом исследовании и свидетельствуют о том, что она уменьшает боли или предупреждает их возникновение в последующем.
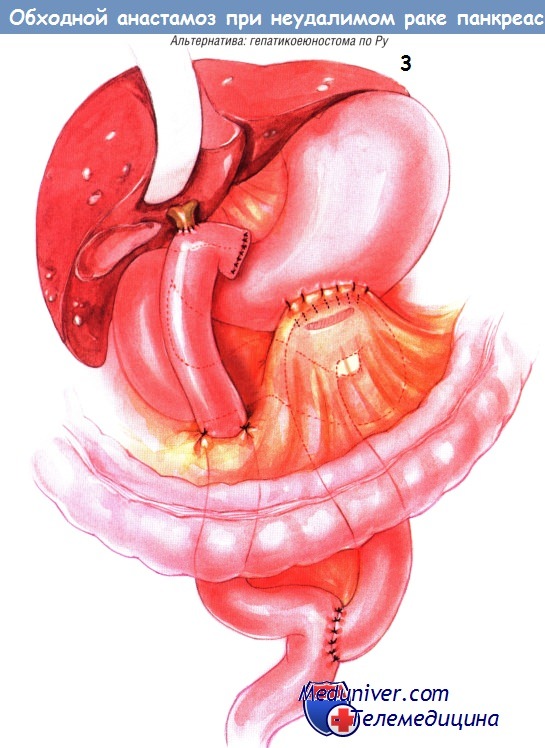
Альтернативный способ создания двойного обходного соустья — создание У-образного анастомоза по Ру дистальнее гастроеюностомы. Целостность пищеварительного тракта восстанавливают еюноеюностомией «бок в бок», её внутренний шов — непрерывный, из рассасывающегося синтетического материала, а наружный — из одиночных узловых швов шёлком № 3/0. Бранша анастомоза по Ру должна быть около 60 см длиной. Повторим вновь, что выполняют холецистэктомию и пересечение общего желчного протока. Дистальный отдел протока прошивают и перевязывают.
Гепатикоеюноанастомоз «конец в бок» выполняют одним рядом одиночных узловых швов синтетической рассасывающейся нитью № 4/0. Браншу анастомоза по Ру подшивают к отверстию в брыжейке поперечной ободочной кишки одиночными швами шёлком № 4/0.
— Также рекомендуем «Показания для дистальной панкреатэктомии при раке поджелудочной железы»
Источник
Ниже дан краткий обзор радикальных и паллиативных вмешательств при раке ПЖ.
В настоящее время хирургическое лечение остается единственно эффективным методом, однако опухоль можно удалить только на ранних стадиях (до 15% опухолей головки ПЖ), а операционный риск чрезвычайно высок. Радикальную операцию можно выполнить всего лишь у 1 — 5% больных, что обусловлено, в первую очередь, поздней диагностикой.
Выделяют следующие радикальные операции: гастропанкреатодуоденальная резекция, панкреатэктомия, дистальные комбинированные резекции ПЖ, расширенная субтотальная и тотальная панкреатодуоденэктомия. Радикальные операции технически очень сложны, их могут выполнить только высококвалифицированные хирурги в крупных центрах. Летальность после этих операций составляет от 27% при дистальной резекции ПЖ — до 17—39% при расширенной панкреатэктомии, пятилетняя выживаемость не превышает 8%. Последний факт обусловлен, прежде всего, тем, что у 50% больных в послеоперационном периоде возникает рецидив опухоли и в 90—95% случаев на первом году после операции развиваются отдалённые метастазы.
Существует мнение, что панкреатодуоденальную резекцию необходимо выполнять во всех случаях при подозрении на рак ПЖ даже без гистологической или цитологической верификации. Данное мнение отчасти обусловлено тем, что даже при лапаротомии и интраоперационном гистологическом исследовании частота ложноотрицательных ответов превышает 10%.
Перед операцией можно лишь предварительно судить о возможности удаления опухоли. Окончательное решение принимают после интраоперационного осмотра органов брюшной полости при исключении отдалённых метастазов и местной распространённости процесса. Наиболее часто во время операции обнаруживают такую причину нерезектабельности опухоли, как опухолевая инфильтрация забрюшинной клетчатки, включая нервные сплетения и поражение метастазами регионарных лимфатических узлов.
Панкреатодуоденальная резекция — основной тип радикальной операции при расположении опухоли в головке ПЖ. Нельзя её выполнить при прорастании опухолью нижней полой вены, аорты, верхней брыжеечной артерии и воротной вены. Для принятия окончательного решения следует отделить ДПК и головку ПЖ от подлежащих нижней полой вены и аорты, что позволяет судить и о вовлечённости верхней брыжеечной артерии; важна также оценка возможности диссекции воротной вены и верхней брыжеечной вены.
Удалённый при панкреатодуоденальной резекции анатомический препарат состоит из общего желчного протока, жёлчного пузыря, головки, шейки и секреторной части ПЖ, ДПК, проксимальной части тощей кишки, малого и части большого сальника, дистальной половины желудка. Кроме тою, иссечению подлежит паракавальная клетчатка, удаляют супрапилорические, инфрапилорические, передние и задние панкреатодуоденальные лимфатические узлы, лимфатические узлы гепатодуоденальной связки и по ходу общей печёночной артерии. Иссекают верхнюю брыжеечную вену (при изолированном опухолевом её поражении) или место се слияния с воротной веной. Такая лимфодиссекция улучшает прогноз, в то время как травматичность вмешательства увеличивается незначительно.
Простое перечисление удалённых органов свидетельствует о сложнейшей технике вмешательства. Ведь хирургу ещё предстоит выполнить серию восстановительных манипуляций — панкреатоностомию, билиодигестивный анастомоз (см. рис. 5-21), гастроеюностомию и межкишечный анастомоз. Средняя продолжительность операции составляет 6,5—7 ч.

Рис. 5-21. Стандартная панкреатодуоденальная резекция (операция Уиппла). Схема. В ходе операции удаляют общий жёлчный проток, жёлчный пузырь, двенадцатиперстную кишку, антральный отдел желудка, головку и часть тела поджелудочной железы: а — линии резекции; б — картина после резекции и перед реконструкцией (А-А — панкреатоеюноанастомоз, В-В — холедохоеюноанастомоз, С-С — гастроеюноанастомоз); в — состояние после резекции
Важны три технических приёма во время выполнения панкреатодуоденальной резекции — объём резекции паракавальной клетчатки и забрюшинной сосудистой диссекции, а также сохранение пилорического отдела желудка.
Особое внимание резекции паракавальной клетчатки уделяют потому, что именно в этой зоне чаще всего возникают рецидивы опухоли. Резекцию сосудов осуществляют при изолированном опухолевом поражении верхней брыжеечной вены или места её соединения с воротной веной. Прорастание верхней брыжеечной артерии чаще всего сопровождается обширным метастазированием в забрюшинные лимфатические узлы, что исключает возможность удаления опухоли.
Существуют мнения, что необходимо удалять узлы чревного сплетения, что позволяет существенно уменьшить выраженность болевого абдоминального синдрома в послеоперационном периоде, особенно в поздние сроки, когда заболевание прогрессирует.
Сохранение пилородуоденального сегмента при панкреатодуоденальной резекции улучшает пищеварительные функции и способствует более быстрому восстановлению массы тела больных.
Важно выявить зону первичного расположения опухоли в ПЖ, в первую очередь для исключения периампуллярных и ампулярных аденокарционом, имеющих значительно лучший прогноз.
Результаты стандартной панкреатодуоденальной резекции во многих больницах неудовлетворительные.
Послеоперационная летальность состав.ляет 12,3%, 1 год проживает 43,1% больных, средняя выживаемость больных составляет 15,5 мес, пятилетняя выживаемость не превышает 3,5—16.7%.
Неудовлетворительные отдалённые результаты, высокая послеоперационная смертность и техническая сложность панкреатодуоденальной резекции послужили основанием для отказа от радикальных вмешательств при раке ПЖ. Однако следует помнить, что репрезентативность результатов сравнительных исследований, проводимых в разных странах, может быть неодинаковой ввиду различий в диагностических критериях и подходах к стадированию рака ПЖ. В частности, в Японии применяют собственную классификацию опухолей ПЖ, отличающуюся от применяемых в США и Европе.
Выживают после гастропанкреатодуоденальной резекции лишь те больные, у которых по данным гистологического исследования послеоперационного материала по краям резекции нет опухолевых клеток. Напротив, в случаях их обнаружения больные живут приблизительно столько же, сколько больные после химиолучевого лечения.
При подтверждённом раке ПЖ выполняют ещё более объёмные операции — тотальную панкреатэктомию и расширенную панкреато-дуоденалъную резекцию. Необходимость в панкреатэктомии обусловлена важностью удаления мультифокальных очагов рака в ПЖ и более радикальным иссечением регионарных лимфоузлов (лимфатических узлов корня селезёнки, вокруг хвоста ПЖ). Несмотря на расширенный объём операции, показатели послеоперационной летальности сократились, однако отдалённые результаты от расширения объёма операции не улучшились, преимущественно за счёт развития тяжёлого сахарного диабета.
Расширенная панкреатодуоденальная резекция предусматривает удаление сегмента воротной вены и вовлечённых в опухолевый процесс артерий с реконструкцией сосудов. Кроме того, удаляют забрюшинные лимфатические узлы от чревной артерии до бифуркации подвздошных артерий. Разработчик техники этой операции Фортнер добился уровня отдалённой выживаемости 20% при послеоперационной летальности 23%.
При нерезектабельной опухоли, наличии или угрозе возникновения желтухи, гастродуоденальной непроходимости, если предполагаемая продолжительность жизни больного составляет более 6—7 мес, производят паллиативные вмешательства, в частности наложение билиодигестивного и гастроеюнального шунта (см. рис. 5-22).

Рис. 5-22. Паллиативные вмешательства при нерезектабельном раке поджелудочной железы. Схема: а — наложение обходного холецистоеюноанастомоза. В подавляющем большинстве случаев больные хорошо переносят операцию, несмотря на выраженную желтуху у ряда из них. Вмешательство обеспечивает достаточный отток жёлчи в кишку и уменьшение (или снижение выраженности) желтухи; б — другой тип обходного билиодигестивного анастомоза, который накладывают при угрозе прорастания опухоли в пузырный проток; в — гастроеюностомия; показана при блокировании опухолью двенадцатиперстной кишки
При предполагаемой продолжительности жизни 1-2 мес показано эндоскопическое введение стента в жёлчные протоки. Установка эндопротеза вместо хирургического шунтирования (холедоходуоденостомии и гастроэнтеростомии) подходит больным с тяжёлыми сопутствующими заболеваниями и липам старческого возраста. Она позволяет уменьшить число осложнений и смертность. Использование новых стентов из металлической сетки даст возможность увеличить продолжительность их нахождения в протоках и снизить частоту возникновения холангита. Рецидивирование желтухи после установления стента чаще всего связано с его обтурацией вследствие сладжа жёлчи; в этом случае проводят замену стента.
Предоперационное дренирование жёлчных протоков с целью уменьшения холестаза не приводит к увеличению продолжительности жизни больных. Недавно описана методика дренирующих малоинвазивных операций с целью декомпрессии жёлчевыводяших путей с помощью ЭУС, позволяющей более точно произвести стентирование.
Пример паллиативной операции — введение спирта (50 мл) или фенола в зону чревного сплетения дая купирования болевого абдоминального синдрома. Такой подход позволяет уменьшить боли или даже купировать их на короткое время, однако у 2/3 пациентов болевой синдром рецидивирует в течение месяца. Блокаду чревного сплетения можно выполнять повторно, однако эффективность следующих процедур более низкая. Тем не менее блокада чревного сплетения более эффективна, чем применение наркотических анальгетиков в сроки до 6 нед.
Появление методики нейролизиса чревного сплетения с использованием ЭУС повысило эффективность вмешательства ввиду большой точности определения зоны введения спирта. Боль проходит у 52% пациентов, а у 30% удаётся уменьшить суточные дозы наркотических анальгетиков.
Существуют указания об эффективности торакоскопической сплапхнэктомии в лечении болевого абдоминального синдрома. Для улучшения результатов хирургического лечения его дополняют химио-и лучевой терапией. Применяют эти методы не только после операции, но и интраоперапионно (введение в воротную вену или печёночную артерию фторурацила, митомицина). Возможны различные схемы комбинации лучевой, химиотерапии и хирургического лечения, введение препаратов в ткань опухоли под контролем ЭУС.
В последние годы всё чаще применяют трансплантацию ПЖ, селективную трансплантацию островковых и ацинарных клеток, что позволяет существенно улучшить качество жизни больных после панкреатэктомии по поводу ранних стадий негенерализованного рака ПЖ.
Маев И.В., Кучерявый Ю.А.
Источник
При необходимости хирургического лечения рака поджелудочной железы хирурги постоянно сталкиваются с альтернативой выбора объема операции. Мы проследили судьбу нескольких десятков больных раком поджелудочной железы, которым был наложен обходной билиодигестивный анастомоз и которые перенесли обширную панкреатодуоденальную резекцию. Срок жизни больных обеих групп оказался одинаковым и недолговечным.
При хирургическом лечении рака поджелудочной железы большинство хирургов производят три группы оперативных вмешательств — эксплоративную лапаротомию, наложение билиодигестивного анастомоза и радикальные операции — резекции поджелудочной железы, панкреатодуоденальные резекции и панкреатэктомии.
При раке периампулярной зоны может быть выполнена трансдуоденальная папиллэктомия и экономная панкреатодуоденальная резекция, рациональность производства которой спорна.
Основной критерий выбора объема хирургического лечения рака поджелудочной железы — операционная смертность — зависит не от ее предполагаемого размера и радикальности,а от того, в конечном счете, в какой стадии находится заболевание к моменту операции.
У трети больных невозможно вообще никакое хирургическое лечение рака поджелудочной железы, поскольку имеются метастазы в воротах печени, блокирующие магистральные желчные протоки, а также отдаленные метастазы.
В половине случаев возможно наложение билиодигестивного анастомоза. Показанием к выполнению паллиативных операций является сердечно-сосудистая недостаточность, старческий возраст, длительная желтуха, кахексия, опасение, что больной не перенесет радикальной операции.
Отбор больных на хирургическе лечение рака поджелудочной железы должен быть очень строгим. Предложено несколько видов разгрузочных анастомозов между желчным пузырем и общим желчным протоком, с одной стороны, и желудочно-кишечным трактом — с другой.
Наибольшую проверку временем выдержала операция, заключающаяся в наложении анастомоза между желчным пузырем и петлей тощей кишки. Преимуществом операции является возможность наложить соустье при любом положении желчного пузыря, а также в случаях, когда желудок или двенадцатиперстную кишку использовать для этой цели нельзя. Отрицательная сторона — необходимость наложения межкишечного соустья, что удлиняет операцию.
Длинную (до 50 см) петлю тощей кишки фиксируют к области дна желчного пузыря впередиободочно. После вскрытия пузыря и полости кишки размером 3 — 4 см накладывают непрерывный шов через все слои сначала на задние, а потом на передние губы анастомоза. Затем следует накладывание узловых швов на переднюю стенку анастомоза и формирование межкишечного анастомоза. Применение разного рода «заглушек», прошивание приводящей кишки ручным или механическим швом и других способов предотвращения кишечного рефлюкса в желчный пузырь представляется необязательным. Мы никогда не имели осложнений, связанных с методикой операции в ее классическом виде, и считаем ненужным удлинение времени операции. Наложение анастомоза между желчным пузырем и желудком мы считаем порочным, потому что давление в желудке выше давления в желчном пузыре и в этом случае гарантировано развитие холангита.
Анастомоз пузыря с двенадцатиперстной кишкой также не получил распространения из-за возможности дуоденального рефлюкса и, главное, из-за опухоли, развивающейся в области задней стенки кишки.
При наличии конкрементов, при сморщенном или деформированном желчном пузыре лучше наложить анастомоз между общим желчным протоком и петлей тощей кишки. В некоторых случаях эту операцию комбинируют с наложением гастроэнтероанастомоза.
При запущенных опухолях панкреатодуоденальной зоны с поражением общего желчного протока приходится выполнять высокие билиодигестивные анастомозы, подшивая петлю тощей кишки к воротам печени и выполняя соустье кишки с внутрипеченочными желчными протоками.
Резекцию поджелудочной железы производят при локализации опухоли в области тела и хвоста. В этих случаях речь идет о левосторонней гемипанкреатэктомии вместе с селезенкой. Подобную операцию выполняют при одной или нескольких инсуломах, которые не поддаются вылущиванию, при гиперинсулинизме, когда в поджелудочной железе опухоль не прощупывается (и ее не удается выявить до операции).
Разрез может быть продольным или поперечным, доступ к поджелудочной железе должен быть свободным и широким. После рассечения брюшины у места ее перехода с селезенки на брюшную стенку дистальный конец поджелудочной железы стараются вывихнуть в рану вместе с селезенкой. Далее раздельно перевязывают и пересекают селезеночные артерию и вену, пересекают в нужном месте поджелудочную железу (в пределах здоровых тканей). Мобилизованные органы вместе с клетчаткой удаляют. На культю главного панкреатического протока накладывают лигатуру, культю поджелудочной железы обрабатывают по одному из способов, предложенных в разные годы Е.Л. Березовым, В.В. Виноградовым, А.А. Шалимовым, B.C. Савельевым и В.Ш. Работниковым и другими хирургами.
Поджелудочную железу можно ампутировать в виде клина и на культю ее наложить П-образные шелковые швы. Было предложено наложение двух рядов швов (узловых и погружных, П-образных), погружение ушитой культи в забрюшинное пространство, наложение двойных П-образных швов через сальник и культю железы и др.
Во всех случаях целесообразно подвести к ложу железы эластичный дренаж.
При резекции хвоста железы методика остается принципиально такой же.
Панкреатодуоденальная резекция. Методика и оперативная техника панкреатодуоденальной резекции претерпела за последние годы ряд изменений и модификаций.
Выполнению панкреатодуоденальной резекции должна предшествовать деликатная, но тщательная ревизия органов панкреатодуоденальной зоны, определяющая операбельность больного. Следует осмотреть поджелудочную железу и брыжейку поперечной ободочной кишки, где возможно прорастание опухоли и наличие метастазов. Важное значение имеет установление взаимоотношения опухоли с нижней полой веной, общим желчным протоком, двенадцатиперстной кишкой, брыжеечными сосудами.
В технике операции различают несколько этапов.
Этап первый. Между браншами или с помощью сшивающего аппарата пересекают желудок, удаляя не менее его половины. Обнажают общую печеночную артерию, перевязывают у места отхождения правую желудочную и гастродуоденальную артерию.
Этап второй. Тупым путем смещают книзу клетчатку с печеночно-двенадцатиперстной связки, выделяют и перевязывают общий желчный проток ниже впадения в него пузырного протока.
Этап третий. Отделяя тупо воротную и брыжеечную вены, подводят под тело поджелудочной железы зажим и пересекают ее, отступая на 2 — 3 см от нижней границы опухоли, на уровне перешейка. На оставшуюся часть железы зажим не накладывают, выделяющийся панкреатический сок удаляют отсосом.
Этап четвертый. Отступя на 10 см от трейтцевой связки, пересекают тонкую кишку. Дистальный фрагмент ее перевязывают, проксимальный после перевязки мобилизуют и выводят из-под брыжеечных сосудов. Нижнюю панкреатодуоденальную артерию при этом перевязывают.
Этап пятый. Пересекают крючковидный отросток и его связку и удаляют одним блоком весь препарат, накладывая лигатуры на кровоточащие сосуды.
Этап шестой. После смены белья и обработки операционного поля пересеченную тощую кишку проводят через отверстие в брыже поперечной ободочной кишки и накладывают панкреатокишечный анастомоз так, чтобы культю поджелудочной железы частично инвагинировать в полость кишки. При этом часть поджелудочной железы и часть петли тонкой кишки ушивают так, чтобы диаметр пересеченного главного панкреатического протока совпал с диаметром оставленного отверстия в кишке. Накладывают швы на края обоих отверстий, при этом важно изолированное вшивание протока, что способствует лучшему сращению и функции панкреатокишечного соустья и является профилактикой расхождения швов.
Этап седьмой. Отступя на 20 см от места наложения панкреатокишечного соустья, накладывают холедохоэнтероанастомоз конец в бок так, чтобы культя протока лежала поперек кишки. Боковые края разреза общего желчного протока подшивают несколькими швами к стенке кишки, последнюю вскрывают и накладывают однорядный хо ледохоеюноанастомоз. Культю общего желчного протока инвагинируют в стенку кишки серозно-мышечными швами. Такой анастомоз функционирует хорошо, имитируя работу БСД в стенке двенадцатиперстной кишки.
Этап восьмой. Отступя еще на 40 см от места последнего анастомоза, накладывают соустье между культей желудка и кишкой, используя принцип Финстерера. Культю желудка по малой кривизне ушивают, после наложения анастомоза к ней фиксируют приводящую кишечную петлю для предотвращения рефлюкса желудочного содержимого.
При наличии конкрементов желчный пузырь удаляют, при отсутствии — сохраняют. К месту анастомозов лучше подвести резиновые дренажи, в брюшной полости также оставляют дренаж для подведения антибиотиков.
При начальных формах рака без поражения лимфатических узлов и прорастания опухоли, при раке БСД пересекают не тощую, а двенадцатиперстную кишку и головку поджелудочной железы мобилизуют вместе с общим желчным протоком. Дистальную часть кишки ушивают погружными кисетными швами, в остальном операцию проводят поэтапно, как и при первом варианте.
При тяжелом состоянии больного хирургическое лечение рака поджелудочной железы разделяют на два этапа, выполняя вначале разгрузочный билиодигестивный анастомоз на длинной петле, а через месяц остальную часть операции.
Это может быть гастроеюностомия или пересечение приводящей петли между энтероэнтероанастомозом и холецистоеюноанастомозом с последующим наложением первого анастомоза между культей поджелудочной железы и отводящим концом пересеченной петли и второго анастомоза между культей желудка и приводящим концом кишечной петли. При небольших локальных раках головки или БСД производят трансдуоденальную папиллэктомию либо экономную панкреатодуоденальную резекцию.
Существует методика резекции головки поджелудочной железы без нарушения целости двенадцатиперстной кишки. Во всех случаях речь идет об удалении опухоли и о полном или частичном сохранении двенадцатиперстной кишки.
Панкреатэктомия. Удаление всей поджелудочной железы (панкреатэктомия) применяют при тотальном поражении поджелудочной железы, при аденомах Золлингера — Эллисона, других формах аденоматоза, при условии нераспространения опухолевого процесса на соседние органы.
Зарубежные ученые в последние годы расширили показания к производству тотальных панкреатэктомий при хирургическом леченим рака поджелудочной железы. Мы отрицательно относимся к этой операции, считая, что она инвалидизирует больных, вызывая хроническую панкреатическую недостаточность.
Тело и головку мобилизуют слева направо, при этом пересекают общий желчный проток, тощую кишку, желудок, и весь конгломерат удаляют единым блоком. Пересеченный общий желчный проток вшивают далее в конец тощей кишки и накладывают гастроэнтероанастомоз. При доброкачественных опухолях пересечение двенадцатиперстной кишки производят у брыжеечных сосудов.
Осложнения хирургического лечения рака поджелудочной железы.
Реконструктивные операции в панкреатодуоденальной области нередко дают тяжелые осложнения в послеоперационном периоде. Важнейшими из них являются печеночная недостаточность, перитонит, панкреатит, шок, холемические кровотечения, поддиафрагмальные и межкишечные абсцессы, кишечная непроходимость, желчные свищи, пневмония.
Наиболее грозным осложнением является печеночно-почечная недостаточность. Ее предвестники — вялость, сонливость, безучастность больного, равнодушие к проводимому лечению, к боли, адинамия, отвращение к пище. При этом уменьшается диурез, в моче появляются цилиндры, эритроциты, белок, у больного наблюдаются отрыжка, икота, вздутие живота, сухость во рту. В тяжелых случаях гепатаргии вялость и апатия могут смениться бредом, больные поют, кричат, пытаются встать с постели, их состояние требует участия психиатра.
Чаще всего гепатаргия приводит к смерти. Большое значение имеет перевод больного на гемодиализ, подключение его к аппарату «искусственная печень». Лечение всегда складывается из мероприятий, направленных на борьбу с шоком (капельное вливание кровезаменителей, плазмы, электролитов, цельной крови, введение анальгетиков и наркотиков), борьбу с интоксикацией (та же терапия плюс антибиотики широкого спектра действия), профилактику легочных и сердечно-сосудистых осложнений (кардиотоники, антибиотики, кислород), борьбу с кровотечением и парезом кишечника. Особенностью пареза кишечника подобного рода является его стойкость, вызванная повреждением нервных сплетений. При этом происходит большая потеря белков и электролитов, что требует ежедневного введения хлорида натрия, хлорида калия на глюкозе, назначения стрихнина, паранефральной новокаиновой блокады, белковых жидкостей. Эффективно оставлять в желудке тонкий полихлорвиниловый катетер, позволяющий эвакуировать скапливающуюся жидкость. Вводимую и выделяемую из организма жидкость необходимо тщательно измерять во избежание гипогидратации и выведения воды из внеклеточных пространств, что усугубляет последствия обмена электролитов и водного обмена. Основным симптомом гипогидратации является сильная жажда, при этом отмечается сухость языка с появлением трещин, потеря массы тела, артериальная гипотензия, значительно повышается температура тела, учащается дыхание.
Если жидкость, наоборот, недостаточно выводится из организма, развивается гипергидратация, что сопровождается тошнотой, обильной рвотой, появлением отеков, олигурии.
Коррекция нарушенного обмена электролитов и водного обмена преследует цель нормализации обмена внутрисосудистой жидкости, восстановление общего количества воды, восполнение дефицита электролитов. Контроль за введением жидкости в организм должен отвечать элементарным требованиям: тщательная регистрация лабораторных показателей уровня электролитов, О ЦК, эритроцитов, гемоглобина, белка и др., регистрация точных количеств вводимых жидкостей и препаратов, строгий клинический досмотр за состоянием больного с фиксацией отдельных признаков заболевания.
Для лечения комы необходимо прекратить питание через рот, попытаться очистить кишечник с помощью клизмы, поставить постоянный катетер в желудок для эвакуации жидкости, вводить капельно в течение суток раствор глутаминовой кислоты, чередуя его введение с вливанием 5 % раствора глюкозы или изотонического раствора хлорида натрия.
Грозным симптомом является поражение почек, что сопровождается падением мочеотделения и повышением содержания в крови мочевины и остаточного азота. Постепенно состояние больных ухудшается, развивается кома. Повреждение канальцев почек при почечной недостаточности — процесс обратимый. Для его лечения необходимо ограничение жидкости, подавление инфекции (антибиотики широкого спектра действия), введение гормональных (преднизолон) и иммунодепрессивных (имуран) препаратов, альбумина, компенсация изменений солевого состава и щелочей, борьба с печеночной недостаточностью. Эффективным средством лечения является искусственный гемодиализ, проводимый повторно.
Послеоперационный некротический панкреатит после хирургического лечения рака поджелудочной железы у больных, уже ослабленных заболеванием и тяжелой операцией, протекает крайне неблагополучно и заканчивается смертельным исходом в связи с перитонитом и интоксикацией.
Лечение панкреатических, дуоденальных и высоких тонкокишечных свищей представляет собой отдельную хирургическую проблему. В результате активации панкреатического сока и пареза кишок на 3 — 5 день после операции создаются условия для расхождения швов анастомозов и последующего развития перитонита. Дренирование брюшной полости во время операции позволяет ограничить реактивное воспаление брюшины, но в дальнейшем на месте тампонов остаются стойкие свищи. Панкреатические свищи возникают наиболее часто. Борьба с ними предусматривает снижение панкреатической секреции, введение в полость свища ингибиторов трипсина, антибиотико- терапию, рентгенотерапию, повторное оперативное вмешательство — фистулоеюностомию.
Другие послеоперационные осложнения лечат по общим хирургическим принципам с индивидуальным успехом.
К поздним осложнениям хирургического лечения рака поджелудочной железы принято относить холангит, рубцевание и сужение анастомозов, сахарный диабет, эрозии желудочно-кишечного тракта, боли в животе, послеоперационные грыжи.
Статью подготовил и отредактировал: врач-хирург Пигович И.Б.
Видео:
Полезно:
Источник



