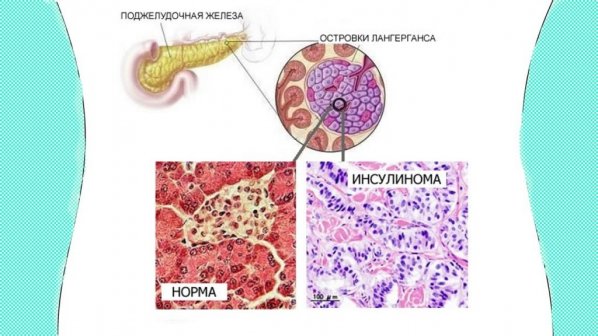
Диагностика секреторная функция поджелудочной железы
Оценка
внешнесекреторной функции поджелудочной
железы: осуществляется с помощью зондовых
(инвазивных, требующих введения кишечного
зонда) и беззондовых методов. Зондовые
методы (тесты) информативные, но
трудоемкие, Преимущество беззондовых
методов заключается в безопасности для
пациента и относительно низкой стоимости,
однако практически все они имеют низкую
чувствительность и специфичность по
сравнению с инвазивными методиками. !
(1)
стандартное копрологическое исследование:
повышенное содержание в кале нейтрального
жира и мыл при малоизмененном содержании
жирных кислот; повышенное количество
мышечных волокон в кале (креаторея) –
является более поздним, чем стеаторея,
признаком недостаточности поджелудочной
железы и свидетельствует о более тяжелой
степени нарушений;
(2)
количественное определение жира в кале
–
трудоемкий тест (норм количество жира
в кале менее 5 г/сут):
•
зондовые методы –
(1) секретин–панкреозиминовый тест
снован на оценке прироста секреции на
фоне введения секретина и холецистокинина;
; (2) непрямой зондовый метод (тест Лунда)
основан на сборе тонкокишечного
содержимого с помощью интубации после
приема стандартного пробного завтрака;
в зависимости от степени внешнесекреторной
недостаточности поджелудочной железы
чувствительность теста колеблется от
66 до 94%;
•
беззондовые методывсе
они основаны на пероральном введении
специфических субстратов для ферментов
поджелудочной железы; после взаимодействия
последних с ферментами поджелудочной
железы в моче и/или в сыворотке крови
определяются продукты расщепления, по
количеству которых судят о степени
внешнесекреторной недостаточности: 1
— бентирамидный тест* (NBT–PABA тест); 2 —
йодо-липоловый тест: липаза расщепляет
йодолипол до йодидов, которые определяются
в моче; 3 — флюоресцеин–дилауратный
тест.
*Бентирамидный
тест (NBT-PABA-тест). Основан
на том, что N-бензоил-L-тирозил-р-аминобензойная
кислота гидролизуется химотрипсином
до р-аминобензойной кислоты (PABA); затем
PABA всасывается, конъюгируется в печени
и экскретируется с мочой, где ее и
определяют.
•
определение степени потребления
плазменных аминокислот поджелудочной
железой:
метод основан на том, что при стимуляции
секретином или церулеином поджелудочная
железа поглощает из плазмы крови большое
количество аминокислот, необходимых
для синтеза панкреатических ферментов;
чувствительность метода составляет
69–96%, специфичность – 54–100%;
•
качественное копрологическое исследование:
общими критериями внешнесекреторной
недостаточности считаются повышенное
содержание нейтрального жира и мыл при
малоизмененном уровне желчных кислот,
увеличение содержания непереваренных
мышечных волокон, а также присутствие
в кале крупных фрагментов непереваренной
пищи;
•
количественное определение жира в кале:
метод основан на том, что после приема
100 г жира с пищей происходит выделение
с калом до 7 г нейтрального жира и жирных
кислот за сутки; увеличение его количества
свидетельствует о расстройствах
переваривания и всасывания жира;
•
определение фекального трипсина и
химотрипсина: тест
основан на измерении уровня трипсина
и химотрипсина в образцах кала
чувствительность теста составляет
70–90%, специфичность – 50–80%; при определении
содержания химотрипсина в кале получают
около 10% ложноотрицательных и 13%
ложноположительных результатов.
В
настоящее время наиболее информативным
способом оценки внешнесекреторной
функции поджелудочной железы служит
определение активности панкреатической
эластазы-1 (Е1) —
фермента поджелудочной железы, который
остается в неизмененном виде во время
его транзита по кишечнику. Концентрация
этого фермента в стуле отражает истинное
состояние экзокринной функции
поджелудочной железы. Концентрация Е1
в дуоденальном соке – 4-6% от общего
белка. Е1 стабильна при хранении образцов
кала: при +4-80С до 3-х дней; при -200С – до 1
года. В отличие от других методов
диагностики внешнесекреторной функции
определение Е1 в кале имеет следующие
преимущества:
• Е1 является абсолютно
специфичной для поджелудочной железы;
•
Е1 – самый стабильный фермент при
транзите по кишечнику и его количество
в кале в 5-6 раз выше, чем в дуоденальном
соке и концентрация Е1 отражает секреторную
способность поджелудочной железы. Таким
образом, с помощью теста на Е1 можно
определить или исключить наличие
экзокринной недостаточности поджелудочной
железы;
• результаты определения
коррелируют с результатами инвазивных
тестов;
• различия в концентрации Е1
кала, полученных от разных индивидуумов
очень незначительны;
• заместительная
ферментативная терапия не влияет на
концентрацию Е1 (моноклональные антитела,
используемые в данном тесте, не
взаимодействуют с эластазой животного
происхождения, которая присутствует в
ферментативных препаратах).
Источник
Для диагностики заболеваний ПЖ применяют следующие методы:
• исследование активности ферментов ПЖ в крови, моче;
• зондовые и беззондовые методы изучения экзокринной функции ПЖ;
• оценка инкреторной функции ПЖ (определение содержания С-пептида в крови, проба Штауба—Трауготта и др.);
• оценка трофической недостаточности.
Кроме того, для лабораторной диагностики заболеваний ПЖ используют иммунологические, генетические, цитологические, гистологические исследования, определение в крови уровня панкреатического полипептида, онкомаркёров СА 19-9, карциноэмбриональный антиген и др.
Исследование активности ферментов поджелудочной железы в крови и моче
Первую футтпу диагностических тестов обычно используют для обнаружения феномена выхода (уклонения) ферментов в кровь, который возникает при деструкции паренхимы органа и повышении внутрипротокового давления.
Ферменты поступают в интерстициальную жидкость, лимфу и кровь, а позже — в мочу. Панкреатические ферменты проникают в кровь также из секреторных ходов и протоков ПЖ. Кроме того, происходит всасывание ферментов в проксимальных отделах тонкой кишки.
Определение амилазы и её изоферментов
Плазма крови содержит а-амилазу двух изоэнзимных типов, продуцируемых ПЖ и слюнными железами (преимущественно околоушными):
• панкреатическую (р-тип);
• слюнную (s-тип).
Кроме того, амилолитическая активность обнаружена во многих тканях: тонком кишечнике, печени, почках, мышцах, лёгких, маточных трубах и жировой ткани. Это, однако, не означает, что все они синтезируют и транспортируют в кровь значительное количество амилазы. Доля амилолитической активности панкреатической а-амилазы составляет 30—50%. Р- и s-амилазы различны по физико-химическим свойствам, имеют разные почечные ктиренсы и периоды полураспада в организме (s-амилаза — 18 ч, р-амилаза — 124 ч).
Амилаза в крови находится в свободном (растворённом) и связанном с белками плазмы и форменными элементами состоянии.
Итак, определение активности амилазы в крови и моче — один из первых и наиболее распространённых биохимических методов диагностики панкреатитов. С 1908 г., когда Вольгемут разработал метод определения активности амилазы в биологических жидкостях, было предложено более двухсот методических приёмов проведения этого анализа.
Изоферменты амилазы измеряют во многих обычных лабораториях. Их определяют в сыворотке, моче или других биологических жидкостях при хроматографии, электрофорезе или изоэлектрическом фокусировании. Модификация амилазного теста — определение клиренсного отношения амилаза—креатинин, но этот тест требует сбора мочи в течение 24 ч. Результат выражают в процентах клиренсного отношения:Клиренсное отношение = (активность мочевой амилазы/активность сывороточной амилазы) X (сывороточный креатинин/мочевой креатинин) X 100
При ОП клиренсное отношение повышено, что можно объяснить увеличением активности панкреатического изофермента, имеющего больший клиренс (по сравнению с изоферментом s-тииа), и уменьшением канальцевой реабсорбции белков. Ввиду вариабельности изменений функций почек при ОП, ценность определения отношения клиренсов амилазы и креатинина вызывает серьёзные сомнения, и в практике этот метод широкого распространения не получил.
Существуют противоречивые сведения о стабильности а-амилазы: наряду с утверждением о том, что активность фермента стабильна при комнатной температуре в течение недели, есть данные о снижение её активности уже через несколько часов. Этим можно объяснить низкую восприимчивость метода. Невысокая чувствительность определения активности амилазы в крови и моче связана также с кратковременностью гиперамилаземии и гиперамилазурии при панкреатитах. Так, активность амилазы в крови начинает нарастать через 2— 12 ч от начала обострения заболевания, достигает максимума через 20—30 ч и при благоприятном течении заболевания нормализуется через 2—4сут.
Активность амилазы в моче начинает нарастать через 4—10 ч от начала заболевания, а через 8—10 ч уже может нормализоваться, но, как правило, сохраняется в течение 3 сут после подъёма.
В период обострения ХП активность амилазы в крови и моче может оставаться в пределах нормальных величин, так как у таких больных подъём активности фермента происходит на фоне исходно низкого уровня, связанного с фиброзом паренхимы ПЖ. При тяжёлом, прогрессирующем течении ОП или при обострении ХП активность амилазы может «истощаться» до нормальных и субнормальных величин. У 20% пациентов с ОП отмечают нормальные показатели активности амилазы сыворотки. Таким образом, по сывороточной активности амилазы невозможно определить тяжесть текущего обострения панкреатита и ближайший прогноз.
По данным литературы, определение активности амилазы в моче более информативно, чем в крови, так как гиперамилазурия более стойка, чем гиперамилаземия. Доступность получения мочи позволяет многократно повторять исследование и, следовательно, обнаруживать даже небольшой подъём показателя. Кроме того, вследствие различий в экскреции почками активность панкреатической изоамилазы в моче значительно выше, чем в крови.
Обострение XII сопровождается специфическим повреждением проксимальной части канальца нефрона, которое приводит к снижению реабсорбции и увеличению почечного клиренса, т.е. гиперамилазурия — результат гиперамилаземии и подавления канальцевой реабсорбции. Как уже отмечено, на этом основано определение соотношения клиренсов амилазы и креатинина. Более чувствительным, чем амилазурический тест, считают вычисление дебитовуроамилазы, когда исследуют мочу, собранную через определённые промежутки времени (до и после пищевой нагрузки). Чувствительность этих дебитов при ХП составляет 49-73%.
Для повышения чувствительности исследования активности амилазы в крови и моче необходимо проводить его в первые сутки пребывания больных ХП в стационаре, не менее двух раз после инструментальных исследований, а также в момент усиления болевого абдоминального синдрома. При этом чувствительность теста повышается с 40 до 75-85%.
Интерпретация результатов определения активности амилазы в крови и моче затруднена ещё и тем, что фермент содержат слюнные железы, толстая кишка, скелетные мышцы, почки, лёгкие, яичники, маточные трубы, следовательно, можно определять амилолитическую активность в молоке, слюне, слёзной жидкости и поте. Таким образом, возможно повышение её уровня в биологических жидкостях вследствие внепанкреатических причин (табл. 2-8): при перфорации язвы, кишечной непроходимости, перитоните, тромбозе брыжеечных сосудов, холецистите, холангите, паротите, почечной недостаточности, внематочной беременности, остром аппендиците, раке лёгких, диабетическом ацидозе, феохромоцитоме; после операций по поводу пороков сердца, резекции печени; при употреблении препаратов опия, сульфаниламидов, тиазидных диуретиков, оральных контрацептивов.
Таблица 2-8. Причины гиперамилаземии

Для повышения специфичности гиперамилаземии предложено считать диагностически значимым повышение активности фермента в 3—6 раз. Однако патогномоничной для панкреатита активности фермента в крови не существует. Вследствие значительного запаса фермента в ацинарных клетках любое нарушение их целостности или малейшее затруднение оттока секрета ПЖ приводит к значительному выходу амилазы в кровь даже при легком течении панкреатита.
Для повышения специфичности исследования активности фермента в крови следует определять не суммарное его содержание, а панкреатическую фракцию. У здоровых людей р-амилаза составляет до 40% общей сывороточной амилазы, остальные 60% представлены слюнным изоферментом. При панкреатитах это соотношение изменяется: активность панкреатической изоамилазы составляет 75—80% активности общей амилазы крови. Определение активности р-амилазы особенно важно больных с ХП и нормальной активностью общей амилазы.
Повышение показателя указывает на обострение ХП, а снижение — на экзокринную недостаточность ПЖ, связанную с атрофией ацинарной ткани и фиброзом органа у больных, перенёсших ряд атак. Специфичность определения активности панкреатической амилазы при ХП не превышает 88,6%, чувствительность — 40—96,9%.
Маев И.В., Кучерявый Ю.А.
Источник
Панкреатит — заболевание, которым страдает наиболее трудоспособная часть населения. Частота его неуклонно растет, а диагностика и лечение представляют значительные трудности.
По мере прогрессирования заболевания хронический панкреатит (ХП) сопровождается развитием функциональной панкреатической недостаточности вследствие потери функционирующей паренхимы органа из-за воспалительной деструкции и формирования фиброза ткани. Секреция поджелудочной железы (ПЖ) играет ключевую роль в реализации пищеварения в целом и в реализации пищеварения в тонкой кишке — в особенности [1]. Фиброз и атрофия ПЖ приводит, помимо снижения секреции ферментов, также к уменьшению секреции бикарбонатов и существенному снижению объема панкреатического секрета. При ХП фиброзная инфильтрация ведет к уменьшению количества островков Лангерганса и их дисфункции. Гормоны, вырабатывающиеся в клетках островков, оказывают влияние на функцию ацинарных клеток: инсулин усиливает выделение панкреатического сока, а соматостатин и панкреатический полипептид ингибирует секрецию энзимов [2, 3]. В настоящее время выявлено, что топографическое расположение островков и ацинарной ткани позволяет осуществлять регуляцию экзокринной функции ПЖ через островки, что подтверждается открытием портального капиллярного круга кровообращения ПЖ, наличие которого обеспечивает попадание гормонов непосредственно из островков на соседние ацинусы. Артериальное кровоснабжение осуществляется сначала через альфа- и дельта-клетки, и только потом кровь попадает к бета-клеткам. Гормоны, секретируемые альфа- и дельта-клетками, могут в высокой концентрации достигать бета-клеток и затем — ацинарной ткани ПЖ [4]. В эксперименте показано, что инсулин повышает транспорт глюкозы и аминокислот в ацинарной ткани, синтез и фосфорилирование белков, холецистокинининдуцированную секрецию амилазы [5]. Гипоинсулинемия приводит к ингибированию роста ацинарных клеток и синтеза панкреатических энзимов [6]. С другой стороны, выявлено участие гастроинтестинальных гормонов в регуляции секреторной деятельности бета-клеток. Продемонстрировано стимулирующее влияние на секрецию инсулина секретина, холецистокинина, гастрина — гормонов, регулирующих экзокринную функцию ПЖ [7, 8].
Развитие сахарного диабета (СД) при ХП варьирует между 30–83%. Среди заболеваний поджелудочной железы, сопровождающихся развитием СД, на долю ХП приходится 76%. По данным различных авторов признаки развития СД при ХП алкогольной этиологии выявляются в 30–50% случаев. Панкреатогенный СД ухудшает качество жизни и является самостоятельным фактором риска смертности при ХП [9–14]. Иммуноцитохимическими исследованиями ткани ПЖ установлено, что снижение секреции инсулина у больных ХП является следствием уменьшения количества бета-клеток островков Лангерганса [15, 16]. Эти изменения зависят от степени воспалительного процесса в ПЖ, длительности и тяжести заболевания. Так, у больных с кальцинозом, перенесших обширный панкреанекроз, нарушения эндокринной функции в той или иной степени выявляются в 90% случаев [17]. Повышение плазменного уровня амилина у больных ХП может являться, по мнению ряда авторов, маркером нарушения эндокринной функции при панкреатитах [18]. Пока сохраняется 20–40% бета-клеток, глюкоза и уровень инсулина в крови при ХП находятся в пределах нормы [2, 7]. Выделение же инсулина на стимуляцию глюкозой чаще всего снижается. Больные с панкреатическим диабетом имеют сниженную инсулиновую активность. Факторы, ответственные за развитие панкреатогенного диабета, включают: снижение массы панкреатических островков и их функции, нарушение секреции гастроинтестинальных гормонов и последствия оперативного лечения панкреатита [15]. Альфа-клетки подвержены деструкции так же, как и бета-клетки, то есть при ХП уровень глюкагона и его резервные возможности могут быть снижены, что способствует развитию гипогликемии. Гипогликемия является частым осложнением СД при ХП, как результат нарушенного отложения гликогена, вследствие неадекватного потребления калорий по причине приема алкоголя или мальабсорбции. Длительная гипогликемия может быть смертельной. Больные с СД, обусловленным ХП, характеризуются нестабильным течением диабета, сниженным потреблением инсулина, устойчивостью к кетоацидозу [19].
Таким образом, в регуляции эндокринной деятельности ПЖ имеет место интегральное воздействие целого ряда гормонов желудочно-кишечного тракта, которые влияют на функцию бета-клеток ПЖ в процессе пищеварения. Инсулин является усилителем и модулятором влияния желудочно-кишечных гормонов на ацинарные клетки. С другой стороны, СД 1-го и 2-го типа протекает с нарушением внешнесекреторной функции ПЖ и диспепсическими расстройствами [20–22]. Дефицит инсулина любого генеза рассматривается как основная причина развития фиброза, жировой дегенерации и атрофии ацинарных клеток [23]. Частота развития осложнений при СД, обусловленных ХП, такая же, как и при других формах СД, и зависит от длительности диабета и адекватности терапии [7].
Целью исследования явилось: выявление особенностей течения ХП, осложненного СД, и обсуждение принципов консервативной терапии.
Материалы, методы и результаты исследования
Обследовано 66 больных ХП в возрасте от 30 до 65 лет (55 мужчин и 11 женщин), средний возраст 46,8 ± 9,2 года. Заболевание сопровождалось у 22 (33,3%) больных формированием кальциноза ПЖ, у 13 (19,7%) — кист ПЖ, у 5 (7,6%) диагностирована псевдотуморозная форма ХП и 10 (15,2%) больных имели клиническое и лабораторное подтверждение наличия СД. У 23 (34,9%) больных в период обострения заболевания отмечалось значительное повышение уровня глюкозы крови натощак, а в период ремиссии он колебался в пределах 6,1–6,9 ммоль/л. По поводу осложненного течения ХП проведено 14 резекционных и 11 дренирующих операций на ПЖ. Диагноз ХП был поставлен на основании клинических, инструментальных, лабораторных данных. Этиологическими причинами заболевания у 50 больных было злоупотребление алкоголем, а у 6 — желчнокаменная болезнь, у 10 — этиологическая причина не выяснена.
Внешнесекреторную функцию ПЖ оценивали по результатам дыхательного теста с использованием 13С-триоктанаина, который предназначен для диагностики in vivo внешнесекреторной функции ПЖ, исследования метаболизма жиров. Триглицериды, содержащие различные жирные кислоты, являются основными компонентами природных жиров. Действующее фармакологическое вещество — 1,3-дистерарил-2-(I-13С) октаноилглицерол, меченный стабильным изотопом углерода. Он метаболизируется в два этапа. На первом этапе происходит отщепление 1-13С-каприловой кислоты в позициях 1, 3, происходящее, в основном, под действием липазы, синтезируемой ПЖ. На втором этапе происходит всасывание отщепленных молекул каприловой кислоты и 2-(1-13С)-монооктаноилглицерола, которому может предшествовать его расщепление до каприловой кислоты. Каприловая кислота при поступлении в тонкую кишку быстро всасывается, связывается с альбумином крови и через систему портального кровотока либо лимфатическую систему и систему общего кровообращения в составе липопротеинов доставляется в печень. Основной канал метаболизма каприловой кислоты — митохондриальное бета-окисление, приводящее к образованию бикарбонат-иона, содержащего углерод-13, который пополняет бикарбонатный пул крови. Это приводит к увеличению доли углерода-13 в углекислоте выдыхаемого воздуха. 13С-триоктаноин-тест проводился натощак. Процедура проведения занимает 6 часов. Во время исследования больному запрещалось курить, проявлять физическую активность и принимать пищу. Для проведения теста готовили тестовый завтрак. До и после приема тестового завтрака больной проводил сбор образцов выдыхаемого воздуха в специальные пронумерованные коллекторы. В коллектор № 1 — образцы воздуха до приема завтрака, затем с интервалом 30 минут в остальные пронумерованные коллекторы. Вывод о состоянии внешнесекреторной функции ПЖ делается на основании обработки полученных данных по суммарной доле выделенной изотопной метки к исходу шестого часа дыхательного теста. Точкой разделения пациентов с нормальной и нарушенной функцией ПЖ является величина 44%. Если суммарная доля выделяемой метки меньше указанной величины, то это указывает на нарушение внешнесекреторной функции ПЖ.
Содержание С-пептида и антител к инсулину определяли в крови иммуноферментным методом с помощью наборов реактивов (AccuBind, США; Orgentec, Германия).
Результаты исследования и их обсуждение
Полученные результаты по данным дыхательного теста свидетельствовали о снижении экзокринной функции ПЖ у больных с ХП как с осложнениями, так и без осложнений при сравнении с нормой 44% (24,3 ± 1,7 и 26,6 ± 1,3% соответственно). Значительное снижение суммарной доли выводимой метки наблюдается у больных с ХП и кальцинозом ПЖ, СД, после резекционных операций по поводу осложнений ХП (табл. 1), и имелись достоверные различия при сравнении с группой больных ХП без осложнений. Уровень же С-пептида в этих группах больных снижался и достоверно отличался при сравнении с группой больных ХП без осложнений (табл. 2), а у больных ХП и СД был снижен до 0,11 ± 0,02 нг/мл, при норме 0,7–1,9 нг/мл, то есть ниже минимальных значений нормы. У больных ХП с нарушением глюкозы натощак уровень С-пептида составил 1,22 ± 0,14 нг/мл, а у больных ХП без признаков нарушения углеводного обмена 1,76 ± 0,12 нг/мл. Выявлена прямая корреляционная зависимость между уровнем С-пептида и показателями дыхательного теста у больных ХП после резекционных операций (r = 0,84, p = 0,03). Антитела к инсулину не определялись во всей группе исследуемых больных. При ХП, осложненном СД, у 7 больных выявлялся кальциноз, у 5 — были проведены резекционные операции, 3 больных имели кальциноз ПЖ, и у них проведены резекционные операции на ПЖ. Этиологической причиной панкреатогенного СД, или СД 3-го типа, в нашем исследовании был алкоголь. Таким образом, можно заключить, что у больных ХП при формировании кальциноза ПЖ, резекциях ПЖ можно прогнозировать развитие СД, что подтверждается и литературными данными. Раннее развитие кальцификации и проведение панкреатодуоденэктомии являются факторами риска формирования СД. Так, при наличии кальцификации опасность развития СД увеличивается в 3 раза, а после тотальной панкреатэктомии СД развивается во всех случаях, после резекционных операций на ПЖ в 40–50%. Такие осложнения ХП, как псевдокисты, дуоденостеноз, холедохостеноз, тромбоз селезеночной и воротной вен, не являются факторами риска присоединения СД [24, 25]. Нарушение внешнесекреторной функции ПЖ у больных панкреатогенным СД чаще всего бывает тяжелой степени, то есть экзокринная и эндокринная недостаточность развиваются параллельно. Антитела к инсулину во всей группе исследуемых больных ХП были отрицательные, что еще раз доказывает специфический тип СД при ХП. Антитела к инсулину могут выявляться только при СД 1-го типа [26]. При СД 1-го и 2-го типа экзокринная недостаточность чаще бывает легкой и умеренной. Особое внимание следует обратить на тот факт, что на практике чаще всего неверно диагностируют СД 1-го или 2-го типа, а не СД 3-го типа, но между этими типами СД имеются различия как в патогенетических механизмах развития заболевания, так и в лечебной тактике (табл. 3) [13, 25].
Лечение СД при ХП должно быть индивидуальным и проводится инсулином. Поддержание оптимального уровня глюкозы может предотвратить микроциркуляторные осложнения. В настоящее время инсулинотерапия проводится различными методами с применением различных форм инсулина. Используют, как правило, препараты человеческого генно-инженерного инсулина. Оптимальным является режим интенсифицированной инсулинотерапии с введением инсулина короткого действия перед каждым приемом пищи и инъекцией инсулина пролонгированного действия перед сном. Такая терапия позволяет имитировать физиологическую секрецию инсулина, при которой имеется базисный уровень гормона в крови и пик его секреции — в ответ на пищевые раздражители. Доза инсулина пролонгированного действия составляет около половины общего количества вводимого инсулина [7, 26]. Кроме того, больные СД при ХП должны обязательно получать ферментную заместительную терапию в адекватных дозах постоянно, что оказывает положительное влияние на компенсацию диабета. Влияние заместительной терапии на метаболизм глюкозы у больных СД, имеющих экзокринную недостаточность ПЖ, остается до конца не решенным. В одних исследованиях было установлено улучшение контроля глюкозы в крови и снижение гликированного гемоглобина (HbA1c) у больных СД и экзокринной недостаточностью, получавших заместительную терапию, в других — этот эффект отсутствовал, но течение сахарного диабета стало более стабильным [27]. Кроме того, ферментным потенциалом пищеварительных желез обозначается относительное количество синтезируемых железами ферментов, состоящее в прямой зависимости от величины клеточного пула-продуцентов ферментов. У больных ХП с осложненным течением заболевания после ПДР происходит значительное снижение ферментного потенциала ПЖ [28]. Среди препаратов, используемых для ферментной заместительной терапии, можно выделить Креон®. Дозировка препарата — 10 000, 25 000 и 40 000 ЕД ЕФ. При подборе ферментного препарата для заместительной терапии определяющим является активность липазы. Это связано с тем, что при заболеваниях ПЖ продукция и секреция липазы страдают раньше, чем амилолитических и протеолитических ферментов. Липаза быстрее и более выраженно инактивируется при закислении двенадцатиперстной кишки (ДПК) из-за снижения продукции панкреатических бикарбонатов. При снижении рН в ДПК происходит преципитация желчных кислот, что усугубляет нарушение всасывания жира. Доза препарата при СД, обусловленном ХП, обычно не менее 25 000–40 000 ЕД ЕФ на один прием и не менее 100 000–180 000 ЕД ЕФ в сутки. О необходимости применения высоких доз ферментных препаратов у больных с тяжелой степенью панкреатической недостаточности имеются указания в литературных источниках последних лет [29].
Литература
- Beger H. G., Matsuno S., Cameron J. L. (ed.) Diseases of the Pancreas. Springer, Berlin Heidlberg New York. 2008. 949 p.
- Кloppell G., Maillet B. Pathology of acute and chronic pancreatitis // Pancreas. 1993. Vol. 8. P. 659–670.
- Leeson T. S., Paparo F. F. Text/Atlas of Hystology. Philadelphia; L. Toronto, 1988. P. 463–475.
- Keller J., Layter P. Acinar-islet interactions: Pancreatic exocrine insufficiency in diabetes mellitus In: Johnson C. D., Imre C. W. et. al. Pacreas disease: Basic science clinical management. London, 2004. 21. P. 267–278.
- Karlsson Sven, Ahren B. O. Cholecystokinin and Regulation of Insulin Secretion // Scand. J. Gastroenterol. 1992. Vol.27. P. 161–165 m.
- Czako L., Hegyi H., Rakonczay J. Z., Jr. et. al. Interactions between the endocrine and exocrine pancreas and their clinical relevanc // Pancreatology. 2009, vol. 9 (4), p. 351–359.
- Pedersen N., Larsen S., Seidelin J. B., Nielsen O. H. Alcohol Modulates Levels of Interleukin — 6 and Monocyte Chemoattractant Protein — 1 in Chronic Pancreatitis // Cand. J. of Gastrenter. 2004. Vol. 39, № 3, p. 277–282.
- Sjoberg R. J., Ridd G. S. Pancreatic diabetes mellitus // Diabetes Care. 1989, vol. 12, 715–724.
- American Diabetes Association Diagnosis and classification of diabetes mellitus // Diabetes Care. 2007. Vol. 30, S42-S47.
- Diem P. Pathogenesis and treatment of diabetes secondary to chronic pancreatitis. In: Buchler M. W., Friess H., Uhl W., Malfertheiner P. (eds). Chronic Pancreatitis. Novel Concepts in Biology and Therapy. Berlin, Blackwell, 2002, 355–358 p.
- Angelopoulos N., Dervenis C., Goula A. et al. Endocrine pancreatic insufficiency in cronic pancreatitis // Pancreatology 2005, vol. 5, p. 122–131.
- Koizumi M., Yoshida Y., Abe N. Pancreatic diabetes in Japan // Pancreas 1998. Vol. 16, p. 385–391.
- YunFeng Cui, Andersen D. K. Pancreatogenic Diabetes: Special Considerations Management // Pancreatology. 2011, vol. 11, № 3, p. 279–294.
- Винокурова Л. В., Астафьева О. В. Взаимодействие экзокринной и эндокринной функций поджелудочной железы при хроническом алкогольном панкреатите // Эксперимент. и клиническая гастроэн. 2002, № 4, с. 58–60.
- Бондарь Т. П., Козинец Г. И. Лабораторно-клиническая диагностика сахарного диабета и его осложнений. М.: Изд. МИА. 2003. 87 с.
- Malka D., Hammel P., Sauvenet A. et al. Risk factors for diabetes mellitus in chronic pancreatitis // J. Gastroenterology. 2000, vol. 119, p. 1324–1332.
- Садоков В. А. Клиническое течение алкогольного панкреатита // Тер. архив. 2003, № 3, с. 45–48.
- Gasiorowska A., Orszulak-Michalak D., Kozlowska A., Malecka-Panas E. Elevatad lasting plasma level of islet amyloid polypeptide (IAPP) in chronic alcoholic pancreatitis (CAP) // Hepatogastroenterology. 2003, vol. 50 (49), p. 258–262.
- Wakasugi H., Funakoshi A., Iguchi H. Clinical assessment of pancreatic diabetes caused by chronic pancreatitis // J. Gastroenterol. 1998, vol. 33, p. 254–259.
- Севергина Э. С. Инсулинзависимый сахарный диабет — взгляд морфолога. М.: ВИДАР, 2002. 149 с.
- Spandens A., El-Salhy V., Suhr O. et al. Prevalence of gastrointestinal symptoms in young and middle — aged diabetic patients // Scandinavian J. of Gastroenteroliogy. 1999, vol. 34, № 12, p. 1196–1202.
- Malka D., Hammel P., Sauvanet A. et al. Risk factors for diabetes mellitus in chronic pacreatitis // Gastroenterology. 2000, vol. 119, p. 1324–1332.
- Морозова Н. Н. Внешнесекреторная функция поджелудочной железы при начальных формах сахарного диабета // Клин. медицина. 1980, № 1, с. 69–72.
- Malka D., Levy Ph. Acinar-islet cell interactions: Diabetes mellitus in cronic pancreatitis. In: Johnson C. D., Imrie C. W. Pancretic disease: Basic science and clinical manfgement. London, 2004, 20, p. 251–266.
- Губергриц Н. Б., Казюлин А. Н. Метаболическая панкреатология. Донецк: «Лебедь», 2011. 460 с.
- Шустов С. Б., Халимов Ю. Ш., Баранов В. Л., Потин В. В. Эндокринология в таблицах и схемах. М.: МИА. 2009. 654 р.
- Пасечников В. Д. Может ли заместительная терапия при недостаточности экзокринной функции поджелудочной железы улучшить течение сахарного диабета // Клиническая гастроэнтерология и гепатология. Русское издание. 2011, т. 4, № 4, р. 196–198.
- Коротько Г. Ф. Рециркуляция ферментов пищеварительных желез. Краснодар, 2011. 143 с.
- Dominguez-Munoz J. Enrigue. Clinical Pancreatology for Practising Gastroenterologists and Surgeons. 2007. 535 р.
Л. В. Винокурова, доктор медицинских наук
И. С. Шулятьев, кандидат медицинских наук
Г. Г. Варванина, доктор медицинских наук
В. Н. Дроздов, доктор медицинских наук, профессор
ГУ ЦНИИ гастроэнтерологии Департамента здравоохранения города, Москва
Контактная информация об авторах для переписки: gastroenter@rambler.ru
Купить номер с этой статьей в pdf
Источник