Гистологическая верификация поджелудочной железы
Постановка
диагноза рака поджелудочной железы без
использования современных методов
диагностики (ультразвуковая томография,
компьютерная томография, магнито-резонансная
томография, ангиография) невозможна.Первые
клинические симптомы возникают достаточно
поздно и, зачастую, при далеко зашедшем
опухолевом процессе.
Поджелудочная
железа анатомически делится на головку,
тело и хвост. При локализации опухоли
в головке поджелудочной железы первым
симптомом заболевания, как правило,
является стойкая механическая желтуха,
причина которой — распространение
опухоли на желчные протоки. Это грозное
состояние, которое требует немедленных
лечебных мероприятий для его купирования.
Раньше единственным способом для
разгрузки желчных протоков являлась
полостная операция с созданием обходного
соустья между желчными протоками и
кишечником. В настоящее время, с развитием
новой высокотехнологичной специальности
— рентгено-эндохирургии — предпочтение
отдается методикам, позволяющим
произвести отток желчи из печени без
открытых полостных вмешательств.
При
обследовании пациента с объемным
образованием в поджелудочной железе
врач должен решить многочисленные
диагностические задачи. Значительные
диагностические трудности возникают
при определении характера поражения
поджелудочной железы. Даже в
специализированных центрах, обладающих
всеми современными диагностическими
возможностями, не всегда удается сделать
однозначный вывод о характере поражения
поджелудочной железы. Наиболее сложно
отличить рак поджелудочной железы от
псевдоопухолевого панкреатита.
Инструментальные
методы обследования, используемые для
диагностики рака органов панкреатодуоденальной
зоны (ПДЗ), в т. ч. и опухолей поджелудочной
железы, подразделяют на неинвазивные
и инвазивные. К первым относятся
рентгенологическое исследование желудка
и двенадцатиперстной кишки (дуоденография),
ультразвуковая вычислительная томография
(УЗТ), рентгеновская компьютерная
томография (КТ), сцинтиграфия поджелудочной
железы (СцГ), к инвазивным — эндоскопическая
ретроградная холангиопанкреатография
(ЭРХПГ), селективная артериография (АГ),
чреспеченочная портография (ЧПГ),
чрескожная чреспеченочная холангиография
(ЧЧПХ) и лапароскопия (ЛС). В последние
годы большое внимание уделяется
чрескожной прицельной биопсии (аспирации)
поджелудочной железы под контролем УЗТ
или КТ (ЧПБ). Использование столь обширного
арсенала инструментальных методов
обследования указывает на отсутствие
единого информативного метода и
свидетельствует о чрезвычайной сложности
дифференциальной диагностики опухолей
этой локализации. Каждый из этих методов
имеет свою разрешающую способность и
диагностическую значимость, однако
только их сочетание позволяет решить
вопросы топической и уточняющей
диагностики, дооперационной морфологической
верификации опухолевого процесса и тем
самым выработать адекватную тактику
лечения больных раком органов ПДЗ.
Рентгенологическое
исследованиежелудка и двенадцатиперстной
кишки (дуоденография) остается наиболее
доступным методом обследования больных
при подозрении на опухоль поджелудочной
железы, однако традиционное его
использование имеет сравнительно низкую
разрешающую способность (точность
метода не превышает 26%) и позволяет
выявлять лишь опухоли больших размеров.
Разрешающая способность метода повысилась
при сочетании дуоденографии с гипотонией
и использовании чресзондовой дуоденографии.
При
поражении головки поджелудочной железы
косвенные признаки могут проявляться
в виде деформации антрального отдела
желудка за счет вдавления опухолью его
задней стенки или большой кривизны,
деформации и щелевидного сужения
различной степени выраженности медиальной
стенки луковицы, горизонтального и
вертикального отделов двенадцатиперстной
кишки. При локализации опухоли в теле
поджелудочной железы можно видеть
вдавление задней стенки или большой
кривизны тела желудка, а при опухоли
хвоста поджелудочной железы – вдавление
свода желудка.
При прорастании
опухолью головки поджелудочной железы
стенки двенадцатиперстной кишки на
фоне вдавления определяется участок
характерной опухолевой инфильтрации
в виде неподвижности слизистой, изменения
ее цвета и структуры поверхности, которая
становится тусклой, мелкобугристой,
легко кровоточит и фрагментируется при
проведении биопсии. Нередко на фоне
инфильтрации выявляется изъязвление
с плотным неровным дном, покрытым
некротическим налетом. Решающим этапом
диагностики является прицельная биопсия
и взятие мазков-отпечатков с биоптатов
для гистологической и цитологической
верификации диагноза.
При
раке тела и хвоста участок прорастания
может выявляться на фоне вдавления
стенки или без явного его проявления.
Визуально прорастание определяется
либо в виде изъязвления с плотным
неровным дном и инфильтрированными
краями, либо в виде уплощенных экзофитных
разрастаний, либо в виде сочетания
экзофитных компонентов с язвенным
дефектом.
Рентгенологическая
семиотика рака поджелудочной железы
Рентгенологические признаки рака
поджелудочной железы могут проявляться
в виде изменений в различных отделах
главного или боковых панкреатических
протоков или в паренхиме железы в
зависимости от локализации опухоли в
головке, теле или хвосте поджелудочной
железы, а также сдавления или прорастания
общего желчного протока при локализации
опухоли в головке железы. Можно выделить
ряд основных рентгенологических
признаков рака поджелудочной
железы:
•обструкция главного
панкреатического протока,
•ограниченный
стеноз главного панкреатического
протока,
•протяженное
сужение главного панкреатического
протока,
•изменение ветвей
главного панкреатического
протока,
•очаговые изменения
в паренхиме поджелудочной железы.
При раке головки поджелудочной
железы, который в подавляющем большинстве
случаев сопровождается механической
желтухой, патогномоничным рентгенолоическим
признаком является сужение просвета
внепеченочных желчных протоков различной
степени выраженности вплоть до полного
блока за счет сдавления или прорастания
их опухолью. Наиболее часто поражается
общий желчный проток, однако при
значительном распространении опухоли
изменения могут локализоваться и на
уровне общего печеночного протока. В
ряде случаев при опухоли, исходящей из
краевых отделов головки поджелудочной
железы, основные изменения на
панкреатохолангиограммах выявляются
в желчных протоках при минимальном
поражении протока поджелудочной
железы.
При обструктивном
типе на панкреатограммах выявляется
полный блок главного панкреатического
протока на различном расстоянии от
устья в зависимости от локализации
опухоли. Характерной для опухолевого
поражения является конусовидная,
скошенная или булавовидно расширенная
культя, а также нитевидное сужение
культи протока (симптом «крысиного
хвоста»).
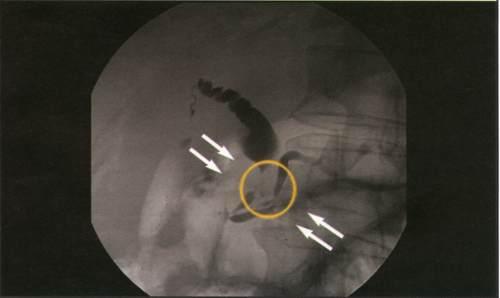
Панкреатохолангиограмма.
Рак головки поджелудочной железы.
Стенозирующий тип.
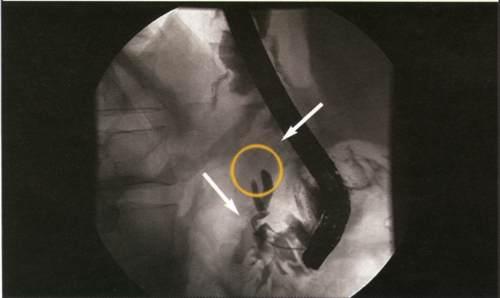
Панкреатохолангиограмма.
Рак головки поджелудочной железы.
Обструктивный тип. Полный блок главного
панкреатического и общего желчного
протоков.
Сцинтиграфия
(СцГ)
с использованием методики двухиндикаторного
исследования с 75Sе-метионином с 198Au
позволяет получить изображение нормальной
поджелудочной железы в 53—97% случаев.
Диагностика опухоли поджелудочной
железы основана на выявлении очаговых
дефектов накопления индикатора или
значительном снижении радиоактивности
в зоне опухоли. Возможности метода
ограничены отсутствием критериев
различия между СцГ картиной опухоли и
хронического панкреатита или кисты ПЖ,
в связи с чем в 30% случаев диагноз РПЖ
является ложноположительным.
Диагностическая точность метода
составляет 64%, причем разрешающая
способность самых современных аппаратов
— опухоли 3 и более см в диаметре.
Ангиосцинтиграфия, в связи с анатомическими
особенностями кровоснабжения железы,
не улучшает результаты метода. Несмотря
на малую чувствительность СцГ при
опухолях ПЖ, высокая ее специфичность
может быть использована в качестве
скрининга, т. к. неизмененная
сцинтиграфическая картина поджелудочной
железы с высокой степенью надежности
свидетельствует об отсутствии в ней
патологических изменений.
Ультразвуковая
вычислительная томография (УЗТ)
является приоритетным методом в
диагностике заболеваний поджелудочной
железы, печени, желчных протоков и
желчного пузыря. Нормальную поджелудочную
железу можно визуализировать с помощью
УЗТ в 80% наблюдений. Метод может быть
использован для скрининига РПЖ и
определения группы повышенного риска
развития рака органов ПДЗ. Чувствительность
УЗТ при РПЖ составляет 83—93%, специфичность
— 81—99%, точность около 84%. УЗТ позволяет
выявлять опухоли поджелудочной железы
размерами 2-3 см. К основным ультразвуковым
признакам опухоли ПЖ относятся наличие
объемного образования с неровными,
бугристыми контурами и пониженной
эхогенностью. Косвенными признаками
могут служить увеличение и деформация
железы, признаки механической желтухи
(расширение внутрипеченочных и
внепеченочных желчных протоков, желчного
пузыря), а также расширение протока
поджелудочной железы. В настоящее время
предложен метод, эндоскопической УЗТ
(ЭУЗТ) поджелудочной железы. Перспективным
направлением в диагностике РПЖ является
также интраоперационная УЗТ.
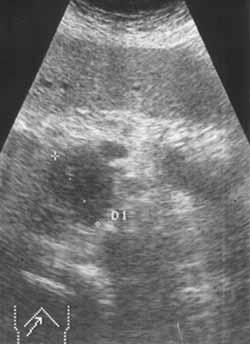
Рак
головки поджелудочной железы. В головке
определяется бугристое образование
сниженной эхогенности. Вирсунгов проток
расширен до 7 мм.
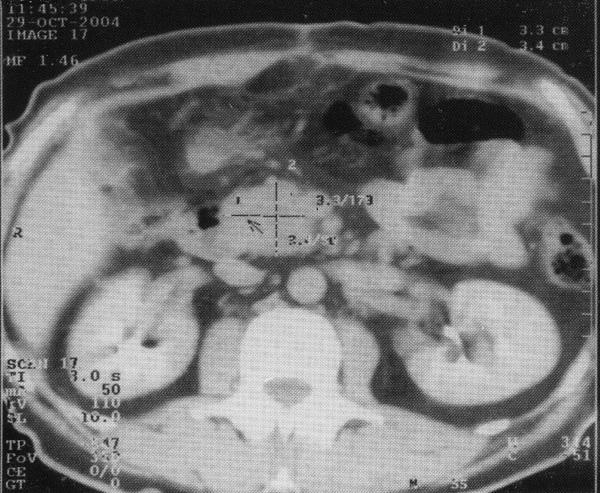
Компьютерная
рентгеновская томография (КТ)
нашла применение в дифференциальной
диагностике опухолей органов ПДЗ.
Преимуществом метода является его
неинвазивность и возможность визуализации
органов. К прямым признакам опухолевого
поражения ПЖ относятся увеличение
размеров, нечеткость контуров и деформация
пораженного участка железы, негомогенность
его структуры и инфильтрация
перипанкреатической клетчатки, сосудов,
стенки двенадцатиперстной кишки.
Косвенными признаками служат расширение
желчных протоков, увеличение желчного
пузыря, наличие асцита, метастазов в
печени и забрюшинных лимфатических
узлах. При опухолях менее 3 см КТ
малоинформативна, что обусловлено
отсутствием различий в относительной
плотности опухолевой ткани и паренхимы
ПЖ. Информативность метода достигает
82—100% при РПЖ III—IV ст. В отличие от
солидных опухолей, цистаденомы и кисты
поджелудочной железы хорошо визуализируются
с помощью КТ.
Магнитно-резонансная
томография
(МРТ)
является методикой с высокой разрешающей
способностью при опухолях поджелудочной
железы. При анализе результатов этого
исследования опытный специалист может
сделать вывод не только о распространенности
опухолевого процесса и связи его с
магистральными сосудами, но и предположить
гистологическую структуру новообразования.
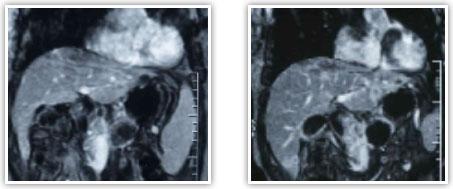
МРТ
в Т1 с контрастированием гадолинием 48
летнего пациента с раком поджелудочной
железы до и после лечения.
При
выявлении новообразований поджелудочной
железы используется также
позитронно-эмисионная
томография
К рисунку ПЭР:
Применение позитронной эмиссионной
томографии при раке поджедлудочной
железы. Множественные очаги гиперфиксации
18F-ФДГ у пациента с аденокарциномой
головки поджелудочной железы и метастазами
опухоли (фронтальные срезы).
Слева.
Срез на уровне головки поджелудочной
железы. Стрелками отмечены опухоль
головки ПЖ (нижний очаг) и два метастаза
в печени.
Справа.
Срез на уровне почки. Стрелками отмечены
три метастаза в печени и метастаз в
надключичный лимфатический узел.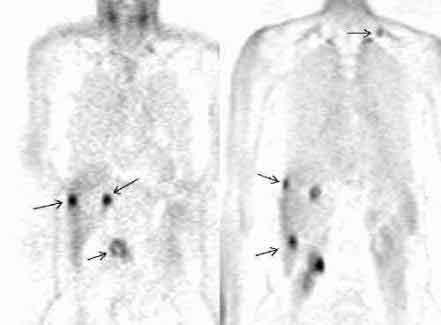
Заключение
Морфологическая
верификация диагноза рака ПЖ представляет
большие трудности. Поэтому при
диагностировании опухоли поджелудочной
железы часто недостаточно применения
одного метода лучевой диагностики.
Только комплексное обследование с
использованием всего современного
диагностического арсенала, включая
определение опухолевых маркеров СА-19-9
и РЭА, может позволить установить
правильный диагноз.
Список
использованной литературы
1.
Блохин Н.Н., Итин А.Б., Клименков А.А. Рак
поджелудочной железы и внепеченочных
желчных путей. — М.: Медицина, 1982.
2.
Габуния Р.И., Колесникова Е.К.. Компьютерная
томография в клинической диагностике.
— М. Медицина, 1995.
3.Гарин
А.М., Базин И.С. Злокачественные опухоли
пищеварительной системы. М., 2003; 171–236.
4.
Сафиуллин Р.Р. Роль комплексной лучевой
диагностики при новообразованиях
поджелудочной железы / Р.Р.Сафиуллин //
Тез. докл. научно-практ. конференции
молодых ученых. – Казань, 2004. – С. 85-86.
5.
Тодуа Ф.И., Федоров В.Д.,.Кузин М.И.
Компьютерная томография органов брюшной
полости. — М. Медицина, 1991.
Соседние файлы в предмете Лучевая диагностика
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
В.Г.Неустроев1, А.А.Владимирова2, Е.В.Казакова2, А.Н.Кыштымова3 Я.С.Петрова3,
1 – заведующий отделом эндоскопии ОГАУЗ Иркутский областной диагностический центр
2 – врач-эндоскопист отдела эндоскопии ОГАУЗ Иркутский областной диагностический центр
3 – врач-цитолог отдела патоморфологии ОГАУЗ Иркутский областной диагностический центр
г.Иркутск
Актуальность проблемы: По данным Ю.И.Патютко и А.Г.Котельникова рак головки поджелудочной железы (ПЖ) составляет 59-87% опухолей ПЖ [1]. Ввиду сложности диагностики и неспецифичности проявлений в 60-90% случаев механическая желтуха является первым симптомом заболевания [2]. С точностью от 94 до 100% ЭУС панкреато-билиарной зоны позволяет установить диагноз, оценить местную распространенность процесса, перспективы радикального оперативного лечения и возможные особенности выполнения ЭРХПГ и стентирования холедоха с целью разрешения желтухи [3]. По данным разных авторов разные способов морфологической верификации диагноза имеют разную чувствительность: браш-биопсия из холедоха 50-73,9%, внутрипротоковая биопсия 42,8-53,4%, комбинация биопсии и браш-биопсии 53,7-64,8%, тонкоигольная пункция под ЭУС-контролем 72,1-94% [4-7].
Материалы и методы: В исследование включены 333 пациента (с 2004 по 2014 гг.), которым выполнялось и ЭУС панкреато-билиарной зоны, и ЭРХПГ с целью дренирования холедоха и разрешения желтухи. Успешность стентирования возросла с накоплением опыта и в среднем составила 78,9 % (263/333): до 2011 — 76,9% (110/143); в 2012 — 78,3% (47/60); в 2013 — 81,4% (57/70); в 2014 — 87,5% (49/56).
У 100 пациентов во время ЭРХПГ по разным причинам не проводились попытки браш-биопсии из холедоха (явное прорастание опухоли в просвет ЖКТ, опухолевый стеноз ДПК, ранее установленный морфологический диагноз).
Оценка эффективности браш-биопсии проводилась в группе из 233 пациентов, у 46 из которых она была дополнена биопсией и мазками-отпечатками из места предполагаемого по ЭУС прорастания опухоли в стенку ДПК.
Для взятия браш-биопсии использовались цитологические щетки Olympus и MTW.
Чувствительность браш-биопсии из холедоха и комбинации браш-биопсии и биопсии из участков, подозрительных на прорастание (2004-2014, N=233) представлена в таблице №1.
Таблица №1. Чувствительность браш-биопсии из холедоха и комбинации браш-биопсии и биопсии из участков слизистой ДПК, подозрительных на прорастание опухоли головки поджелудочной железы (по годам).
2003- 2011г. | 2012г. | 2013г. | 2014г. | |
Браш-биопсия | 60,4 | 73,5 | 67,3 | 74,3 |
Браш-биопсия + биопсия | 62,5 | 79,6 | 73,1 | 82,9 |
Обсуждение: Наиболее точным на сегодняшний день малоинвазивным методом морфологической верификации очагового образования ПЖ является тонкоигольная пункция под контролем ЭУС. Оправданность применения этой методики при обнаружении очагового образования в паренхиме железы, не сопровождающегося механической желтухой, не подлежит сомнению. Однако, при развитии механической желтухи на первый план выступает необходимость дренирование холедоха (временного или окончательного). Комбинация ЭУС и ЭРХПГ позволяет установить диагноз (в том числе с морфологическим подтверждением); определить предполагаемую хирургическую тактику по распространенности процесса и дренировать холедох (временно или окончательно).
Мы считаем, что проведение браш-биопсии из холедоха и биопсии из предполагаемого прорастания опухоли в ДПК имеет преимущества, так как проводятся параллельно устранению механической желтухи, минимально инвазивны, более доступны и проще выполнимы, чем пункция под контролем ЭУС, клинически и экономически целесообразны, достаточно информативны.
С накоплением опыта возрастает и успешность стентирования, и результативность морфологической верификации диагноза. На наш взгляд, повысить результативность браш-биопсии позволили некоторые технические особенности и приемы. Щетки обязательно проводились за область стриктуры не менее 2 раз, при этом инструмент проводился по проводнику или рядом с ним. Мы выполняли не менее 10 пассов на уровне стриктуры, при этом отметили, что лучше «собирают» клеточный материал более «пушистые» щетки с более жесткими щетинками.
Все вышесказанное позволило сформулировать алгоритм, принятый в отделе эндоскопии ИОДЦ при обнаружении очагового образования ПЖ, подозрительного в отношении рака.
При выявлении на ЭУС очага в головке ПЖ, сопровождающегося механической желтухой и подозрительного в отношении рака, выполняем ЭРХПГ с попыткой стентирования и браш-биопсией из холедоха. При подозрении на прорастание стенки ДПК (по результатам ЭУС) дополнительно берем биопсию и мазки-отпечатки из предполагаемого места прорастания. При наличии очага в головке ПЖ с механической желтухой и отсутствии подтверждения диагноза после ЭРХПГ с браш-биопсией проводим пункцию очага под ЭУС-контролем.
Выводы:
- Для морфологического подтверждения диагноза необходимо применение всех доступных методов диагностики в определенной последовательности.
- В случае развития механической желтухи после диагностической ЭУС наиболее целесообразна попытка проведения ЭРХПГ с ЭПСТ, браш-биопсией из холедоха, стентированием холедоха.
- В случае подозрения на прорастание опухолью стенки ДПК (по результатам ЭУС) высокой информативностью обладает «лестничная» биопсия, выполненная с помощью дуоденоскопа.
- В случае отсутствия подтверждения диагноза после стентирования и браш-биопсии, а также при очаговых новообразованиях ПЖ без желтухи показана пункция под ЭУС-контролем.
- Точность морфологического диагноза возрастает при накоплении опыта всеми участниками процесса.
Список литературы
- Ю.И.Патютко, А.Г.Котельников Хирургия рака органов билиопанкреатодуоденальной зоны. – М.: ОАО «Издательство «Медицина», – 2007 . – 448 с.
- Kalsen, M.H. Pancreatic cancer-assessment of prognosis by clinical presentation / M.H. Kalsen, J.M. MacIntyre, J. Barkin // Castr. – 1983. – 84. – P.1202.
- ЭУСбука: Руководство по эндоскопической ультрасонографии. – М.: Практическая медицина, 2013. – 400 с.
- A prospective, comparative trial to optimize sampling techniques in EUS-guided FNA of solid pancreatic masses / J. K. Lee [et all.] // GASTROINTESTINAL ENDOSCOPY, 2013. — V.77, No. 5, — P. 745-751.
- https://www.usendoscopy.com/~/media/Files/Documents/Poster/Diehl-Infinity-Poster-2013.pdf
- EUS-FNA is superior to ERCP-based tissue sampling in suspected malignant biliary obstruction: results of a prospective, single-blind, comparative study / F. Weilert [et all.] // GASTROINTESTINAL ENDOSCOPY, 2014. — V.80, No. 1, — P. 97-104.
- Comparative effectiveness of biliary brush cytology and intraductal biopsy for detection of malignant biliary strictures: a systematic review and meta-analysis / U.Navaneethan [et all.] // GASTROINTESTINAL ENDOSCOPY, 2015. — V.81, No. 1, — P. 168-176.
Источник

