Гормоны островки поджелудочной железы
Оглавление темы «Гормон околощитовидных желез. Гормоны эпифиза. Гормоны поджелудочной железы. Гормоны половых желез. Гормоны тимуса.»: Гормоны поджелудочной железы. Островки Лангерганса. Соматостатин. Амилин. Регуляторные функции гормонов поджелудочной железы.Эндокринную функцию в поджелудочной железе выполняют скопления клеток эпителиального происхождения, получившие название островков Лангерганса и составляющие всего 1 —2 % массы поджелудочной железы — экзокринного органа, образующего панкреатический пищеварительный сок. Количество островков в железе взрослого человека очень велико и составляет от 200 тысяч до полутора миллионов. В островках различают несколько типов клеток, продуцирующих гормоны: альфа-клетки образуют глюкагон, бета-клетки — инсулин, дельта-клетки — соматостатин, джи-клетки — гастрин и РР- или F-клетки — панкреатический полипептид. Помимо инсулина в бета-клетках синтезируется гормон амилин, обладающий противоположными инсулину эффектами. Кровоснабжение островков более интенсивно, чем основной паренхимы железы. Иннервация осуществляется постганлионарными симпатическими и парасимпатическими нервами, причем среди клеток островков расположены нервные клетки, образующие нейроинсулярные комплексы.
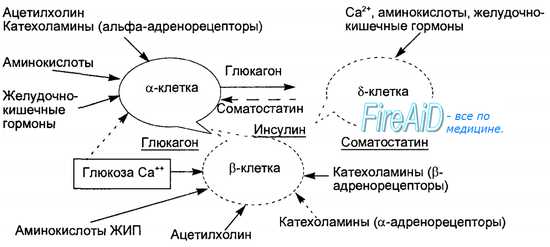
Инсулин синтезируется в эндоплазматическом ретикулуме бета-клеток вначале в виде пре-проинсулина, затем от него отщепляется 23-аминокис-лотная цепь и остающаяся молекула носит название проинсулина. В комплексе Гольджи проинсулин упаковывается в гранулы, в них осуществляется расщепление проинсулина на инсулин и соединительный пептид (С-пептид). В гранулах инсулин депонируется в виде полимера и частично в комплексе с цинком. Количество депонированного в гранулах инсулина почти в 10 раз превышает суточную потребность в гормоне. Секреция инсулина происходит путем экзоцитоза гранул, при этом в кровь поступает эквимолярное количество инсулина и С-пептида. Определение содержания последнего в крови является важным диагностическим тестом оценки секреторной способности (3-клеток. Секреция инсулина является кальцийзависимым процессом. Под влиянием стимула — повышенного уровня глюкозы в крови — мембрана бета-клеток деполяризуется, ионы кальция входят в клетки, что запускает процесс сокращения внутриклеточной микротубулярной системы и перемещение гранул к плазматической мембране с последующим их экзоцитозом. Секреторная функция разных клеток островков взаимосвязана, зависит от эффектов образуемых ими гормонов, в связи с чем островки рассматриваются как своеобразный «мини-орган» (рис. 6.21). Выделяют два вида секреции инсулина: базальную и стимулированную. Базальная секреция инсулина осуществляется постоянно, даже при голодании и уровне глюкозы крови ниже 4 ммоль/л. Стимулированная секреция инсулина представляет собой ответ бета-клеток островков на повышенный уровень D-глюкозы в притекающей к бета-клеткам крови. Под влиянием глюкозы активируется энергетический рецептор бета-клеток, что увеличивает транспорт в клетку ионов кальция, активирует аденилатциклазу и пул (фонд) цАМФ. Через эти посредники глюкоза стимулирует выброс инсулина в кровь из специфических секреторных гранул. Усиливает ответ бета-клеток на действие глюкозы гормон двенадцатиперстной кишки — желудочный ингибиторный пептид (ЖИП). В регуляции секреции инсулина определенную роль играет и вегетативная нервная система. Блуждающий нерв и ацетилхолин стимулируют секрецию инсулина, а симпатические нервы и норадреналин через альфа-адренорецепторы подавляют секрецию инсулина и стимулируют выброс глюкагона. Специфическим ингибитором продукции инсулина является гормон дельта-клеток островков — соматостатин. Этот гормон образуется и в кишечнике, где тормозит всасывание глюкозы и тем самым уменьшает ответную реакцию бета-клеток на глюкозный стимул. Образование в поджелудочной железе и кишечнике пептидов, аналогичных мосговым, например сомато-статина, подтверждает существование в организме единой APUD-системы. Секреция глюкагона стимулируется снижением уровня глюкозы в крови, гормонами желудочно-кишечного тракта (ЖИП гастрин, секретин, холе-цистокинин-панкреозимин) и при уменьшении в крови ионов Са2+. Подавляют секрецию глюкагона инсулин, соматостатин, глюкоза крови и Са2+. В эндокринных клетках кишечника образуется глюкагоноподобный пептид-1, стимулирующий всасывание глюкозы и секрецию инсулина после приема пищи. Клетки желудочно-кишечного тракта, продуцирующие гормоны, являются своеобразными «приборами раннего оповещения» клеток панкреатических островков о поступлении пищевых веществ в организм, требующих для утилизации и распределения участия панкреатических гормонов. Эта функциональная взаимосвязь нашла отражение в термине «гастро-энтеро-панкреатическая система». — Также рекомендуем «Инсулин. Физиологические эффекты инсулина. Схема транспорта глюкозы через клеточные мембраны. Основные эффекты инсулина.» |
Источник
 В 19 веке молодой ученый из Германии обнаружил неоднородность тканей поджелудочной железы. Клетки, отличавшиеся от основной массы, располагались небольшими скоплениями, островками. Группы клеток в дальнейшем назвали именем патологоанатома — островки Лангерганса (ОЛ).
В 19 веке молодой ученый из Германии обнаружил неоднородность тканей поджелудочной железы. Клетки, отличавшиеся от основной массы, располагались небольшими скоплениями, островками. Группы клеток в дальнейшем назвали именем патологоанатома — островки Лангерганса (ОЛ).
Их доля в общем объеме тканей составляет не более 1-2%, однако эта небольшая часть железы выполняет свою функцию, отличную от пищеварительной.
Предназначение островков Лангерганса
 Основная часть клеток поджелудочной железы (ПЖ) вырабатывает ферменты, способствующие пищеварению. Функция островных скоплений другая – они синтезируют гормоны, поэтому их относят к эндокринной системе.
Основная часть клеток поджелудочной железы (ПЖ) вырабатывает ферменты, способствующие пищеварению. Функция островных скоплений другая – они синтезируют гормоны, поэтому их относят к эндокринной системе.
Таким образом, поджелудочная железа является частью двух основных систем организма – пищеварительной и эндокринной. Островки являются микроорганами, вырабатывающими 5 видов гормонов.
Большая часть панкреатических групп расположены в хвостовой части поджелудочной железы, хотя хаотичные, мозаичные вкрапления захватывает всю экзокринную ткань.
ОЛ отвечают за регулирование углеводного обмена и поддерживают работу других эндокринных органов.
Гистологическое строение
Каждый островок представляет собой самостоятельно функционирующий элемент. Вместе они составляют сложный архипелаг, который составлен из отдельных клеток и более крупных образований. Размеры их значительно различаются – от одной эндокринной клетки до зрелого, крупного островка (>100 мкм).
В панкреатических группах выстроена иерархия расположения клеток, их 5 видов, все выполняют свою роль. Каждый островок окружен соединительной тканью, имеет дольки, где находятся капилляры.
В центре расположены группы бета-клеток, по краям образований – альфа и дельта-клетки. Чем больше размер островка, тем больше в нем периферийных клеток.
Островки не имеют протоков, вырабатываемые гормоны выводятся по системе капилляров.

Разновидности клеток
Разные группы клеток продуцируют свой вид гормона, регулируя пищеварение, липидный и углеводный обмен.
- Альфа-клетки. Эта группа ОЛ расположена по краю островков, их объем составляет 15-20% от общего размера. В них происходит синтез глюкагона – гормона, регулирующего количество глюкозы в крови.
- Бета-клетки. Группируются в центре островков и составляют большую часть их объема, 60- 80%. Они синтезируют инсулин, около 2 мг в сутки.
- Дельта-клетки. Отвечают за выработку соматостатина, их от 3 до 10%.
- Эпсилон-клетки. Количество от общей массы не более 1%. Их продукт – грелин.
- PP-клетки. Гормон панкреатический полипептид вырабатывается этой частью ОЛ. Составляют до 5% островков.
С течением жизни удельный вес эндокринной составляющей поджелудочной железы сокращается – от 6% в первые месяцы жизни до 1-2 % к 50-ти годам.
Гормональная активность
Гормональная роль поджелудочной железы велика.
Синтезированные в маленьких островках активные вещества током крови доставляются в органы и регулируют метаболизм углеводов:
- Основной задачей инсулина является минимизация уровня сахара в крови. Он увеличивает всасывание глюкозы клеточными оболочками, ускоряет ее окисление и помогает сохранению в виде гликогена. Нарушение синтеза гормона приводит к развитию диабета 1 типа. При этом анализы крови показывают наличие антител к вета-клеткам. Сахарный диабет 2 типа развивается, если снижается чувствительность тканей к инсулину.
- Глюкагон выполняет противоположную функцию – увеличивает уровень сахара, регулирует выработку глюкозы в печени, ускоряет расщепление липидов. Два гормона, дополняя действие друг друга, гармонируют содержание глюкозы – вещества, обеспечивающего жизнедеятельность организма на клеточном уровне.
- Соматостатин замедляет действие многих гормонов. При этом происходит снижение скорости всасывания сахара из пищи, уменьшение синтеза пищеварительных ферментов, снижение количества глюкагона.
- Панкреатический полипептид снижает количество ферментов, замедляет выброс желчи и билирубина. Считается, что он останавливает расход пищеварительных ферментов, сохраняя их до очередного приема пищи.
- Грелин считается гормоном голода или сытости. Его выработка дает сигнал организму о чувстве голода.
Количество вырабатываемых гормонов зависит от полученной с пищей глюкозы и скорости ее окисления. При увеличении ее количества выработка инсулина увеличивается. Синтез запускается при концентрации 5,5 ммоль/л в плазме крови.
Спровоцировать выработку инсулина может не только прием пищи. У здорового человека максимальная концентрация отмечается в период сильных физических напряжений, стрессов.
Эндокринная часть ПЖ вырабатывает гормоны, которые оказывают решающее влияние на весь организм. Патологические изменения ОЛ способны нарушить работу всех органов.
Видео о задачах инсулина в организме человека:
Поражение эндокринной части поджелудочной железы и ее лечение
Причиной поражения ОЛ могут быть генетическая предрасположенность, инфекции и отравления, воспалительные заболевания, иммунные проблемы.
В результате происходит прекращение или значительное снижение выработки гормонов разными клетками островков.
В результате этого могут развиться:
- СД 1 типа. Характеризуется отсутствием или дефицитом инсулина.
- СД 2 типа. Определяется неспособностью организма воспользоваться выработанным гормоном.
- Гестационный диабет развивается во время беременности.
- Другие типы сахарного диабета (MODY).
- Нейроэндокринные опухоли.
Основные принципы лечения сахарного диабета 1 типа заключаются во введение в организм инсулина, выработка которого нарушена или снижена. Применяют два вида инсулинов – быстрый и длительного действия. Последний вид имитирует выработку гормона ПЖ.
 СД 2 типа требует строгого соблюдения диеты, умеренных физических упражнений и приема препаратов, способствующих сжиганию сахара.
СД 2 типа требует строгого соблюдения диеты, умеренных физических упражнений и приема препаратов, способствующих сжиганию сахара.
Во всем мире наблюдается рост заболеваемости диабетом, его уже называют чумой 21 века. Поэтому медицинские исследовательские центры ищут способы борьбы с заболеваниями островков Лангерганса.
Процессы в поджелудочной железе развиваются быстро и приводят к отмиранию островков, которые должны синтезировать гормоны.
В последние годы стало известно:
- стволовые клетки, пересаженные на ткань ПЖ, хорошо приживаются и способны в дальнейшем продуцировать гормон, так как начинают работать как бета-клетки;
- ОЛ вырабатывают больше гормонов, если удалить часть железистой ткани ПЖ.
Это позволяет пациентам отказаться от постоянного приема лекарственных средств, строгой диеты и вернуть нормальный образ жизни. Проблемой остается иммунная система, которая может отторгнуть подсаженные клетки.
Еще одним возможным способом лечения рассматривается пересадка от донора части островковой ткани. Этот способ заменяет установку искусственной ПЖ или ее полную пересадку от донора. При этом удается остановить прогрессирование заболевания и нормализовать глюкозу в крови.
Проведены успешные операции, после которых у больных с диабетом 1 типа отпала необходимость во введении инсулина. Орган восстановил популяцию бета-клеток, синтез собственного инсулина возобновился. После операции была проведена иммуносупрессивная терапия, чтобы не допустить отторжения.
Видео-материал о функциях глюкозы и заболевании диабетом:
Медицинские институты работают над изучением возможности пересадки поджелудочной железы от свиньи. Первые средства для лечения сахарного диабета как раз использовали части поджелудочной железы свиней.
Ученые сходятся на том, что необходимы исследования особенностей строения и работы островков Лангерганса из-за большого количества важных функций, которые выполняют синтезируемые в них гормоны.
Постоянный прием искусственных гормонов не помогает победить болезнь и ухудшает качество жизни пациента. Поражение этой маленькой части ПЖ вызывает глубокие нарушения работы всего организма, поэтому исследования продолжаются.
Источник
Поджелудочная железа относится к железам со смешанной секрецией. Внешнесекреторная функция ее заключается в синтезе ряда ключевых ферментов пищеварения, в частности амилазы, липазы, трипсина, химо-трипсина, карбоксипептидазы и др., поступающих в кишечник с соком поджелудочной железы. Внутрисекреторную функцию выполняют, как было установлено в 1902 г. Л.В. Соболевым, панкреатические островки (островки Лангерганса), состоящие из клеток разного типа и вырабатывающие гормоны, как правило, противоположного действия. Так, α- (или А-) клетки продуцируют глюкагон, β- (или В-) клетки синтезируют инсулин, δ-(или D-) клетки вырабатывают соматостатин и F-клетки – малоизученный панкреатический полипептид. Далее будут рассмотрены инсулин и глюкагон как гормоны, имеющие исключительно важное значение для жизнедеятельности организма.
Инсулин. Инсулин, получивший свое название от наименования панкреатических островков (лат. insula – островок), был первым белком, первичная структура которого была раскрыта в 1954 г. Ф. Сэнджером. В чистом виде инсулин был получен в 1922 г. после его обнаружения в экстрактах панкреатических островков Ф. Бантингом и Ч. Бестом. Молекула инсулина, содержащая 51 аминокислотный остаток, состоит из двух полипептидных цепей, соединенных между собой в двух точках дисульфидными мостиками. В настоящее время принято обозначать цепью А инсулина 21-членный пептид и цепью В – пептид, содержащий 30 остатков аминокислот. Во многих лабораториях осуществлен, кроме того, химический синтез инсулина. Наиболее близким по своей структуре к инсулину человека является инсулин свиньи, у которого в цепи В вместо треонина в положении 30 содержится аланин.
Существенных различий в аминокислотной последовательности в инсулине от разных животных нет. Инсулины различаются аминокислотным составом цепи А в положениях 8–10.
Согласно современным представлениям, биосинтез инсулина осуществляется в β-клетках панкреатических островков из своего предшественника проинсулина, впервые выделенного Д. Стайнером в 1966 г. В настоящее время не только выяснена первичная структура проинсулина, но и осуществлен его химический синтез. Проинсулин представлен одной полипептидной цепью, содержащей 84 аминокислотных остатка; он лишен биологической, т.е. гормональной, активности.
Синтезированный из проинсулина инсулин может существовать в нескольких формах, различающихся по биологическим, иммунологическим и физико-химическим свойствам. Различают две формы инсулина: 1) свободную, вступающую во взаимодействие с антителами, полученными к кристаллическому инсулину, и стимулирующую усвоение глюкозы мышечной и жировой тканями; 2) связанную, не реагирующую с антителами и активную только в отношении жировой ткани.
В физиологической регуляции синтеза инсулина доминирующую роль играет концентрация глюкозы в крови. Так, повышение содержания глюкозы в крови вызывает увеличение секреции инсулина в панкреатических островках, а снижение ее содержания, наоборот,– замедление секреции инсулина. Этот феномен контроля по типу обратной связи рассматривается как один из важнейших механизмов регуляции содержания глюкозы в крови. На секрецию инсулина оказывают влияние, кроме того, электролиты (особенно ионы кальция), аминокислоты, глюкагон и секретин. Приводятся доказательства роли циклазной системы в секреции инсулина. Предполагают, что глюкоза действует в качестве сигнала для активирования аденилат-циклазы, а образовавшийся в этой системе цАМФ – в качестве сигнала для секреции инсулина.
При недостаточной секреции (точнее, недостаточном синтезе) инсулина развивается специфическое заболевание – сахарный диабет. Помимо клинически выявляемых симптомов (полиурия, полидипсия и полифагия), сахарный диабет характеризуется рядом специфических нарушений процессов обмена. Так, у больных развиваются гипергликемия (увеличение уровня глюкозы в крови) и гликозурия (выделение глюкозы с мочой, в которой в норме она отсутствует). К расстройствам обмена относят также усиленный распад гликогена в печени и мышцах, замедление биосинтеза белков и жиров, снижение скорости окисления глюкозы в тканях, развитие отрицательного азотистого баланса, увеличение содержания холестерина и других липидов в крови. При диабете усиливаются мобилизация жиров из депо, синтез углеводов из аминокислот (глюконеогенез) и избыточный синтез кетоновых тел (кетонурия). После введения больным инсулина все перечисленные нарушения, как правило, исчезают, однако действие гормона ограничено во времени, поэтому необходимо вводить его постоянно. Клинические симптомы и метаболические нарушения при сахарном диабете могут быть объяснены не только отсутствием синтеза инсулина. Получены доказательства, что при второй форме сахарного диабета, так называемой инсулинрезистентной, имеют место и молекулярные дефекты: в частности, нарушение структуры инсулина или нарушение ферментативного превращения проинсулина в инсулин. В основе развития этой формы диабета часто лежит потеря рецепторами клеток-мишеней способности соединяться с молекулой инсулина, синтез которого нарушен, или синтез мутантного рецептора.
У экспериментальных животных введение инсулина вызывает гипогликемию (снижение уровня глюкозы в крови), увеличение запасов гликогена в мышцах, усиление анаболических процессов, повышение скорости утилизации глюкозы в тканях. Кроме того, инсулин оказывает опосредованное влияние на водный и минеральный обмен.
Механизм действия инсулина окончательно не расшифрован, несмотря на огромное количество фактических данных, свидетельствующих о существовании тесной и прямой зависимости между инсулином и процессами обмена веществ в организме. В соответствии с «унитарной» теорией все эффекты инсулина вызваны его влиянием на обмен глюкозы через фермент гексокиназу. Новые экспериментальные данные свидетельствуют, что усиление и стимуляция инсулином таких процессов, как транспорт ионов и аминокислот, трансляция и синтез белка, экспрессия генов и др., являются независимыми. Это послужило основанием для предположения о множественных механизмах действия инсулина.
Глюкагон.Глюкагон впервые был обнаружен в коммерческих препаратах инсулина еще в 1923 г., однако только в 1953 г. венгерский биохимик Ф. Штрауб получил этот гормон в гомогенном состоянии. Глюкагон синтезируется в основном в α-клетках панкреатических островков поджелудочной железы, а также в ряде клеток кишечника. Он представлен одной линейно расположенной полипептидной цепью, в состав которой входит 29 аминокислотных остатков в следующей последовательности:
Н–Гис–Сер–Глн–Гли–Тре–Фен–Тре–Сер–Асп–Тир–Сер–Лиз–Тир–Лей– Асп–Сер–Aрг–Aрг–Ала–Глн–Асп–Фен–Вал–Глн–Трп–Лей–Мет–Асн––Тре–ОН
Первичная структура глюкагонов человека и животных оказалась идентичной; исключение составляет только глюкагон индюка, у которого вместо аспарагина в положении 28 содержится серин. Особенностью структуры глюкагона является отсутствие дисульфидных связей и цистеина. Глюкагон образуется из своего предшественника проглюкагона, содержащего на С-конце полипептида дополнительный октапептид (8 остатков). Имеются данные, что у проглюкагона, так же как и у проинсулина, существует предшественник – препроглюкагон (мол. масса 9000), структура которого пока не расшифрована.
По биологическому действию глюкагон, как и адреналин, относятся к гипергликемическим факторам, вызывает увеличение концентрации глюкозы в крови главным образом за счет распада гликогена в печени. Органами-мишенями для глюкагона являются печень, миокард, жировая ткань, но не скелетные мышцы. Биосинтез и секреция глюкагона контролируются главным образом концентрацией глюкозы по принципу обратной связи. Таким же свойством обладают аминокислоты и свободные жирные кислоты. На секрецию глюкагона оказывают влияние также инсулин и инсулиноподобные факторы роста.
Общим итогом действия глюкагона являются ускорение распада гликогена и торможение его синтеза в печени, что приводит к увеличению концентрации глюкозы в крови.
Гипергликемический эффект глюкагона обусловлен, однако, не только распадом гликогена. Имеются бесспорные доказательства существования глюконеогенетического механизма гипергликемии, вызванной глюкагоном. Установлено, что глюкагон способствует образованию глюкозы из промежуточных продуктов обмена белков и жиров. Глюкагон стимулирует образование глюкозы из аминокислот путем индукции синтеза ферментов глюконеогенеза при участии цАМФ, в частности фосфоенолпируваткарбок-сикилазы – ключевого фермента этого процесса. Глюкагон в отличие от адреналина тормозит гликолитический распад глюкозы до молочной кислоты, способствуя тем самым гипергликемии. Существуют и различия в физиологическом действии: в отличие от адреналина глюкагон не повышает кровяного давления и не увеличивает частоту сердечных сокращений. Следует отметить, что, помимо панкреатического глюкагона, в последнее время доказано существование кишечного глюкагона, синтезирующегося по всему пищеварительному тракту и поступающего в кровь. Первичная структура кишечного глюкагона пока точно не расшифрована. Таким образом, панкреатические островки, синтезирующие два противоположного действия гормона – инсулин и глюкагон, выполняют ключевую роль в регуляции обмена веществ на молекулярном уровне.
Источник