Гормоны поджелудочной железы инсулин и глюкагон регулируют обмен
Гормонами поджелудочной железы являются инсулин и глюкагон.
Глюкагон
Строение
Представляет собой полипептид, включающий 29 аминокислот с молекулярной массой 3,5 кДа и периодом полураспада 3-6 мин.
Синтез
Осуществляется в клетках поджелудочной железы и в клетках тонкого кишечника.
Регуляция синтеза и секреции
Активируют: гипогликемия, адреналин.
Уменьшают: глюкоза, жирные кислоты.
Механизм действия
Аденилатциклазный активирующий.
Мишени и эффекты
Конечным эффектом является повышение концентрации глюкозы и жирных кислот в крови.
Жировая ткань
- повышает активность внутриклеточной гормон-чувствительной ТАГ-липазы и, соответственно, стимулирует липолиз.
Печень
- активация глюконеогенеза и гликогенолиза,
- за счет повышенного поступления жирных кислот из жировой ткани усиливает кетогенез.
Патология
Гиперфункция
Глюкагонома – редко встречающееся новообразование из группы нейроэндокринных опухолей. У больных отмечается гипергликемия и поражение кожи и слизистых оболочек.
Инсулин
Дополнительная, более подробная информация, об инсулине находится на следующей странице.
Строение
Представляет собой полипептид из 51 аминокислоты, массой 5,7 кД, состоящий из двух цепей А и В, связанных между собой дисульфидными мостиками.
Синтез
Синтезируется в клетках поджелудочной железы в виде проинсулина, в этом виде он упаковывается в секреторные гранулы и уже здесь образуется инсулин и С-пептид.
Регуляция синтеза и секреции
Активируют синтез и секрецию:
- глюкоза крови – главный регулятор, пороговая концентрация для секреции инсулина – 5,5 ммоль/л,
- жирные кислоты и аминокислоты,
- влияния n.vagus – находится под контролем гипоталамуса, активность которого определяется концентрацией глюкозы крови,
- гормоны ЖКТ: холецистокинин, секретин, гастрин, энтероглюкагон, желудочный ингибирующий полипептид,
- хроническое воздействие гормона роста, глюкокортикоидов, эстрогенов, прогестинов.
Уменьшают: влияние симпато-адреналовой системы.
Механизм действия
Осуществляется через рецепторы с тирозинкиназной активностью (подробно).
Мишени и эффекты
Основным эффектом является снижение концентрации глюкозы в крови благодаря усилению транспорта глюкозы внутрь миоцитов и адипоцитов и активации внутриклеточных реакций утилизации глюкозы:
- активируя фосфодиэстеразу, которая разрушает вторичный мессенджер цАМФ, инсулин прерывает эффекты адреналина и глюкагона на печень и жировую ткань.
- в мышцах и жировой ткани стимулирует транспорт глюкозы в клетки (активация Глют-4),
- в печени и мышцах ускоряет синтез гликогена (активация гликогенсинтазы).
- в печени, мышцах и адипоцитах инсулин стимулирует гликолиз, активируя фосфофруктокиназу и пируваткиназу.
- полученный в гликолизе пируват превращается в ацетил-SКоА под влиянием активированного инсулином пируватдегидрогеназного комплекса, и далее используется для синтеза жирных кислот. Превращение ацетил-SКоА в малонил-SКоА, первый субстрат синтеза жирных кислот, также стимулируется инсулином (ацетил-SКоА-карбоксилаза).
- в мышцах усиливает транспорт нейтральных аминокислот в миоциты и стимулирует трансляцию (рибосомальный синтез белков).
Ряд эффектов инсулина заключается в изменении транскрипции генов и скорости трансляции ферментов, отвечающих за обмен веществ, за рост и деление клеток.
Благодаря этому индуцируется синтез ферментов метаболизма
- углеводов в печени (глюкокиназа, пируваткиназа, глюкозо-6-фосфатдегидрогеназа),
- липидов в печени (АТФ-цитрат-лиаза, ацетил-SКоА-карбоксилаза, синтаза жирных кислот, цитозольная малатдегидрогеназа) и адипоцитах (ГАФ-дегидрогеназа, пальмитатсинтаза, липопротеинлипаза).
и происходит репрессия фосфоенолпируват-карбоксикиназы (подавление глюконеогенеза).
Инактивация инсулина
Инактивация инсулина начинается после интернализации инсулин-рецепторного комплекса и образования эндосомы, в которой и происходит деградация инсулина. Участвуют две ферментные системы:
- Глутатион-инсулин-трансгидрогеназа, которая восстанавливает дисульфидные связи между цепями А и В, в результате чего гормон распадается.
- Инсулиназа (инсулин-протеиназа), гидролизующая инсулин до аминокислот.
Период полужизни инсулина не превышает 5-6 минут. Происходит деградация в основном в печени и почках, но и другие ткани принимают в этом участие. Также в почках инсулин может фильтроваться, захватываться эпителиоцитами проксимальных канальцев и разрушаться до аминокислот.
Патология
Гипофункция
Инсулинзависимый и инсулиннезависимый сахарный диабет. Для диагностики этих патологий в клинике активно используют нагрузочные пробы и определение концентрации инсулина и С-пептида.
Источник
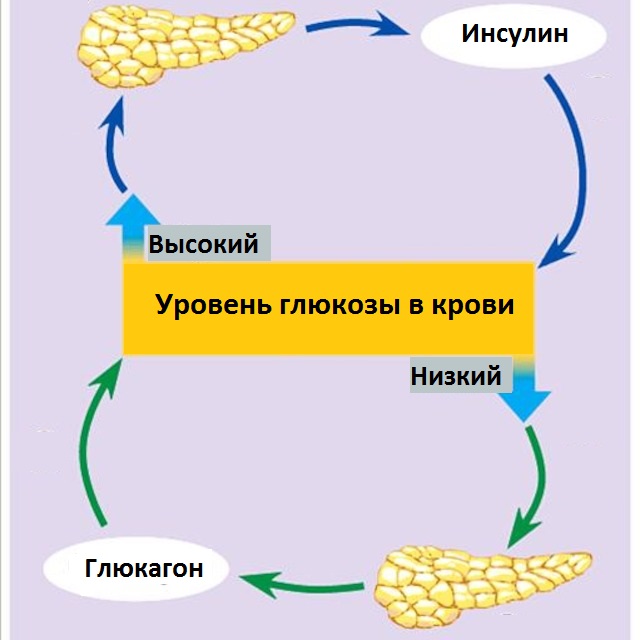
Глюкагон и инсулин – гормоны поджелудочной железы. Функция всех гормонов – регуляция обмена веществ в организме. Основная функция инсулина и глюкагона – обеспечение организма энергетическими субстратами после еды и в период голодания. После еды необходимо обеспечить поступление глюкозы в клетки и запасание ее излишков. В период голодания – извлечь глюкозу из резервов (гликогена) или синтезировать ее или другие энергетические субстраты.
Распространено мнение, что инсулин и глюкагон расщепляют углеводы. Это неверно. Обеспечивают расщепление веществ ферменты. Гормоны же регулируют эти процессы.
Синтез глюкагона и инсулина
Гормоны производятся в железах внутренней секреции. Инсулин и глюкагон — в поджелудочной железе: инсулин в β-клетках, глюкагон – в α-клетках островков Лангерганса. Оба гормона имеют белковую природу и синтезируются из предшественников. Инсулин и глюкагон выделяются в противоположных состояниях: инсулин при гипергликемии, глюкагон – при гипогликемии. Полупериод жизни инсулина — 3-4 минуты, его постоянная варьирующая секреция обеспечивает поддержание уровня глюкозы в крови в узких пределах.
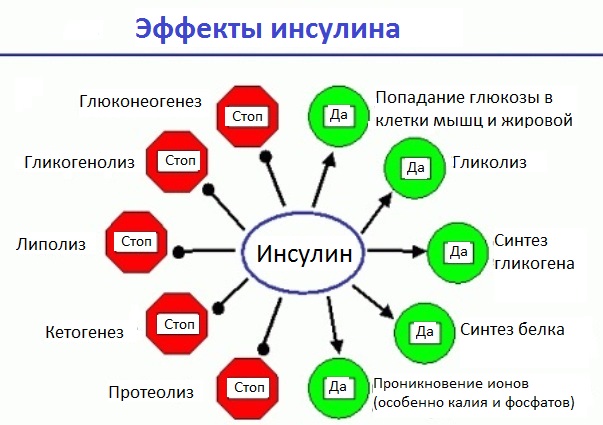
Эффекты инсулина
Инсулин регулирует обмен веществ, прежде всего – концентрацию глюкозы. Он влияет на мембранные и внутриклеточные процессы.
Мембранные эффекты инсулина:
- стимулирует транспорт глюкозы и ряда других моносахаридов,
- стимулирует транспорт аминокислот (главным образом аргинина),
- стимулирует транспорт жирных кислот,
- стимулирует поглощение клеткой ионов калия и магния.
Инсулин оказывает внутриклеточные эффекты:
- стимулирует синтез ДНК и РНК,
- стимулирует синтез белков,
- усиливает стимуляцию фермента гликогенсинтазы (обеспечивает синтез гликогена из глюкозы – гликогенез),
- стимулирует глюкокиназу (фермент способствующий превращению глюкозы в гликоген в условиях ее избытка),
- ингибирует глюкозо-6-фосфатазу (фермент, катализирующий превращение глюкозо-6-фосфата в свободную глюкозу и, соответственно, повышающий уровень сахара в крови),
- стимулирует липогенез,
- ингибирует липолиз (за счет торможения синтеза цАМФ),
- стимулирует синтез жирных кислот,
- активирует Na+/K+-АТФ-азу.
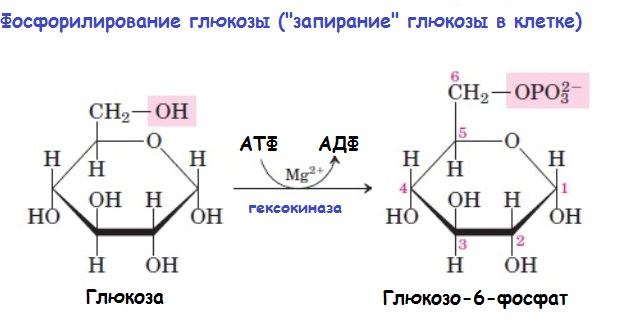
Роль инсулина в транспорте глюкозы в клетки
Глюкоза попадает в клетки с помощью специальных белков-транспортеров (GLUT). В разных клетках локализуются многочисленные GLUT. В мембранах клеток скелетных и сердечных мышц, жировой ткани, лейкоцитов, коркового слоя почек работают инсулинзависимые транспортеры – GLUT4. Транспортеры инсулина в мембранах клеток ЦНС, печени нсулиннезависимы, поэтому обеспечение клеток этих тканей глюкозой зависит только от ее концентрации в крови. В клетки почек, кишечника, эритроцитов глюкоза попадает вообще без переносчиков, путем пассивной диффузии. Таким образом, инсулин необходим для попадания глюкозы в клетки жировой ткани, скелетных мышц и сердечных мышц. При недостатке инсулина в клетки этих тканей попадет лишь небольшое количество глюкозы, недостаточное для обеспечения их метаболических потребностей, даже в условиях высокой концентрации глюкозы в крови (гипергликемии).
Роль инсулина в обмене глюкозы
Инсулин стимулирует утилизацию глюкозы, включая несколько механизмов.
- Повышает активность гликогенсинтазы в клетках печени, стимулируя синтез гликогена из остатков глюкозы.
- Повышает активность глюкокиназы в печени, стимулируя фосфорилирование глюкозы с образованием глюкозо-6-фосфата, который «запирает» глюкозу в клетке, т. к. не способен проходить через мембрану из клетки в межклеточное пространство.
- Ингибирует фосфатазу печени, катализирующую обратное превращение глюкозо-6-фосфата в свободную глюкозу.
Все перечисленные процессы обеспечивают поглощение глюкозы клетками периферических тканей и снижение ее синтеза, что приводит к снижению концентрации глюкозы в крови. Кроме того, усиление утилизации глюкозы клетками сохраняет запасы других внутриклеточных энергетических субстратов – жиров и белков.
Роль инсулина в обмене белков
Инсулин стимулирует как транспорт свободных аминокислот в клетки, так и синтез белка в них. Синтез белка стимулируется двумя путями:
- за счет активации мРНК,
- за счет увеличения поступления аминокислот в клетку.
Кроме того, как было сказано выше, усиление использования клеткой глюкозы в качестве энергетического субстрата, замедляет распад в ней белка, что приводит к увеличению белковых запасов. За счет такого эффекта инсулин участвует в регуляции процессов развития и роста организма.
Роль инсулина в жировом обмене
Мембранные и внутриклеточные эффекты инсулина приводят к увеличению запасов жира в жировой ткани и печени.
- Инсулин обеспечивает проникновение глюкозы в клетки жировой ткани и стимулирует ее окисление в них.
- Стимулирует образование липопротеиновой липазы в эндотелиальных клетках. Этот вид липазы ферментирует гидролиз триацилглицеролов, связанных с липопротеинами крови, и обеспечивает поступление полученных жирных кислот в клетки жировой ткани.
- Ингибирует внутриклеточную липопротеиновую липазу, таким образом, тормозя липолиз в клетках.
Функции глюкагона
Глюкагон оказывает влияние на углеводный, белковый и жировой обмен. Можно сказать, что глюкагон – антагонист инсулина по оказываемым эффектам. Главным результатом работы глюкагона является повышение концентрации глюкозы в крови. Именно глюкагон обеспечивает поддержание необходимого уровня энергетических субстратов — глюкозы, белков и жиров в крови в период голодания.
1. Роль глюкагона в обмене углеводов.
Обеспечивает синтез глюкозы путем:
- усиления гликогенолиза (расщепления гликогена до глюкозы) в печени,
- усиления глюконеогенеза (синтеза глюкозы из неуглеводистых предшественников) в печени.
2. Роль глюкагона в обмене белков.
Гормон стимулирует транспорт глюкагонных аминокислот в печень, что способствует в клетках печени:
- синтезу белков,
- синтезу глюкозы из аминокислот – глюконеогенезу.
3. Роль глюкагона в жировом обмене.
Гормон активирует в жировой ткани липазу, в результате в крови повышается уровень жирных кислот и глицерина. Это в конечном итоге опять же приводит к повышению концентрации глюкозы в крови:
- глицерин как неуглеводистый предшественник включается в процесс глюконеогенеза – синтез глюкозы;
- жирные кислоты превращаются в кетоновые тела, которые используются в качестве энергетических субстратов, что сохраняет запасы глюкозы.
Взаимосвязь гормонов
Инсулин и глюкагон неразрывно связаны между собой. Их задача – регулировать концентрацию глюкозы в крови. Глюкагон обеспечивает ее повышение, инсулин – понижение. Они выполняют противоположную работу. Стимулом выработки инсулина является повышение концентрации глюкозы в крови, глюкагона – понижение. Кроме того, выработка инсулина тормозит секрецию глюкагона.

Если нарушается синтез одного из этих гормонов, другой начинает работать некорректно. Например, при сахарном диабете уровень инсулина в крови низкий, ингибиторное действие инсулина на глюкагон ослаблено, в результате уровень глюкагона в крове слишком высокий, что приводит к постоянному повышению уровня глюкозы в крови, чем и характеризуется данная патология.

К неправильной выработке гормонов, некорректному их соотношению приводят погрешности в питании. Злоупотребление белковой пищей стимулирует избыточное выделение глюкагона, простыми углеводами – инсулина. Появление дисбаланса в уровне инсулина и глюкагона приводят к развитию патологий.
Источник
Инсулин
относится к гормонам белковой природы.
Он синтезируется b-клетками поджелудочной
железы. Инсулин является одним из
важнейших анаболических гормонов.
Связывание инсулина с клетками-мишенями
приводит к процессам, которые увеличивают
скорость синтеза белка, а также накопление
в клетках гликогена и липидов, являющихся
резервом пластического и энергетического
материала. Инсулин, возможно за счет
своего анаболического эффекта,
стимулирует рост и размножение клеток.
Молекула инсулина состоит из двух
полипептидных цепей — А-цепи и В-цепи.
В состав А-цепи входит 21 аминокислотный
остаток, в состав В-цепи — 30. Эти цепи
связаны между собой двумя дисульфидными
мостиками: один между А7 и В7 ( номера
аминокислот,
считая
с N-концов полипептидных цепей ), второй
между А20 и В19. Третий дисульфидный
мостик находится в цепи А, связывая А6
и А11. Главным физиологическим стимулом
выделения инсулина из b-клеток в кровь
является повышение содержания глюкозы
в крови. Влияние инсулина на обмен
углеводов можно охарактеризовать
следующими
эффектами:
1.Инсулин
увеличивает проницаемость клеточных
мембран для глюкозы в так называемых
инсулин-зависимых тканях.
2.Инсулин
активирует окислительный распад
глюкозы в клетках.
3.Инсулин
ингибирует распад гликогена и активирует
его син тез в гепатоцитах.
4.Инсулин
стимулирует превращение глюкозы в
резервные триглицериды.
5.Инсулин
ингибирует глюконеогенез, снижая
активность некоторых ферментов
глюконеогенеза.
Влияние
инсулина на обмен липидов складывается
из ингибирования липолиза в липоцитах
за счет дефосфорилирования
триацилглицероллипазы и стимуляции
липогенеза.
Инсулин
оказывает анаболическое действие на
обмен белков: он стимулирует поступление
аминокислот в клетки, стимулирует
транскрипцию многих генов и стимулирует,
соответственно, синтез многих белков,
как внутриклеточных, так и внеклеточных.
ГЛЮКАГОН
Глюкагон
представляет собой гормон полипептидной
природы, выделяемый a-клетками
поджелудочной железы. Основной
функцией этого гормона является
поддержание энергетического гомеостаза
организма за счет мобилизации эндогенных
энергетических рессурсов, этим
объясняется его суммарный катаболический
эффект.
В
состав полипептидной цепи глюкагона
входит 29 аминокислотных остатков,
его молекулярная масса 4200, в его составе
от сутствует цистеин. Глюкагон был
синтезирован химическим путем, чем
была окончательно подтверждена его
химическая структура.
Основным
местом синтеза глюкагона являются
a-клетки поджелудочной железы, однако
довольно большие количества этого
гормона образуются и в других органах
желудочно-кишечного тракта. Синтезируется
глюкагон на рибосомах a-клеток в виде
более длин ного предшественника с
молекулярной массой около 9000. В ходе
процессинга происходит существенное
укорочение полипептидной цепи,после
чего глюкагон секретируется в кровь.
В крови он находится в свободной форме,
его концентрация в сыворотке крови
составляет 20-100 нг/л. Период его полужизни
равняется примерно 5 минутам. Основная
часть глюкагона инактивируется в
печени путем гидролитического отщепления
2 аминокислотных остатков с N-конца
молекулы. Секреция глюкагона
a-клетками поджелудочной железы
тормозится высоким уровнем глюкозы в
крови, а также соматостатином, выделяемым
D-клетками поджелудочной железы.
Возможно, что секреция глюкагона
ингибируется также инсулином или ИФР-1.
Стимулируется секреция понижением
концентрации глюкозы в крови, однако
механизм этого эффекта неясен. Кроме
того, секрецию глюкагона стимулируют
соматотропный гормон гипофиза, аргинин
и Са2+.
Механизм
действия глюкагона достаточно хорошо
изучен. Ре цепторы для гормона
локализованы в наружной клеточной
мембране. Образование гормонрецепторных
комплексов сопровождается активацией
аденилатциклазы и увеличением в клетках
концентрации цАМФ, сопровождающимся
активацией протеинкиназы и
фосфорилированием
белков
с изменением функциональной активности
последних. Под действием глюкагона
в гепатоцитах ускоряется мобилизация
гликогена с выходом глюкозы в кровь.
Этот эффект гормона обусловлен активацией
гликогенфосфорилазы и ингибированием
гликогенсинтетазы в результате их
фосфорилирования. Следует заметить,
что глюкагон, в отличие от адреналина,
не оказывает влияния на скорость
гликогенолиза в мышцах.
Глюкагон
стимулирует липолиз в липоцитах,
увеличивая тем самым поступление в
кровь глицерола и высших жирных кислот.
В печени гормон тормозит синтез жирных
кислот и холестерола из ацетил-КоА, а
накапливающийся ацетил-КоА используется
для синтезаацетоновых тел. Таким
образом, глюкагон стимулирует кетогенез.
В
почках глюкагон увеличивает клубочковую
фильтрацию, по-видимому, этим объясняется
наблюдаемое после введения глюкагона
повышение экскреции ионов натрия,
хлора, калия , фосфора и мочевой
44444кислоты.
Соседние файлы в папке 1-30
- #
- #
- #
- #
- #
- #
Источник
функции
поджелудочной железы
Поджелудочная
железа – железа со смешанной функцией.
Морфологической
единицей
железы служат островки Лангерганса,
преимущественно они
расположены
в хвосте железы. Бета-клетки островков
вырабатывают инсулин,
альфа-клетки
– глюкагон, дельта-клетки – соматостатин.
В экстрактах ткани
поджелудочной
железы обнаружены гормоны ваготонин и
центропнеин.
Инсулин
регулирует
углеводный обмен, снижает концентрацию
сахара в крови,
способствует
превращению глюкозы в гликоген в печени
и мышцах. Он повышает
проницаемость
клеточных мембран для глюкозы: попадая
внутрь клетки, глюкоза
усваивается.
Инсулин задерживает распад белков и
превращение их в глюкозу,
стимулирует
синтез белка из аминокислот и их активный
транспорт в клетку,
регулирует
жировой обмен путем образования высших
жирных кислот из продуктов
углеводного
обмена, тормозит мобилизацию жира из
жировой ткани.
В
бета-клетках инсулин образуется из
своего предшественника проинсулина.
Он
переносится
в клеточные аппарат Гольджи, где
происходят начальные стадии
превращения
проинсулина в инсулин.
В
основе регуляции инсулина лежит
нормальное содержание глюкозы в крови:
гипергликемия
приводит к увеличению поступления
инсулина в кровь, и наоборот.
Паравентрикулярные
ядра гипоталамуса повышают активность
при
гипергликемии,
возбуждение идет в продолговатый мозг,
оттуда в ганглии
поджелудочной
железы и к бета-клеткам, что усиливает
образование инсулина и
его
секрецию. При гипогликемии ядра
гипоталамуса снижают свою активность,
и
секреция
инсулина уменьшается.
Гипергликемия
непосредственно приводит в возбуждение
рецепторный аппарат
островков
Лангерганса, что увеличивает секрецию
инсулина. Глюкоза также
непосредственно
действует на бета-клетки, что ведет к
высвобождению инсулина.
Глюкагон
повышает
___________количество глюкозы, что также
ведет к усилению
продукции
инсулина. Аналогично действует гормоны
надпочечников.
Вегетативная
нервная система регулирует выработку
инсулина посредством
блуждающего
и симпатического нервов. Блуждающий
нерв стимулирует выделение
инсулина,
а симпатический тормозит.
Количество
инсулина в крови определяется активностью
фермента инсулиназы,
который
разрушает гормон. Наибольшее количество
фермента находится в печени__и
мышцах. При однократном протекании
крови через печень разрушается до 50 %
находящегося
в крови инсулина.
Важную
роль в регуляции секреции инсулина
выполняет гормон соматостатин,
который
образуется в ядрах гипоталамуса и
дельта-клетках поджелудочной
железы.
Соматостатин тормозит секрецию инсулина.
Активность
инсулина выражается в лабораторных и
клинических единицах.
Глюкагон
принимает участие в регуляции углеводного
обмена, по действию на
обмен
углеводов он является антагонистом
инсулина. Глюкагон расщепляет
гликоген
в печени до глюкозы, концентрация глюкозы
в крови повышается.
Глюкагон
стимулирует расщепление жиров в жировой
ткани.
Механизм
действия глюкагона обусловлен его
взаимодействием с особыми
специфическими
рецепторами, которые находятся на
клеточной мембране. При
связи
глюкагона с ними увеличивается активность
фермента аденилатциклазы и
концентрации
цАМФ, цАМФ способствует процессу
гликогенолиза.
Регуляция
секреции глюкагона. На образование
глюкагона в альфа-клетках
оказывает
влияние уровень глюкозы в крови. При
повышении глюкозы в крови
происходит
торможение секреции глюкагона, при
понижении – увеличение. На
образование
глюкагона оказывает влияние и передняя
доля гипофиза.
Гормон
роста соматотропин
повышает
активность альфа-клеток. В
противоположность
этому гормон дельта-клетки – соматостатин
тормозит
образование
и секрецию глюкагона, так как он блокирует
вхождение в альфа-
клетки
ионов Ca, которые необходимы для образования
и секреции глюкагона.
Физиологическое
значение липокаина.
Он способствует утилизации жиров за
счет
стимуляции образования липидов и
окисления жирных кислот в печени, он
предотвращает
жировое перерождение печени.
Функции
ваготонина
–
повышение тонуса блуждающих нервов,
усиление их
активности.
Функции
центропнеина
–
возбуждение дыхательного центра,
содействие
расслаблению
гладкой мускулатуры бронхов, повышение
способности гемоглобина
связывать
кислород, улучшение транспорта кислорода.
Нарушение
функции поджелудочной железы.
Уменьшение
секреции инсулина приводит к развитию
сахарного диабета,
основными
симптомами которого являются гипергликемия,
глюкозурия, полиурия
(до
10 л в сутки), полифагия (усиленный
аппетит), полидиспепсия (повышенная
жажда).
Увеличение
сахара в крови у больных сахарным
диабетом является результатом
потери
способности печени синтезировать
гликоген из глюкозы, а клеток –
утилизировать
глюкозу. В мышцах также замедляется
процесс образования и
отложения
гликогена.
У
больных сахарным диабетом нарушаются
все виды обмена.
6.
Гормоны надпочечников.
Глюкокортикоиды__Надпочечники
– парные
железы, расположенные над верхними
полюсами
почек.
Они имеют важное жизненное значение.
Различают два типа гормонов:
гормоны
коркового слоя и гормоны мозгового
слоя.
Гормоны
коркового слоя длятся на три группы:
1)
глюкокортикоиды
(гидрокортизон, кортизон, кортикостерон);
2)
минералокортикоиды
(альдестерон, дезоксикортикостерон);
3)
половые
гормоны (андрогены, эстрогены, прогестерон).
Глюкокортикоиды
синтезируются в пучковой зоне коры
надпочечников. По
химическому
строению гормоны являются стероидами,
образуются из холестерина,
для
синтеза необходима аскорбиновая кислота.
Физиологическое
значение глюкокортикоидов.
Глюкокортикоиды
влияют на обмен углеводов, белков и
жиров, усиливают
процесс
образования глюкозы из белков, повышают
отложение гликогена в печени,
по
своему действию являются антагонистами
инсулина.
Глюкокортикоиды
оказывают катаболическое влияние на
белковый обмен,
вызывают
распад тканевого белка и задерживают
включение аминокислот в белки.
Гормоны
обладают противовоспалительным
действием, что обусловлено
снижением
проницаемости стенок сосуда при низкой
активности фермента
гиалуронидазы.
Уменьшение воспаления обусловлено
торможением освобождения
арахидоновой
кислоты из фосфолипидов. Это ведет к
ограничению синтеза
простагландинов,
которые стимулируют воспалительный
процесс.
Глюкокортикоиды
оказывают влияние на выработку защитных
антител:
гидрокортизон
подавляет синтез антител, тормозит
реакцию взаимодействия
антитела
с антигеном.
Глюкокортикоиды
оказывают выраженное влияние на
кроветворные органы:
1)
увеличивают количество эритроцитов за
счет стимуляции красного костного
мозга;
2)
приводят к обратному развитию вилочковой
железы и лимфоидной ткани, что
сопровождается
уменьшением количества лимфоцитов.
Выделение
из организма осуществляется двумя
путями:
1)
75–90 % поступивших гормонов в кровь
удаляется с мочой;
2)
10–25 % удаляется с калом и желчью.
Регуляция
образования глюкокортикоидов.
Важную
роль в образовании глюкокортикоидов
играет кортикотропин передней
доли
гипофиза. Это влияние осуществляется
по принципу прямых и обратных
связей:
кортикотропин повышает продукцию
глюкокортикоидов, а избыточное их
содержание
в крови приводит к торможению кортикотропина
в гипофизе.
В
ядрах переднего отдела гипоталамуса
синтезируется
нейросекрет
кортиколиберин,
который стимулирует образование
кортикотропина
в
передней доле гипофиза, а он, в свою
очередь, стимулирует образование
глюкокортикоида.
Функциональное отношение «гипоталамус
– передняя доля__гипофиза – кора
надпочечников» находится в единой
гипоталамо-гипофизарно-
надпочечниковой
системе, которая играет ведущую роль в
адаптационных
реакциях
организма.
Адреналин
–
гормон мозгового вещества надпочечников
– усиливает
образование
глюкокортикоидов.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
14.02.201524.91 Mб29Эндодонтия.djvu
- #
- #
- #
- #
- #
- #
- #
Источник