Интраоперационная лучевая терапия поджелудочная железа
Лучевая терапия рака поджелудочной железы играет важную роль в терапии злокачественной патологии. Процедура представляет собой воздействие высоких доз радиационного излучения непосредственно на злокачественный очаг. Важность лучевой терапии обусловлена высокой чувствительностью аномальных клеток, зародившихся в эпителиальном слое панкреаса, к радиации.
Особенности лучевой терапии при раке поджелудочной железы
Раковое новообразование панкреаса имеет высокую радиочувствительность, что делает облучение рака поджелудочной железы достаточно эффективным. Но, несмотря на резистентность аномальных структур к ионизирующим лучам, применяется этот метод не во всех клиниках и только при наличии у пациента определённых медицинских показаний.
Ограниченное использование для уничтожения генно модифицированных клеточных структур радиационного излучения связано с анатомическими особенностями секреторно-пищеварительного органа:
- В непосредственной близости от панкреаса расположено большое количество внутренних органов, имеющих определённый порог чувствительности, поэтому облучение может проводиться только ограниченными дозами.
- Без специальных аппаратов достигнуть точного попадания пучка лучей на злокачественный очаг невозможно, что связано с подвижностью секреторно-пищеварительного органа, провоцируемой дыханием человека.
- Из-за удалённого анатомическое расположение панкреаса в большинстве случаев самая эффективная внутренняя радиотерапия (бархитерапия) становится невозможной.

Эффективность лучевой терапии при раке поджелудочной железы
Но, несмотря на трудности проведения процедуры, данная терапевтическая методика, имеющая высокую эффективность при лечении онкопатологий, широко применяется в клиниках, имеющих специальное оборудование. С помощью этой процедуры достигается разрушение максимального количества аномальных клеток, значительное уменьшение размеров злокачественного новообразования и предупреждение возможных рецидивов после радикального удаления опухоли.
Высокая эффективность лучевой терапии при раке поджелудочной даёт возможность использовать данную процедуру как самостоятельный метод лечения на самых ранних стадиях развития патологического состояния. Но это в клинической практике отмечается очень редко, что обусловлено бессимптомным развитием злокачественных структур и поздним их выявлением, когда без хирургического вмешательства обойтись невозможно.
Чтобы специалист более адекватно поставил задачу облучения при раковом поражении панкреаса, необходима точная диагностика рака поджелудочной железы. Только после получения достоверных результатов радиолог сможет определить цели предстоящей процедуры и подобрать наиболее оптимальную схему радиационного воздействия.
Виды облучений при раке поджелудочной железы
Радиохирургия при раке поджелудочной железы проводится несколькими хорошо себя зарекомендовавшими способами.
Чаще всего для разрушения аномальной структуры, локализованной в панкреасе, применяются следующие виды радиационного облучения:
- Дистанционная или наружная радиотерапия. Пучок лучей направляется с расстояния 10-15 см в поражённую область. Благодаря применению современных технологий радиологи могут добиться высокой точности облучения онкоопухоли, позволяющей не задевать радиационными лучами здоровых тканей.
- Интраоперационная гамма-терапия. Процедура проводится одномоментно с оперативным вмешательством, что позволяет разрушать злокачественные клетки прямо на открытом операционном поле. Такой прямой способ воздействия на злокачественное новообразование показывает наиболее высокую результативность.
Стереотаксическая радиотерапия, высокоточная техника разрушения аномального новообразования, для проведения которой используется Кибер-нож (CyberKnife). Данная техника облучения аномальных структур является самой современной и позволяет добиться высоких результатов. Радиохирургия рака поджелудочной железы, при проведении которой применяют Кибер-нож, считается самой безопасной для больного, так как даёт специалисту возможность отследить меняющееся при дыхании положение органа.
Паллиативная лучевая терапия при раке поджелудочной также имеет широкое применение. Её используют на финальном этапе развития процесса малигнизации. Целью такого лечения считается не достижение выздоровления неоперабельного пациента, а облегчение его состояния. Симптоматическая лучевая терапия при раке поджелудочной позволяет купировать большинство мучительных проявлений, сопровождающих последнюю стадию развития злокачественной структуры.
Показания и противопоказания к проведению лучевой терапии
Облучение при раковых новообразованиях секреторно-пищеварительного органа необходимо в большинстве клинических случаев. Как показывает статистика, 65-70% пациентов, у которых выявлена онкология панкреаса, нуждаются в таком лечении. Лучевая терапия при раке поджелудочной железы помогает в большинстве клинических случаев. Основными показаниями к её проведению считаются крупные размеры опухоли, наличие в брюшной полости и регионарных лимфоузлах метастазов, выявление злокачественных клеток на операционном поле после проведения хирургического вмешательства. Также лучевую терапию рекомендуется проводить после того, как выполнена операция при раке поджелудочной железы, в целях профилактики. Облучение в этом случае снижает риски возникновения послеоперационного рецидива болезни. Но у этой процедуры имеется и ряд противопоказаний, делающих её проведение недопустимым.
К ним относятся:
- Начало распада злокачественного новообразования, сопровождающееся внутренним кровотечением или образованием на поверхности секреторно-пищеварительного органа нагноений.
- Начало обширного процесса метастазирования с поражением вторичными очагами отдалённых участков организма.
- Активное прорастание аномальных клеток в находящиеся поблизости полые органы, желудок и кишечник.
- Наличие в анамнезе патологий крови, недавно перенесённого инфаркта миокарда, острого туберкулёза лёгких.
- Кахексия и выраженная интоксикация, провоцирующие общее тяжёлое состояние пациента.
- Гнойные поражения и аллергические высыпания на кожном покрове.
Подготовка и проведение облучения
Для достижения высокой результативности процедуры, позволяющей эффективно разрушить рак поджелудочной железы, пациент должен быть к ней подготовлен.
С этой целью в предлучевом периоде проводят:
- Детальное исследование характера опухолевого новообразования и общего состояния человека, позволяющее выявить все показания и возможные противопоказания к проведению процедуры.
- Составление индивидуального лечебного плана с расчётом ритма облучения и величины суммарной дозы радиации.
- Выявление топографии новообразования и уточнение её границ относительно к кожному покрову.
Благодаря проведённой предоперационной подготовке радиолог с наибольшей точностью проведёт процедуру радиационного разрушения опухоли. Непосредственно перед сеансом пациента, переодетого в больничную рубашку, размещают на столе линейного ускорителя в соответствии с метками на коже. Сделанными во время предлучевой подготовки. После того, как точность расположения онкобольного подтверждена КТ, врач выходит из кабинета и включает аппаратуру. Все нюансы процедуры специалист будет отслеживать удалённо, через монитор, а вести переговоры с пациентом через специальное переговорное устройство.
Схемы и курсы
Наружное облучение при раке поджелудочной железы проводится циклами. Обычно процедуры, при которых пациент получает фиксированную дозу радиации, выполняются ежедневно (кроме выходных) на протяжении 6 недель. Но эти сроки у каждого конкретного пациента могут значительно колебаться, так как подход к лучевой терапии строго индивидуален.
Стандартом при злокачественной опухоли в поджелудочной железе считаются следующие схемы воздействия радиации:
- Конвенциональное 2D-облучение РОД (разовая очаговая доза) составляет 2Гр, а СОД, суммарное воздействие, 60Гр.
- Конформное 3D-облучение разнится в суммарной дозе. При наличии остаточной микроскопической аномальной структуры бывает достаточно 60ГР, а макроскопический очаг, оставшийся на операционном поле, требует увеличения дозировки радиации до 70ГР.
Стоит знать! Правильно подобранные и проведённые курсы радиационного облучения позволяют на 2 и 3 стадии рака поджелудочной железы значительно продлить период ремиссии, а на заключительном этапе улучшить качество жизни.
Дополняющее лечение
Радиотерапия, эффективно разрушающая рак поджелудочной железы, показывает более высокие результаты, когда применяется в одном протоколе с другими методами терапии. Обычно лучевая терапия рака поджелудочной железы дополняет хирургическое вмешательство. Благодаря воздействию радиационного облучения онкологи-хирурги добиваются более высоких результатов операции. Нередко радиохирургическое лечение рака поджелудочной железы проводится в комбинации с химиотерапией. Противоопухолевые препараты в этом случае способствуют усилению эффекта лучевого воздействия. Такие совместные протоколы лечения позволяют добиться более длительного периода ремиссии и сокращают риск развития осложнений и побочных эффектов.
Реабилитация
Продолжительность восстановительного периода после проведения курса лучевой терапии индивидуальна для каждого конкретного пациента. Реабилитация, следующая за процедурой облучения, разрушившей в большей степени рак поджелудочной железы, является при этом опасном заболевании важнейшим этапом терапии.
Чтобы восстановление органов, функционирование которых нарушило облучение рака поджелудочной железы, необходимо выполнять следующие реабилитационные мероприятия:
- правильно питаться (рацион должен быть достаточно калорийным и в то же время щадящим);
- распланировать распорядок дня таким образом, чтобы на отдых оставалось максимальное количество времени;
- вести активный образ жизни с частыми прогулками на свежем воздухе, желательно у водоёмов или в лесополосе, где воздух более чистый и влажный.
Особенности питания до, во время и после проведения лучевой терапии
Правильный и сбалансированный рацион питания при проведении курсов облучения и после них направлен на максимальное уменьшение их последствий. В связи с тем, что лучевая терапия при раке поджелудочной железы зачастую приводит к значительной потере веса, радиологам нередко приходится кардинально менять лечебные курсы. Такие изменения оказывают плохое влияние на качество жизни онкобольного и результаты проводимой терапии. Именно поэтому необходимо кардинально корректировать пищевой рацион.
Диетологи рекомендуют при облучении панкреаса (как до проведения курса, так и во время или после него) специальную бесшлаковую диету. Соблюдение такой диеты при лучевой терапии позволяет достигнуть максимального щажения пищеварительных органов и устранение развивающихся в них бродильных и воспалительных процессов.
Общие её рекомендации заключаются в следующем:
- запрет на солёную, острую, кислую пищу;
- устранение из рациона всех видов молочных продуктов;
- снижение до минимума содержание в блюдах растительной клетчатки.
Стоит знать! Чаще всего при прохождении процедур облучения у пациентов происходит значительное снижение аппетита, поэтому питание при лучевой терапии должно быть обогащено продуктами, содержащими максимальное количество калорий и питательных веществ: шоколадом, взбитыми сливками, мёдом, яйцами, орехами.
Осложнения и последствия лучевого лечения рака поджелудочной железы
Воздействие на организм при ликвидации онкологических поражений радиационным излучением всегда приводит к развитию неприятных, а в некоторых случаях и достаточно серьёзных последствий. Облучение при раке поджелудочной железы не обходится без осложнений. Особенно подвержены их появлению пациенты, проходящие длительные курсы радиотерапии с большими суммарными дозами радиации. Тем не менее, стоит отметить, что последствия лучевой терапии при раке поджелудочной чаще всего имеют лёгкую степень выраженности и не препятствуют доведению до конца лечебного курса.
Основными побочными эффектами, провоцируемыми радиационным излучением, являются:
- разрушение волосяных луковиц, провоцирующее развитие аллопеции (быстрой потере волос, приводящей к облысению);
- появление сухости, шелушения и отёчности на кожных покровах в местах соприкосновения с высокочастотными лучами;
- диспепсические явления со стороны органов пищеварения;
- развитие нервозности и проблем с дыханием.
Некоторые осложнения лучевой терапии при раке поджелудочной могут развиваться уже после прохождения пациентом терапевтического курса. Специалисты называют поздно появляющуюся негативную симптоматику остаточным явлением и связывают её возникновение с длительной реализацией в тканевых структурах радиационного эффекта.
Информативное видео
Будьте здоровы!
Источник
Лечение рака поджелудочной железы и его прогноз
Радикальная хирургическая резекция дает только надежду на излечение. Радикальная панкреатикодуоденэктомия и тотальная панкреаэктомия представляют собой технически сложные процедуры.
Конечно, желаемым результатом является сохранение части поджелудочной железы, но значительная часть проблем в данном случае связана с формированием анастомозов. Тотальная панкреаэктомия приводит к развитию диабета и недостаточности экзокринных функций.
У большинства пациентов на момент установления диагноза опухоль образует узловые и отдаленные метастазы или формирует значительные опухолевые массы, которые являются неоперабельными.
В связи с этим лишь незначительное число больных раком поджелудочной железы может быть подвергнуто хирургической резекции. Таким образом, важным аспектом предоперационной подготовки является тщательное определение размеров и степени распространения опухоли.
В целом, опухоли тела или хвоста поджелудочной железы имеют более благоприятный прогноз. Рак поджелудочной железы характеризуется высокой смертностью: послеоперационная летальность составляет 15-20%, а пятилетняя выживаемость не превышает 15%.
В случае нерезектабельности опухоли обструкция желчных протоков может быть облегчена путем формирования обходных билиодигестивных анастомозов. Обычно это проводится при хирургическом вмешательстве.
Однако в последнее время данная процедура проводится при помощи специальных катетеров для системы желчных протоков (чрескожный чрезпеченочный путь или через фатеров сосочек).
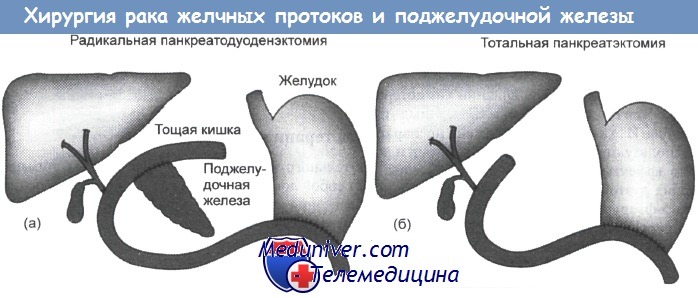
Хирургическая операция рака желчных протоков (а) и поджелудочной железы (б)
Лучевая терапия рака поджелудочной железы
Лучевая терапия, в первую очередь, применяется в качестве паллиативного метода лечения, особенно, для облегчения болей. Для наружного облучения требуется высокая доза (50-60 Гр).
Некоторые исследователи отмечают, что у незначительного числа пациентов выявляется длительная ремиссия опухоли, а иногда и выздоровление. В качестве сенсибилизатора радиации в лучевой терапии применяют 5-фторурацил, который улучшает общее состояние; общие результаты при этом невыразительны.
Для интерстициальной лучевой терапии используется J; иногда дополнительно применяют наружное облучение. Ультразвуковое исследование и компьютерная томография оказывают значительную помощь в планировании лечения.
Химиотерапия рака поджелудочной железы
Число цитотоксических препаратов, применяемых в лечении рака поджелудочной железы, незначительно. Из химиотерапевтических лекарств наиболее часто используют 5-фторурацил, нитрозомочевину, митомицин С и алкилирующие агенты. У разных авторов критерии противоопухолевого ответа различаются.
Комбинированная химиотерапия приводит к уменьшению скорости роста опухоли. Результаты химиотерапии у больных раком поджелудочной железы свидетельствует о небольшой эффективности данного метода лечения; пациенты никогда не излечиваются полностью. Токсичность лечения делает химиотерапию неприменимой для большинства пациентов: это связано с плохим состоянием здоровья и прогрессированием заболевания у больного. В последнее время исследуется внутривенное введение химиотерапевтических препаратов.
Адъювантная химиотерапия с использованием 5-фторурацила и фолиновой кислоты более эффективна у пациентов, подвергшихся резекции рака поджелудочной железы. Однако одновременное применении химио- и лучевой терапии не выявляет значимо положительного результата. У пациентов, прошедших курс химиотерапии, пятилетняя выживаемость составляет 21%, у тех, кто не принимал данные препараты, — 8%.

Паллиативное лечение и прогноз рака поджелудочной железы
Для снятия болей при паллиативном лечении используются анальгетики. Кроме того, в качестве паллиативного метода применяют лучевую терапию. Химический блок, осуществляемый путем введения спирта в брюшное сплетение, является трудоемкой процедурой, но иногда очень эффективной для уменьшения боли.
Подкожное дренирование желчных протоков способствует уменьшению зуда и стеатореи, являющихся следствием механической желтухи. Стероиды на время могут улучшать аппетит. В целом, прогноз для пациентов с раком поджелудочной железы неблагоприятный. Как для мужчин, так и для женщин медиана выживаемости составляет менее 1 года. До 5 лет доживают менее 2% всех пациентов.
— Вернуться в оглавление раздела «Онкология»
Оглавление темы «Опухоли печени и поджелудочной железы»:
- Клиника и диагностика рака печени
- Лечение и прогноз рака печени
- Ангиосаркома печени — причины, диагностика
- Гепатобластома — диагностика, лечение
- Рак желчного пузыря и желчных протоков — частота, причины, механизмы развития
- Клиника и диагностика рака желчного пузыря
- Лечение рака желчного пузыря и желчных путей
- Рак поджелудочной железы — частота, причины, механизмы развития
- Исследование и диагностика рака поджелудочной железы
- Лечение рака поджелудочной железы и его прогноз
Источник
Многие знают, что лучевая терапия при раке бывает двух основных разновидностей, в зависимости от того, когда ее проводят:
- Неоадъювантная проводится до операции. Она помогает сократить объем опухоли, упростить ее удаление, перевести из неоперабельной формы в операбельную.
- Адъювантную лучевую терапию назначают после операции. Она помогает уничтожить опухолевые клетки, которые остались в теле пациента, и тем самым предотвратить рецидив.
Если рак нельзя удалить хирургическим путем, лучевая терапия может быть назначена в паллиативных целях, чтобы уничтожить максимальный объем опухолевой ткани, справиться с болью, кровотечением и другими симптомами.
Существует и еще одна разновидность лучевой терапии — интраоперационная (сокращенно — ИОЛТ). Ее проводят прямо на операционном столе. Поговорим о том, для чего она нужна, как проводится, и какие имеет преимущества.
Для чего облучать опухоль во время операции?
Классическая процедура лучевой терапии напоминает рентгенографию, только продолжается дольше, и во время нее применяют более высокие дозы излучения. Она эффективно уничтожает многие злокачественные опухоли, но обладает одним недостатком, который ограничивает возможности ее применения. Рентгеновские и радиоактивные лучи повреждают не только раковые, но и здоровые клетки. Это грозит серьезными осложнениями и повышенным риском возникновения новой злокачественной опухоли в зоне облучения.
Ученые постоянно ищут новые технологии, которые помогли бы подавать в опухоль максимальную дозу излучения, не затрагивая окружающие здоровые ткани. Есть разные решения, и одно из них — интраоперационная лучевая терапия, когда облучение проводят прямо на операционном столе, пока пораженный орган «открыт». У такого подхода есть некоторые преимущества:
- Если врач планирует провести курс адъювантной лучевой терапии, нужно выждать некоторое время после операции. Нужно, чтобы произошло заживление. Но такая отсрочка повышает риск рецидива. Интраоперационная ЛТ уничтожает раковые клетки сразу же после того, как удалена опухоль.
- Излучение не проходит через кожу и не повреждает ее.
- Врач может направить пучок лучей точно в то место, где находилась злокачественная опухоль, практически не затрагивая здоровые ткани. Соседние органы можно отодвинуть, защитить.
- Интраоперационная ЛТ в среднем продолжается 4–5 минут. Зачастую она помогает избежать длительного (5–6 недель) курса лучевой терапии после операции.
- Метод позволяет воздействовать на опухоль высокими дозами излучения, не боясь серьезных побочных эффектов. В целом применение интраоперационной ЛТ помогает сократить число осложнений у пациентов.
В каких случаях прибегают к интраоперационной лучевой терапии?
Как правило, этот метод лечения применяют у пациентов с ранними стадиями злокачественных опухолей. Часто интраоперационную ЛТ сочетают с курсом неоадъювантной лучевой терапии. Она показана в случаях, когда опухоль сложно удалить, и когда есть риск того, что в теле пациента после операции могли остаться раковые клетки.
Интраоперационная лучевая терапия широко применяется в онкологии, ее эффективность доказана многочисленными научными исследованиями. Впервые она была применена еще в 1960-х годах — для лечения злокачественных опухолей органов живота. Сейчас показания к ее применению расширились. Например, врачи часто используют интраоперационное облучение во время органосохраняющих операций при раке молочной железы.
Как проводят процедуру?
Раньше, для того чтобы провести ИОЛТ, пациента нужно было доставить из операционной в отделение лучевой терапии. При этом нужно было обеспечить стерильность — ведь облучение проводится на открытой ране. В 1990-х годах появились удобные мобильные устройства. Их можно использовать прямо в операционной. Излучение в рану подают через специальный аппликатор.
В настоящее время наибольшее распространение приобрела интраоперационная электронная лучевая терапия, во время которой используют электроны с высокой энергией.
Для проведения интраоперационной лучевой терапии необходимо специальное оборудование, врач должен обладать соответствующими навыками и уметь правильно определять показания. В настоящее время немногие онкологические центры практикуют этот вид лечения. Мы знаем, куда обратиться, и поможем попасть в нужную клинику. Свяжитесь со специалистом компании МедНавигатор +7 (495) 721-30-21.
Применение при раке молочной железы
Планируя операцию при раке молочной железы на ранних стадиях, хирургу зачастую приходится делать непростой выбор между мастэктомией (полным удалением молочной железы) и органосохраняющей операцией. С одной стороны, если расширить объем вмешательства и удалить всю молочную железу, вероятность того, что в теле женщины останется опухолевая ткань, будет минимальной. В то же время, хочется удалить опухоль так, чтобы сохранить грудь.
Были проведены исследования, которые показали: лампэктомия (удаление пораженной опухолью части молочной железы) с последующим курсом лучевой терапии так же эффективна, как и мастэктомия, и не сопровождается повышенным риском рецидива. При этом ИОЛТ может стать дополнением или альтернативой классической лучевой терапии. Ее актуальность особенно возросла после того, как врачи начали чаще практиковать онкопластические операции — когда одновременно с удалением опухоли проводят реконструктивно-пластическое вмешательство, восстанавливают внешний вид груди. При этом, за счет смещения тканей, повышается риск того, что в ране останутся опухолевые клетки.
Так, согласно данным одного наблюдения, у женщин, перенесших онкопластическую операцию в сочетании с ИОЛТ, более чем в 90% отмечался отличный косметический результат, а частота возникновения сером находилась на уровне 2%.
В одном из исследований при сравнении ИОЛТ и классической лучевой терапии оказалось, что спустя четыре года после лечения результаты в двух группах были примерно одинаковыми. В другом исследовании 78 пациентов перенесли операцию с ИОЛТ, впоследствии не было отмечено ни одного рецидива.
Идеальными пациентами для процедуры считаются женщины старше 50 лет с раком молочной железы на ранних стадиях.
Интраоперационная лучевая терапия может продолжаться от 1 до 30 минут, в зависимости от особенностей излучения.
Применение при других онкологических заболеваниях
ИОЛТ может применяться далеко не только при раке молочной железы. Есть немало данных о проведении этого вида лечения при других онкологических заболеваниях:
- рак головы и шеи;
- рак толстой и прямой кишки (колоректальный рак);
- саркома мягких тканей;
- злокачественные опухоли в педиатрии;
- рак шейки матки, мочевого пузыря, почек, простаты;
- рак желудка, поджелудочной железы.
Не всякая онкологическая клиника может предложить пациентам наиболее современные, оптимальные методы лечения. Взять хотя бы рак молочной железы: некоторым женщинам лечащие врачи рекомендовали мастэктомию, но специалисты компании МедНавигатор находили врача-эксперта, который выполнял органосохраняющую операцию, и это не сопровождалось более высоким риском рецидива.
Свяжитесь с нами, мы поможем вам получить второе мнение у ведущих специалистов и попасть на лечение в лучшие клиники мира. Воспользуйтесь нашими знаниями и опытом: +7 (495) 721-30-21.
Источник