Оценка эндокринной функции поджелудочной железы
Функции поджелудочной железы
Добавлено: 01.11.2019
Добавил: СветланаСергеевна
Просмотров: 17619
Комментариев: 1
Поджелудочная железа – это орган пищеварительной системы, обеспечивающий переваривание питательных веществ – жиров, белков, углеводов. Вместе с тем, поджелудочная железа – это орган эндокринной системы. Она секретирует в кровь гормоны, регулирующие все виды обмена веществ. Таким образом, поджелудочная железа выполняет две функции – эндокринную и экзокринную.
Эндокринная функция поджелудочной железы
Поджелудочная железа секретирует в кровь пять гормонов, регулирующих в основном углеводный обмен. Эндокринная часть поджелудочной железы составляет не более 2% от всей массы органа. Она представлена островками Лангерганса – скоплениями клеток, которые находятся в окружении паренхимы поджелудочной железы.
Большинство островков Лангерганса сосредоточены в хвосте органа. По этой причине поражение хвоста поджелудочной железы воспалительным процессом часто приводит к недостаточности эндокринной функции органа. В островках Лангерганса находятся клетки разных типов, секретирующие разные гормоны. Больше всего в них содержится бета-клеток, вырабатывающих инсулин.
Функции гормонов поджелудочной железы
Поджелудочная железа вырабатывает пять гормонов. Два из них существенно влияют на обмен веществ. Это инсулин и глюкагон. Другие гомоны имеют меньшее значение для регуляции метаболизма, либо секретируются поджелудочной железой в малых количествах.
Инсулин
Анаболический гормон, основной функцией которого является транспорт сахара в клетки организма. Он снижает уровень глюкозы в крови за счет:
- изменения проницаемости клеточных мембран для глюкозы
- активации ферментов, обеспечивающих расщепление глюкозы
- стимуляции превращения глюкозы в гликоген
- стимуляции превращения глюкозы в жир
- угнетения образования глюкозы в печени
Другие функции инсулина
- стимулирует синтез белков и жиров
- препятствует расщеплению триглицеридов, гликогена и белков
Глюкагон
Принимает важнейшее участие в углеводном обмене. Основная функция этого гормона поджелудочной железы – стимуляция гликогенолиза (процесс расщепления гликогена, в процессе которого в кровь выделяется глюкоза).
Кроме того, глюкагон:
- активирует процесс образования глюкозы в печени
- стимулирует расщепление жира
- стимулирует синтез кетоновых тел
Физиологическое действие глюкагона:
- повышает артериальное давление и частоту пульса
- повышает силу сердечных сокращений
- способствует расслаблению гладкой мускулатуры
- усиливает кровоснабжение мышц
- повышает секрецию адреналина и других катехоламинов
Соматостатин
Вырабатывается не только в поджелудочной железе, но и в гипоталамусе. Его единственная функция – это подавление секреции других биологически активных веществ:
- серотонина
- соматотропина
- тиреотропного гормона
- инсулина
- глюкагона
Вазоактивный интестинальный пептид
Стимулирует перистальтику кишечника, увеличивает приток крови к органам ЖКТ, угнетает выработку соляной кислоты, усиливает выработку пепсиногена в желудке.
Панкреатический полипептид
Стимулирует желудочную секрецию. Подавляет внешнесекреторную функцию ПЖ.
Физиологическое действие глюкагона поджелудочной железы
Экзокринная функция ПЖ заключается в секреции панкреатического сока. По системе протоков он попадает в двенадцатиперстную кишку, где участвует в процессе пищеварения. Секрет поджелудочной железы содержит:
- ферменты — расщепляют питательные вещества, поступающие в кишечник с едой
- ионы бикарбоната — ощелачивают желудочный сок, поступающий в двенадцатиперстную кишку из желудка
Регуляция экзокринной функции поджелудочной железы осуществляется гормонами, которые вырабатываются в желудке и кишечнике:
- холецистокинин
- секретин
- гастрин
Все эти вещества угнетают активность поджелудочной железы. Они вырабатываются в ответ на растяжение стенок желудка и кишечника. Их секрецию стимулирует панкреатический сок, попадающий в двенадцатиперстную кишку после приема пищи.
Функции ферментов поджелудочной железы
ПЖ вырабатывает ферменты, которые переваривают все виды питательных веществ – углеводы, белки и жиры.
1. Протеазы
Ферменты, расщепляющие белки. Учитывая, что разновидностей протеинов много, поджелудочная железа вырабатывает несколько видов протеолитических ферментов:
- химотрипсин
- эластаза
- трипсин
- карбоксипептидаза
2. Липаза
Этот фермент расщепляет жиры.
3. Амилаза
Фермент, расщепляющий полисахариды (сложные углеводы).
4. Нуклеазы
Несколько видов ферментов, которые расщепляют нуклеиновые кислоты (ДНК и РНК).
Нарушение функции поджелудочной железы
Некоторые болезни поджелудочной железы сопровождаются нарушением функции этого органа. Чаще всего это происходит при остром или хроническом панкреатите, когда вследствие воспалительного процесса уничтожается большая часть паренхимы поджелудочной железы. Экзокринная функция со временем нарушается у большинства больных хроническим панкреатитом. Эндокринная – приблизительно у четверти пациентов.
Нарушение экзокринной функции сопровождается расстройством пищеварения и диспепсическими симптомами. Для этого состояния характерны следующие признаки:
- полифекалия
- частый и жидкий стул
- наличие жира в кале
- вздутие кишечника
- похудение
При нарушении эндокринной функции поджелудочной железы обычно развивается сахарный диабет. Он протекает легче, чем классический диабет первого типа, так как не все бета-клетки островков Лангерганса уничтожаются. Тем не менее, через несколько лет от начала заболевания у пациента обычно возникает потребность в инъекциях инсулина. Иногда удается нормализовать уровень глюкозы в крови при помощи диеты и сахароснижающих препаратов.
Источник
Позвоните в клинику, и мы расскажем, как правильно подготовиться к сдаче необходимых вам анализов. Строгое соблюдение правил гарантирует точность исследований.
Накануне сдачи анализов необходимо воздержаться от физических нагрузок, приема алкоголя и существенных изменений в питании и режиме дня. Большинство исследований сдаются строго натощак, то есть должно пройти не менее 12 и не более 16 часов после последнего приема пищи.
За два часа до сдачи следует воздержаться от курения и кофе. Все анализы крови сдаются до проведения рентгенографии УЗИ и физиотерапевтических процедур. По возможности воздержитесь от приема лекарств, а если это невозможно, предупредите доктора, назначающего вам анализы.
Все анализы рекомендуется сдавать в утреннее время, так как лабораторные нормы рассчитаны именно для утренних показателей. Исключение составляют случаи, когда докторунеобходимо оценить ваше состояние на данный момент.
Очень важно точно следовать указанным рекомендациям в избежание ошибок на преаналитическом этапе проведения исследования!
Исследования крови
Общий анализ крови
Кровьсдается из пальца или из вены. Подготовка: кровь сдается натощак. Перед сдачей анализа избегайте физический нагрузок, стрессов. Время и место забора материала: в течение дня, в клинике.
Биохимический анализ крови
Кровь сдается из вены. Определение биохимических показателей позволяет оценить все обменные процессы, протекающие в организме, а также функцию органов и систем. Подготовка: кровь сдается натощак. Время и место забора материала: до 14 часов, в клинике (электролиты — в будние дни до 09.00).
Глюкозотолерантный тест
Соблюдение правил подготовки к сдаче анализа позволит получить достоверные результаты и правильно оценить работу поджелудочной железы, а следовательно, назначить адекватное лечение. Подготовка: необходимо соблюдать правила подготовки и рекомендации по питанию, данные вашим лечащим врачом. Количество углеводов в пище должно быть не менее 125 г. в день в течение 3-х дней перед проведением теста. Физические нагрузки не допускаются в течение 12 часов перед началом теста и во время его проведения. Время и место забора материала: ежедневно до 12.00, в клинике.
Гормональные исследования
Гормоны — вещества, концентрация которых в крови изменяется циклически и имеет суточные колебания, поэтому анализ должен забираться в строгом соответствии с физиологическими циклами или по рекомендации вашего лечащего врача. Подготовка: кровь сдается натощак. Время и место забора материала: ежедневно до 11.00, в клинике.
Исследование системы гемостаза
Кровь сдается из вены. Подготовка: кровь сдается натощак. Время и место забора материала: в будние дни до 09.00, в клинике.
Определение группы крови
Кровь сдается из вены. Подготовка: кровь сдается натощак. Время и место забора материала: до 14 часов, в клинике.
Определение антител к возбудителям
Кровь сдается из вены. Подготовка: кровь сдается натощак. Время и место забора материала: до 14 часов, в клинике.
Гепатиты (В, С)
Кровь сдается из вены. Подготовка: кровь сдается натощак. Время и место забора материала: до 14 часов, в клинике.
RW (сифилис)
Кровь сдается из вены. Подготовка: кровь сдается натощак. Время и место забора материала: до 14 часов, в клинике.
Экспресс-анализ на ВИЧ
Кровь сдается из вены. Подготовка: кровь сдается натощак. Время и место забора материала: в течение дня, в клинике.
Источник
Эндокринная
часть поджелудочной железы образована
лежащими между ацинусов панкреатическими
островками, или островками Лангерганса
— светлыми
образованиями размером 50— 500 мкм,
состоящими из разных типов эпителиальных
клеток (альфа-, бета-и дельта-клеток).
Островки составляют около 1,5% объема
железы; у человека их насчитывается
около 1 млн.
Островки
состоят из клеток – инсулоцитов, среди
которых на основании наличия в них
различных по физико-химическим и
морфологическим свойствам гранул
выделяют 5 основных видов:
—
бета-клетки, синтезирующие инсулин
(60—80
%);
—
альфа-клетки, продуцирующие глюкагон
(20
%);
—
дельта-клетки, образующие соматостатин;
—
D1-клетки, выделяющие ВИП;
 —
—
PP-клетки, вырабатывающие панкреатический
полипептид.
Кроме
того, методами иммуноцитохимии и
электронной микроскопии было показано
наличие в островках незначительного
количества клеток, содержащих гастрин,
тиролиберин и соматолиберин.
Островки
представляют собой компактные пронизанные
густой сетью фенестрированных капилляров
скопления упорядоченных в гроздья или
тяжи внутрисекреторных клеток. Клетки
слоями окружают капилляры островков,
находясь в тесном контакте с сосудами;
большинство эндокриноцитов контактируют
с сосудами либо посредством цитплазматических
отростков, либо примыкая к ним
непосредственно.
3.1. Инсулин: химическая природа, регуляция секреции, механизм действия, роль в обмене.
Инсулин
представляет собой простой полипептид
с молекулярной массой около 6000, состоящий
из двух линейных цепей: А — с 21 аминокислотой
и В — с 30 аминокислотами, соединенных
двумя бисульфидными мостиками. В цепи
А есть еще один «внешний» бисульфидный
мостик. Структура инсулина у различных
животных в основном совпадает. В настоящее
время принята точка зрения, согласно
которой вначале синтезируется одна
цепь аминокислот с последующим
свертыванием молекулы и образованием
бисульфидных связей. В этом процессе
участвует так называемый соединительный
пептид, или пептид С, состоящий из 33
аминокислот и соединяющий цепи А и В.
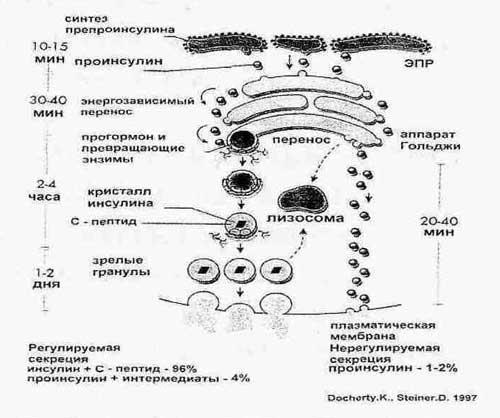
После свертывания образуется предшественник
инсулина, или проинсулин, с молекулярной
массой свыше 9000.
Биологическая
активность проинсулина составляет
примерно 10% активности инсулина.
Соединительный пептид С отщепляется
от инсулина в гранулах β-клеток перед
секрецией в кровь и поступает в нее в
количестве, эквимолекулярном инсулину.
Определение уровня пептида С является
более надежным индикатором секреции
β-клеток, чем определение собственно
инсулина, так как последний в отличие
от С-пептида частично задерживается в
печени, может подвергаться воздействию
циркулирующих противоинсулиновых
антител и подвергаться другим воздействиям,
искажающим истинную картину. Разъединение
цепей А и В приводит к полной инактивации
инсулина.


Регуляция
секреции инсулина происходит на основе
простой обратной связи, регулирующим
фактором в которой является уровень
гликемии: секреция инсулина повышается
при гипергликемии и понижается при
гипогликемии. При этом (3-клетки являются
одновременно хеморецепторами и
эффекторами. К основной регуляции
функции (3-клеток присоединяется
модулирующее влияние некоторых
гормональных факторов: СТГ, гормонов
надпочечников — стероидов и катехоламинов.
Вероятно, в интраинсулярной регуляции
участвуют глюкагон и соматостатин, а
также ионы кальция, связанные с
кальмодулином. Определенное влияние
на секрецию инсулина могут оказывать
и нервные факторы (блуждающий нерв).
Косвенное участие в регуляции секреции
инсулина принимают адреналин, глюкагон,
глюкокортиконцы и тиреоидные гормоны,
а соответственно, АКТГ и ТТГ, вызывающие
гипергликемию. Предполагается, что
существуют также интраинсулярные
регуляторные связи между α-, β- и
γ-клетками, в основе которых лежит
непосредственное (не связанное с
гипергликемией) стимулирующее действие
глюкагона на секрецию инсулина. К другим
эндогенным факторам, оказывающим
стимулирующее воздействие на секрецию
инсулина, относятся некоторые аминокислоты
(особенно лейцин и аргинин), ионы натрия,
холинергические вещества; высокая
внутриклеточная концентрация калия
блокирует секрецию инсулина.
Секреция
инсулина происходит постоянно, и около
50% инсулина, высвобождаемого из β-клеток,
никак не связано с приемом пищи или
иными влияниями. В течение суток
поджелудочная железа выделяет примерно
1/5 от запасов имеющегося в ней инсулина.
Главным
стимулятором секреции
инсулина является повышение концентрации
глюкозы в крови выше 5,5 ммоль/л, максимума
секреция достигает при 17-28 ммоль/л.
Особенностью этой стимуляции является
двухфазное усиление секреции инсулина:
первая
фаза длится
5-10 минут и концентрация гормона может
10-кратно возрастать, после чего его
количество понижается,вторая
фаза начинается
примерно через 15 минут от начала
гипергликемии и продолжается на
протяжении всего ее периода, приводя
к увеличению уровня гормона в 15-25 раз.
Чем
дольше в крови сохраняется высокая
концентрация глюкозы, тем большее число
β-клеток подключается к секреции
инсулина.
Стимуляция синтеза инсулина
происходит от момента проникновения
глюкозы в клетку до трансляции инсулиновой
мРНК. Она регулируется повышением
транскрипции гена инсулина, повышением
стабильности инсулиновой мРНК и
увеличением трансляции инсулиновой
мРНК.
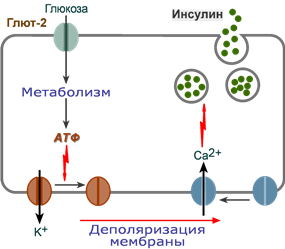
Стимуляция секреции инсулина
1.
После проникновения глюкозы в β-клетки
(через ГлюТ-1 и ГлюТ-2) она
фосфорилируется гексокиназой
IV (глюкокиназа,
обладает низким сродством к глюкозе),
2.
Далее глюкоза аэробно окисляется, при
этом скорость окисления глюкозы линейно
зависит от ее количества,
3.
В результате нарабатывается АТФ,
количество которого также прямо зависит
от концентрации глюкозы в крови,
4.
Накопление АТФ стимулирует закрытие
ионных K+-каналов,
что приводит к деполяризации мембраны,
5.
Деполяризация мембраны приводит к
открытию потенциал-зависимых Ca2+-каналов
и притоку ионов Ca2+ в
клетку,
6.
Поступающие ионы Ca2+ активируют
фосфолипазу C и запускают кальций-фосфолипидный
механизм проведения сигнала с образованием
ДАГ и инозитол-трифосфата,
7.
Появление инозитол-трифосфата в цитозоле
открывает Ca2+-каналы
в эндоплазматической сети, что ускоряет
накопление ионов Ca2+ в
цитозоле,
8.
Резкое увеличение концентрации в клетке
ионов Ca2+ приводит
к перемещению секреторных гранул к
плазматической мембране, их слиянию с
ней и экзоцитозу кристаллов зрелого
инсулина наружу,
9.
Далее происходит распад кристаллов,
отделение ионов Zn2+ и
выход молекул активного инсулина в
кровоток.
Описанный
ведущий механизм может корректироваться
в ту или иную сторону под действием ряда
других факторов, таких как аминокислоты,
жирные кислоты, гормоны ЖКТ
и других гормоны, нервная
регуляция.
Из
аминокислот на секрецию гормона наиболее
значительно влияют лизин и аргинин.
Но сами по себе они почти не стимулируют
секрецию, их эффект зависит от наличия
гипергликемии, т.е. аминокислоты только
потенциируют действие глюкозы.
Свободные
жирные кислоты также
являются факторами, стимулирующими
секрецию инсулина, но тоже только в
присутствии глюкозы. При гипогликемии
они оказывают обратный эффект, подавляя
экспрессию гена инсулина.
Логичной
является положительная чувствительность
секреции инсулина к действию гормонов
желудочно-кишечного тракта
– инкретинов (энтероглюкагона
и глюкозозависимого инсулинотропного
полипептида), холецистокинина, секретина, гастрина, желудочного
ингибирующего полипептида.
Клинически
важным и в какой-то мере опасным является
усиление секреции инсулина при длительном
воздействии соматотропного
гормона, АКТГ и глюкокортикоидов, эстрогенов, прогестинов.
При этом возрастает риск истощения
β-клеток, уменьшение синтеза инсулина
и возникновение инсулинзависимого
сахарного диабета. Такое может наблюдаться
при использовании указанных гормонов
в терапии или при патологиях, связанных
с их гиперфункцией.
Нервная
регуляция β-клеток поджелудочной железы
включает адренергическую и холинергическую регуляцию.
Любые стрессы (эмоциональные и/или
физические нагрузки, гипоксия,
переохлаждение, травмы, ожоги) повышают
активность симпатической нервной
системы и подавляют секрецию инсулина
за счет активации α2-адренорецепторов.
С другой стороны, стимуляция
β2-адренорецепторов
приводит к усилению секреции.
Также
выделение инсулина контролируется n.vagus,
в свою очередь находящегося под контролем
гипоталамуса, чувствительного к
концентрации глюкозы крови.
К
органам-мишеням инсулина можно отнести
все ткани, имеющие к нему рецепторы.
Рецепторы инсулина находятся практически
на всех клетках, кроме нервных, но в
разном количестве. Наибольшая их
концентрация наблюдается на мембране
гепатоцитов (100-200 тыс на клетку) и
адипоцитов (около 50 тыс на клетку), клетка
скелетной мышцы имеет около 10 тысяч
рецепторов, а эритроциты — только 40
рецепторов на клетку.
Нервные
клетки не имеют рецепторов к инсулину,
который просто не проникает через
гематоэнцефалический барьер.
Рецептор
инсулина представляет собой гликопротеин,
построенный из двух димеров, каждый из
которых состоит из α- и β-субъединиц,
(αβ)2.
Обе субъединицы кодируются одним геном
19 хромосомы и формируются в результате
частичного протеолиза единого
предшественника. Период полужизни
рецептора составляет 7-12 часов.
При
связывании инсулина с рецептором
изменяется конформация рецептора и
они связываются друг с другом, образуя
микроагрегаты.
Связывание
инсулина с рецептором инициирует
ферментативный каскад реакций фосфорилирования.
Первым делом аутофосфорилируются тирозиновые
остатки на
внутриклеточном домене самого рецептора.
Это активирует рецептор и ведет
к фосфорилированию остатков серина
на особом белке, называемом субстрат
инсулинового рецептора (СИР,
или чаще IRS от
англ. insulin receptor substrate).
Таких IRS выделяют четыре типа – IRS‑1,
IRS‑2, IRS‑3, IRS‑4.
Также к субстратам инсулинового рецептора
относят белки Grb-1 и Shc,
которые отличаются от IRS аминокислотной
последовательностью.
Дальнейшие
события разделяются по двум направлениям:
1.
Реакции, связанные с активностью ферментов
MAP-киназ –
в целом управляют активностью хроматина.
2.
Процессы, связанные с
активацией фосфоинозитол-3-киназы –
в основном контролируют метаболические
реакции. Сюда же относятся процессы,
которые регулируют активность глюкозных
транспортеров и
поглощение глюкозы клетками.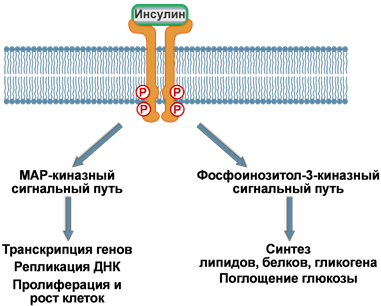
Тем
не менее, такое подразделение
условно,
так как в клетке присутствуют ферменты,
чувствительные к активации и того и
другого каскадного пути.
Соседние файлы в папке Рефераты Презентации
- #
- #
- #
- #
- #
Источник


