Поджелудочная железа причины патогенез

Патогенез панкреатита изучается уже много лет, и, тем не менее, не все процессы, приводящие к его развитию, изучены. Исследования проводятся до сих пор, так как они могут помочь в лечении и профилактике данного заболевания. Даже с использованием современных методов диагностики выявить причину развития панкреатита не удается. У 20% больных связь возникновения заболевания с этиологическим фактором не прослеживается.
Причины
Панкреатит может развиваться под воздействием многих факторов. Все причины заболевания можно разделить на: врожденные и приобретенные.
К врожденным или наследственным факторам относят муковисцидоз, аминоацидурию и др.
Приведем самые распространенные из приобретенных факторов:
- Алкогольная интоксикация. Это ведущая причина панкреатита. Она составляет 80% от всех остальных факторов, вызывающих заболевание.
- Болезни желчного пузыря, печени, желчевыводящих путей.
- Язвенная болезнь желудка и двенадцатиперстной кишки.
- Острая почечная недостаточность.
- Аутоиммунные заболевания.
- Эндокринная патология: болезнь Иценко-Кушинга, гиперпаратиреоидизм.
- Травмы живота.
- Воздействие бытовых, пищевых и промышленных токсинов, передозировка лекарственных препаратов.
- Сосудистые заболевания: неспецифический аортоартериит.
Патогенез острого панкреатита
В развитии панкреатита играет роль гиперсекреция панкреатического сока, повышение давления в выводящей системе и преждевременная активация ферментов. Патогенез заболевания связан с гиперсекрецией панкреатического сока, что может быть спровоцировано избыточным употреблением пищи, содержащей большое количество жиров. Такой рацион стимулирует обильную секрецию сока, из-за которой и повышается внутрипротоковое давление.
Ферментная теория имеет в основе нарушение физиологического выведения ферментов из поджелудочной железы. Ферменты, которые становятся активными, еще в паренхиме органа вызывают его деструкцию. Самым опасным ферментом является трипсин. Он влияет на калликреин-кининовую систему, тем самым повышая проницаемость сосудов, вызывая отеки и другие нарушения микроциркуляции. При остром панкреатите такие изменения происходят в короткие сроки, вызывая тяжелую интоксикацию и шок.
Патогенез панкреатита связан с воздействием фермента липазы, которая разрушает клеточные мембраны и триглицериды. В результате их распада образуются свободные жирные кислоты, pH смещается в сторону ацидоза. Кислая среда активирует трипсин и начинается разрушение структур поджелудочной железы. Так как клетки органа также содержат ферменты, запускается каскад деструктивных процессов. Клеточные гидролитические ферменты разрушают стенки сосудов и других тканей, из-за чего в паренхиме поджелудочной образуются кровоизлияния.
Учитывая механизмы развития панкреатита можно сделать вывод, что на начальных стадиях происходят процессы жирового панкреатита, а далее они перетекают в геморрагический панкреонекроз.
Имеет основания инфекционная теория панкреатита. Ее патогенез основан на развитии заболевания из-за проникновения микроорганизмов в железки органа. Инфекционные агенты могут проникать в паренхиму поджелудочной железы через протоковую систему, лимфу или кровь. Не редко развиваются гнойные осложнения в ткани органа.
Не лишена анатомических и функциональных начал нервно-рефлекторная теория. Из-за нарушения нервной регуляции, в частности, при повышении тонуса блуждающего нерва, повышается активность секреторного аппарата поджелудочной железы и ее чувствительность к гормональным и пищевым раздражителям.
Панкреатит оказывает влияние на системную гемодинамику. Патогенез сосудистых нарушений основан на повышении проницаемости стенок сосудов и переходу жидкой части крови в интерстициальное пространство, развитию гиповолемического шока. Сосудистая недостаточность быстро нарастает без соответствующих лечебных мероприятий и не редко приводит к летальному исходу.
Патогенез билиарного панкреатита
Этот вид панкреатита развивается при патологии билиарной системы. Патогенез билиарного панкреатита связан с забросом поджелудочного сока и желчи. Данные процессы происходят при повышении давления в желчевыводящих путях или двенадцатиперстной кишке.
Причиной может послужить морфологическое изменение сфинктера Одди или большого дуоденального сосочка. В поджелудочной железе активированный трипсин приводит к лизису паренхимы и самоперевариванию. В дальнейшем разрушенные участки органа замещаются фиброзной тканью. Все патологические процессы при билиарном панкреатите приводят к потере функции железы.
Алкогольный панкреатит
Прием алкоголя служит сигналом для выделения большого количества панкреатического сока. Он отличается насыщенностью белками и низким содержанием бикарбонатов. Такой секрет имеет густую консистенцию и приводит к закупорке выводящих протоков и образование кальцинатов. Патогенез этого процесса завершается развитием аутолиза и образования ретенционных кист, псевдокист.
Дополнительным механизмом, способствующим формированию камней в протоках, является дефицит литостатина – белка, который стабилизирует кальций. Он выполняет важную функцию, так как панкреатический сок насыщен солями кальция. Известно, что алкоголь вызывает спазм сфинктера Одди, оказывает общие метаболические эффекты (гиперметаболизм), стимулирует железы внешней и внутренней секреции и усиливает кислотопродуцирующую функцию желудка.
Патогенез наследственного панкреатита
При семейной форме панкреатита происходит генная мутация. Патогенез наследственной формы основан на замене аминокислоты лейцин на валин.
Такая мутация приводит к нарушению дезактивации трипсиногена внутри клетки. В результате этого, трипсиноген превращается в трипсин, что ведет к процессу аутолиза.
Аллергический панкреатит
Аллергический панкреатит встречается чаще у больных бронхиальной астмой, крапивницей, аллергическим ринитом. При данном типе заболевания играет роль органная аллергическая реакция. Он разделен на три этапа:
- На первом происходит сенсибилизация организма
- 2-й этап протекает с образование антител к аллергену
- Последний этап – это поражение ткани поджелудочной железы
Что может вызвать аутоиммунный процесс? Это продукты распада белка, микробные токсины, элементы тканей больного при нарушении иммунной толерантности. При исследовании крови можно выявить антипанкреатические антитела и циркулирующие иммунные комплексы.
Недостатком вышеназванных теорий является то, что они выделяют одну причину развития заболевания. Согласно современным исследованиям, этиологический фактор запускает каскад иммунологических, сосудистых и метаболических процессов.
Поэтому, можно сделать вывод, что данное заболевание имеет многофакторную природу, сложные механизмы патогенеза и подвержено влиянию всех физиологических и патологических процессов, происходящих в организме человека.
Автор: Никулина Наталья Викторовна,
специально для сайта Zhkt.ru
Полезное видео о поджелудочной железе
Источник
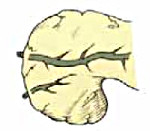
Расщепленная поджелудочная железа – порок развития, при котором на начальных этапах эмбриогенеза нарушается слияние протоковой системы органа, в результате чего основную функцию по дренированию железы берет на себя добавочный панкреатический проток. Заболевание часто не имеет клинических проявлений. При гипертензии добавочного потока может развиваться панкреатит, сопровождающийся интенсивной болью в верхних отделах живота, тошнотой, рвотой, диареей. Для установления точного диагноза проводят ЭРХПГ и МРХПГ. Бессимптомное течение болезни не требует лечения. При узком выводном отверстии панкреатического протока проводят его эндоскопическое или открытое расширение. Развитие панкреатита требует назначение диеты, спазмолитиков, ферментативных средств.
Общие сведения
Расщепленная (раздвоенная) поджелудочная железа относится к аномалиям протоковой системы, при которой доминирует добавочный (дорсальный) проток. Основной сброс секрета происходит через малый дуоденальный сосочек, а через большой сосок выводится оставшаяся часть секрета и желчь. В этом случае нарушается нормальное дренирование железы, возникает внутрипротоковая гипертензия, которая может привести к воспалению органа. Впервые заболевание подробно описано в середине ХIХ века в трудах австрийского анатома Й. Хиртля. Болезнь диагностируется у 4-11 % жителей планеты, чаще у людей европеоидной расы. Патология в равной степени встречается у лиц обоих полов. В большинстве случаев аномалия не влияет на экзокринную и эндокринную функции поджелудочной железы и не ухудшает качество жизни пациентов.
Расщепленная поджелудочная железа
Причины
Причины болезни до конца не изучены. Данная аномалия развития поджелудочной железы формируется в период закладки органа, примерно на 30-й день эмбрионального развития. На этом этапе происходит нарушение дифференцировки панкреас на хвост, тело и головку. Существует предположение о наследственной природе болезни, однако достоверных исследований по данному вопросу нет. В процессе эмбриогенеза расщепленная поджелудочная железа может возникать под влиянием следующих факторов:
- Неблагоприятные экзогенные воздействия. Тератогенным эффектом обладают различные неблагоприятные факторы внешней среды, с которыми сталкивается женщина на протяжении беременности (радиоактивное облучение, химическое загрязнение воздуха и др.). Различные патологии внутриутробного развития может вызывать курение, употребление алкоголя и наркотических веществ, постоянное нервно-психическое напряжение будущей матери.
- Инфекционные заболевания. Перенесенные беременной инфекции (краснуха, герпес, сифилис, токсоплазмоз, листериоз и др.) оказывают влияние на дифференцировку и закладку органов плода.
- Прием некоторых медикаментов. Использование женщиной лекарственных средств, противопоказанных к приему в период беременности, могут вызывать аномалии развития органов ЖКТ плода.
Патогенез
Поджелудочная железа начинает формироваться с 4-5 недели гестации из дорсального и вентрального выпячиваний дуоденальной закладки. Основные этапы дифференцировки морфологических структур органа (головки, тела, хвоста, протоковой системы) приходятся на 6-12 недели внутриутробного развития. Окончательное формирование железы заканчивается к концу беременности. В антенатальном периоде панкреатический сок преимущественно выводится по дорсальному (добавочному) протоку в малый дуоденальный сосочек, тогда как вентральный (основной) выводной канал отводит небольшую часть секрета совместно с желчью в большой дуоденальный сосок.
После рождения процесс оттока сока поджелудочной железы меняется прямо противоположно. Протоковая система взрослого человека состоит из главного (Вирсунгова) выводного канала, который собирает около 70% панкреатического секрета из дольковых протоков, проходит в толще органа от хвоста до головки, где в него впадает добавочный (Санториниев) проток. Затем основной проток сливается с общим желчным, образуя печеночно-поджелудочную ампулу, и открывается в тонкий кишечник через большой (Фатеров) дуоденальный сосок. При аномалии сращения зародышевых листков, когда объединение протоков не происходит, доминирующим каналом остается добавочный, и сброс секрета продолжается через малый дуоденальный сосочек.
Классификация
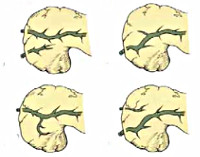
Исходя из анатомической локализации и характера расщепления, в гастроэнтерологии выделяют несколько вариантов аномалии поджелудочной железы. Существует 4 вида расщепления органа:
- Полное. Является наиболее распространённой формой болезни и встречается в 70% случаев. Основная часть секрета дренируется в малый сосочек, а оставшийся панкреатический сок вместе с желчью выходит в 12-перстную кишку через Фатеров сосок. Крайней степенью аномалии является атрофия вентрального протока, при которой в малое дуоденальное отверстие выводится весь сок поджелудочной железы, а в большое — желчь. Данная форма встречается в 20-25 % случаев и наиболее часто вызывает панкреатит ввиду длительной внутрипротоковой гипертензии.
- Неполное. Расщепленный орган разделен на две части, протоки которых на определенном участке сообщаются друг с другом, но открываются в кишку посредствам двух изолированных отверстий. Распространённость данной аномалии — 5-6 %.
- Изолированное. Происходит формирование отдельно расположенного дорсального сегмента, который выводит желчь от передней части панкреас через малый дуоденальный сосочек. Основная часть желчи дренируется по Вирсунгову протоку в большое дуоденальное отверстие.
Симптомы расщепленной поджелудочной железы
У большинства пациентов заболевание протекает бессимптомно. Несоответствие диаметра малого сосочка и количества поступающего в него панкреатического сока приводит к нарушению оттока секрета и развитию обструктивного панкреатита. Спровоцировать острое воспаление органа может прием алкоголя, чрезмерное употребление жирной, острой, копченой пищи. Возникает опоясывающая боль в верхнем отделе живота, которая иррадиирует в позвоночник и усиливается через полчаса после приема пищи. Болезненные ощущения носят острый, режущий характер и не купируются спазмолитиками. Появляются диспепсические явления: сухость во рту, отрыжка, тошнота и рвота, диарея. Воспаление может сопровождаться повышением температуры тела, отсутствием аппетита, бледностью и синюшностью кожных покровов. Возможен переход острой формы болезни в хроническую.
Осложнения
Осложнения расщепленной поджелудочной железы встречаются редко. При длительном течении хронического обструктивного панкреатита с частыми приступами обострения может возникать обтурационная желтуха вследствие холестаза, реактивный реактивный гепатит, воспалительные заболевания желчных протоков и желчного пузыря (холангиты, холециститы). Затруднение оттока панкреатического сока способствует образованию панкреатических панкреатических кист и псеводокист. При неблагоприятном течении болезни может возникать панкреосклероз или панкреонекроз. Поражение островков Лангерганса ведет к развитию сахарного диабета.
Диагностика
Ввиду частого отсутствия признаков болезни выявление врожденной аномалии затруднено. Чаще всего обнаружение расщепленной поджелудочной железы является случайной находкой при плановом обследовании или при диагностике других заболеваний. Консультация гастроэнтеролога с проведением физикального осмотра и изучением анамнеза жизни информативна только при возникновении симптомов панкреатита. Для подтверждения диагноза необходимо провести следующие инструментальные исследования:
- Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ). Данный метод помогает визуализировать протоковую систему расщепленной железы (размер, количество, строение выводных каналов). Чаще всего при введении контраста в большой сосочек определяется короткий канал, а в малый – контрастируется вся сеть протоков железы.
- Магнитно-резонансная холангиопанкреатография (МРХПГ). Наиболее современный и малоинвазивный метод, который основывается на введении контрастного вещества в панкреатические протоки и холедох при проведении МР-исследования. Позволяет определить не только количество и размеры каналов, но оценить их работу.
При развитии панкреатита выполняют УЗИ поджелудочной железы, лабораторные исследования (ОАК, биохимический анализ крови, анализ кала). Проведение дифференциальной диагностики целесообразно при появлении симптомов воспаления органа. В этом случае патологию дифференцируют с острым острым панкреатитом другой этиологии, острым острым холециститом, пищевой токсикоинфекцией, перфорацией язвы желудка или двенадцатиперстной кишки и другими заболеваниями, имеющими схожую симптоматику.
Лечение расщепленной поджелудочной железы
При отсутствии клинических проявлений данная аномалия не нуждается в лечении. Нарушение оттока панкреатического секрета ввиду узости одного из сосочков требует хирургического вмешательства. В настоящее время хирурги отдают предпочтение эндоскопическому расширению устья выводящего канала. Для улучшения оттока секрета внутрь дорсального протока устанавливают пластиковый стент. При отсутствии эффекта от эндоскопической сфинктеротомии выполняют открытую операцию, в ходе которой рассекают ткани, расположенные вокруг малого сосочка.
Развитие острого панкреатита требует назначения спазмолитических, обезболивающих, ферментативных препаратов. Особую роль играет диетическое питание, которое предполагает отказ от жирной, жареной, острой пищи. Предпочтение следует отдавать вареным и запечённым постным блюдам. Лицам с данной аномалией панкреас следует отказаться от употребления алкогольных напитков.
Прогноз и профилактика
Прогноз при заболевании, как правило, благоприятный. В редких случаях развитие осложнений (панкреонекроз, холестаз) может повлечь за собой серьезные жизнеугрожающие последствия. Профилактика заключается в ведении здорового образа жизни, отказе от вредных привычек и соблюдении основ правильно питания. Важную роль играет предотвращение возникновения воспалительных изменений органа. Пациентам с расщеплением железы следует 1-2 раза в год проходить УЗИ брюшной полости.
Источник
Панкреатит
представляет собой тяжелое заболевание
поджелудочной железы, в основе которого
лежит внутриорганная активация
продуцируемых железой пищеварительных
ферментов и выраженное в различной
степени ферментативное повреждение
ткани (панкреонекроз), с последующим
развитием фиброза, нередко распространяющееся
на окружающие ткани (парапанкреофиброз),
а также осложняемое вторичной инфекцией.
Клинически панкреатит может протекать
в острой и хронической формах, нередко
тесно связанных между собой.
Этиология.
Этиологией
возникновения хронического панкреатита
являются:
1.
Алкоголь, раздражая слизистую оболочку
12 п.к„ не только усиливает продукцию
секретина, панкреозимина, гистамина,
гастрина, а, следовательно, и внешнюю
секрецию ПЖ, но и вызывает рефлекторный
спазм сфинктера Одди, приводящий к
внутрипротоковой гипертензии. Длительное
употребление алкоголя сопровождается
дуоденитом с нарастающей атонией
сфинктера, что приводит к
дуоденопанкреатическому и
билиарнопанкреатическому рефлюксу,
особенно во время рвоты. Имеет значение
и белково-витаминная недостаточность
свойственная хроническому алкоголизму.
Некоторые авторы полагают, что алкоголь
может оказывать и прямое токсическое
воздействие на паренхиму ПЖ. Кроме того,
имеются данные, что хроническая
алкогольная интоксикация изменяет
состав панкреатического сока за счет
увеличения количества белка, лактоферрина
и снижения бикарбонатов и ингибиторов
протеаз, что способствует образованию
конкрементов.
2.
Заболевания желчного пузыря и
желчевыводящих путей, при доминировании
желчнокаменной болезни, включая и
состояние после холецистэктомии.
Сопровождающий эти заболевания
воспалительно-склеротический процесс
в дистальных отделах желчевыводящих
путей приводит к стенозу, либо
недостаточности сфинктера Одди. Спазм
или стеноз сфинктера приводят к
гипертензии в протоковой системе ПЖ и,
как следствие, выходу компонентов
панкреатического сока в паренхиму с
развитием в ней воспалительных и
склеротических изменений. Рефлюкс желчи
при этом не имеет решающего значения,
так как ХП развивается и при раздельном
впадении холедоха и вирсунгиева протока
в 12 п.к. Слизистая оболочка панкреатических
протоков в норме резистентна к действию
желчи, и только при длительной инкубации
желчи в смеси с панкреатическим секретом
или культурой бактерий желчь приобретает
повреждающее действие на ПЖ. В случае
недостаточности большого дуоденального
соска происходит рефлюкс кишечного
содержимого в протоки ПЖ с активацией
протеолитических ферментов, что в
сочетании с гипертензией и оказывает
повреждающее воздействие на паренхиму
органа.
3. Травма ПЖ, в том
числе интраоперационная, В развитии
послеоперационного панкреатита имеет
значение не только прямое воздействие
на ткань железы и ее протоки, но и
деваскуляризация ПЖ,
4.
Заболевания желудочно-кишечного тракта,
особенно 12 п.к.: отек в области Фатерова
соска, затрудняющий отток панкреатического
секрета, дуоденостаз, сопровождающийся
дуоденопанкреатическим рефлюксом;
дивертикулы 12 п.к., которые могут
приводить либо к сдавлению протоков с
последующей гипертензией, либо, в
случае открытия протока в дивертикул-
к дуоденопанкреатическому рефлюксу.
Дуоденит не только поддерживает
воспаление Фатерова соска, но и вызывает
секреторную дисфункцию ПЖ вследствие
нарушения продукции полипептидных
гормонов ЖКТ. Пенетрация язвы 12 п.к.
или желудка в ПЖ чаще приводит к очаговому
воспалительному процессу, а в ряде
случаев — к типичному хроническому
рецидивирующему панкреатиту.
5.
Одностороннее питание углеводной и
жирной пищей при недостатке белков
ведет к резкой стимуляции внешней
секреции с последующим срывом
регенераторных процессов в ПЖ.
Особенно большое значение имеет прием
алкоголя с жирной пищей.
6.
Эндокринопатии и нарушения обмена
веществ:
—
гиперпаратиреоз, который ведет к
гиперкальцисмии и кальцификации ПЖ
/кальций способствует переходу
трипсиногена в трипсин в протоках ПЖ
—
гиперлипидемия, которая ведет к жировой
инфильтрации клеток ПЖ, повреждению
сосудистой стенки, образованию тромбов,
микроэмболии сосудов;
7.
Аллергические факторы. В крови ряда
больных обнаруживаются антитела к ПЖ;
в некоторых случаях отмечается выраженная
эозинофилия (до 30-40% и более). В литературе
описаны случаи появления болевых кризов
при употреблении клубники, и развития
ХП на фоне бронхиальной астмы.
8.
Наследственные факторы. Так известно,
что у детей, родители которых страдают
ХП, повышена вероятность его развития
по аутосомно-доминантному типу.
Подчеркивается более частая встречаемость
ХП у лиц с 0(1) группой крови. В некоторых
случаях это бывает причиной так называемых
ювенильных панкреатитов.
9.
Пороки развития панкреобилиодуоденапьной
зоны: кольцевидная ПЖ, сопровождающаяся
дуоденостазом; добавочная ПЖ с различными
вариантами хода протоков, не обеспечивающими
отток секрета; энтерогенные кисты ПЖ.
10.
Лекарственные препараты: стероидные
гормоны, эстрогены, сульфаниламиды,
метилдофа, тетрациклин, сульфасалазин,
метронидазол, ряд нестероидных
противовоспалительных средств,
иммунодепрессанты, антикоагулянты,
ингибиторы холинэстеразы и другие.
11.
Неспецифический язвенный колит, болезнь
Крона, гемохроматоэ и ряд других
заболеваний, сопровождающихся
склеротическими изменениями в ПЖ без
клинической манифестации, что можно
рассматривать как неспецифическую
тканевую реакцию на токсические или
циркуляторные воздействия. В эту же
группу, вероятно, следует отнести фиброз
ПЖ при циррозах печени.
12.
Инфекционные и паразитарные болезни:
эпидемический паротит, вирусный гепатит,
инфекционный мононуклеоз, брюшной тиф,
туберкулез, сифилис, кишечные инфекции,
амебиаз и т.д., сопровождающиеся межуточным
воспалением ПЖ с последующим ее склерозом.
Патогенез.
Можно считать общепризнанным, что в
основе патогенеза панкреатита у
подавляющего большинства больных лежит
повреждение ткани железы ею же
продуцируемыми пищеварительными
ферментами. В норме эти ферменты
выделяются в неактивном состоянии
(кроме амилазы и некоторых фракций
липазы) и становятся активными лишь
после попадания в двенадцатиперстную
кишку. Большинство современных авторов
выделяют три главных патогенетических
фактора, способствующих аутоагрессии
ферментов в секретирующем их органе:
1)
затруднение оттока секрета железы в
двенадцатиперстную кишку и внутрипротоковая
гипертензия;
2)
ненормально высокие объем и ферментативная
активность сока поджелудочной железы;
3) рефлюкс в
протоковую систему поджелудочной железы
содержимого двенадцатиперстной кишки
и желчи.
Механизмы
патологической внутриорганной активации
ферментов и повреждения ткани железы
различаются в зависимости от причины
панкреатита. Так известно, что алкоголь,
особенно в больших дозах, рефлекторным
и гуморальным путем резко повышает
объем и активность панкреатического
сока. К этому дбавляется стимулирующее
действие алиментарного фактора, поскольку
алкоголики питаются нерегулярно, не
столько едят, сколько закусывают,
принимая много жирной и острой пищи.
Кроме того, алкоголь способствует спазму
сфинктера печеночно-панкреатической
ампулы (сфинктера Одди), вызывает
повышение вязкости панкреатического
секрета, образование в нем белковых
преципитатов, в дальнейшем трансформирующихся
в конкременты, характерные для хронической
формы заболевания. Все это затрудняет
отток секрета и ведет к внутрипротоковой
гипертензии, которая при уровне,
превышающем 35-40 см вод. ст., способна
обусловить повреждение клеток эпителия
протоков и ацинусов и освобождение
цитокиназ, запускающих механизм активации
ферментов. Спазм сфинктера Одди, возможно,
ведет к желчно-панкреатическому рефлюксу
и внутрипротоковой активации ферментов
за счет желчных кислот. Не исключают
также и прямое повреждающее действие
высоких концентраций алкоголя в крови
на железистые клетки.
При
панкреатите, связанном с заболеваниями
желчных путей, главным патогенетическим
фактором является нарушение оттока
панкреатического сока в двенадцатиперстную
кишку, что связано, прежде всего, с
наличием упоминавшегося «общего канала»,
то есть печеночно-панкреатической
(фатеровой) ампулы, через которую отходят
желчные конкременты и куда обычно
впадает главный панкреатический проток.
Известно, что при раздельном впадении
желчного и панкреатических протоков,
а также при отдельном впадении в
двенадцатиперстную кишку добавочного
протока, сообщающегося с главным протоком
поджелудочной железы, билиарный
панкреатит не развивается.
Проходя
через фатерову ампулу, желчные конкременты
временно задерживаются в ней, вызывая
спазм сфинктера Одди и преходящую
протоковую гипертензию, обусловливающую
ферментативное повреждение ткани железы
и, возможно, приступ острого панкреатита,
в ряде случаев протекающий малосимптомно
или же маскирующийся приступом желчной
колики. Повторное «проталкивание»
желчных камней через ампулу за счет
высокого панкреатического и билиарного
давления может привести к травме
слизистой дуоденального сосочка и
стенозирующему панпиллиту, все более
затрудняющему пассаж желчи и
панкреатического сока, а также и повторное
отхождение камней. Иногда наступает
стойкое ущемление желчного конкремента
в ампуле, ведущее к обтурациониой желтухе
и тяжелому панкреонекрозу.
Самостоятельную
роль в патогенезе панкреатита могут
играть также заболевания двенадцатиперстной
кишки, связанные с дуоденостазом и
гипертензией в ее просвете и способствующие
рефлюксу дуоденального содержимого в
панкреатический проток (в том числе
«синдром приводящей петли» после
резекции желудка по типу Бильрот П).
Некоторые авторы указывают и на значение
дивертикулов двенадцатиперстной кишки,
в особенности перипапиллярных, которые
могут обусловливать как спазм, так и
(редко) атонию сфинктера Одди.
Травматический
панкреатит может быть связан как с
прямым, так и с опосредованным воздействием
на поджелудочную железу. При прямой
травме к внутриорганной активации
ферментов ведет механическое повреждение
железы с выделением из омертвевающих
клеток уже упоминавшихся активаторов
(цитокиназ) и последующим развитием в
дополнение к травматическому еще и
ферментативного панкреонекроза. При
эндоскопических вмешательствах на
большом дуоденальном сосочке (РХПГ,
ЭПСТ) часто травмируется слизистая
оболочка фатеровой ампулы и терминального
отдела главного панкреатического
протока. В результате травмы кровоизлияний
и реактивного отека может затрудняться
отток панкреатического секрета и
развиваться протоковая гипертензия.Стенки
протока могут повреждаться и от
избыточного давления при введении
контрастного вещества при РХПГ.
При
опосредованном воздействии случайных
и операционных травм на поджелудочную
железу (травматический шок, кровопотеря,
кардиохирургические вмешательства с
длительной перфузией) повреждение
железистой ткани с высвобождением
активирующих клеточных факторов связано
в основном с микроциркуляторными
расстройствами и соответствующей
гипоксией.
Следует
обратить внимание на еще один важный
аспект патогенеза хронического
панкреатита, недостаточно освещаемый
в литературе. По представлениям
большинства клиницистов панкреонекроз
считается определяющей особенностью
наиболее тяжелых форм острого
деструктивного панкреатита. Однако
повреждение и гибель (омертвение, некроз)
ткани поджелудочной железы под
воздействием внутриорганной активации
и аутоагрессии пищеварительных ферментов
определяет возникновение и течение
любых, в том числе и хронических, форм
рассматриваемого заболевания.
При
хроническом панкреатите, не являющемся
следствием острого, также имеет место
ферментативное повреждение, некробиоз,
некроз и аутолиз панкреатоцитов,
происходящие как постепенно, под влиянием
длительно действующего фактора, так и
остро скачкообразно в период обострений
хронического процесса.
Патологическая
анатомия.
В процессе развития панкреатита в ткани
поджелудочной железы происходит
разрастание соединительной ткани, в
результате чего развивается фиброз и
склероз. В дальнейшем развиваются
обызвествление, нарушение проходимости
панкреатических протоков..
Соседние файлы в предмете Хирургия
- #
- #
- #
- #
- #
- #
- #
- #
Источник

