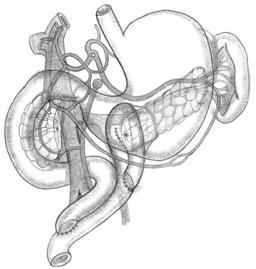
Протоковая гипертензия поджелудочной железы
Хирургическое лечение хронического осложненного панкреатита
Хронический панкреатит одно из распространенных заболеваний. Мы писали уже о хроническом панкреатите на нашем сайте. Теперь пришла очередь поговорить об осложнениях хронического панкреатита и их лечении. Сразу нужно оговориться, что лечение осложнений хронического панкреатита проводится хирургически.
К осложнениям хронического панкреатита относят:
- кисту поджелудочной железы,
- свищ поджелудочной железы,
- фиброзные изменения в головке поджелудочной железы,
- вирсунголитиаз (камни в протоках),
- панкреатическую протоковую гипертензию (повышение давления в протоках),
- инфекционные осложнения (воспалительные инфильтраты, гнойные холангиты, перитониты, септические состояния).
К внепанкреатическим осложнениям (развившимся в соседних с поджелудочной железой органах) относят:
- портальную гипертензию — повышение давления в венозной системе органов брюшной полости вследствие тромбоза или сдавления портальной (воротной) и селезеночной вен;
- билиарную гипертензию — повышение давления в желчных протоках,
- дуоденальную непроходимость — нарушение прохождения пищи по двенадцатиперстной кишке.
Киста поджелудочной железы
Кисты поджелудочной железы образуются в результате гибели ткани поджелудочной железы. Такая ситуация возникает вследствие атаки острого панкреатита или как исход такого заболевания, как панкреонекроз. Кисты поджелудочной железы могут иметь связь с главным панкреатическим протоком, в зависимости от этого выбирается метод лечения кисты поджелудочной железы. Раньше, а к сожалению и сейчас в некоторых неспециализрованных клиниках, для лечения кист поджелудочной железы применяются полостные очень травматичные операции. Суть этих операций заключается в создании сообщения между кистой поджелудочной железы и каким -либо полым органом (желудок, тонкая кишка). Эти операции имеют большое количество осложнений и неудовлетворительных результатов. Все это подтолкнуло ученых к разработке новых методов лечения кист поджелудочной железы. В настоящее время лечение проводится без полостных операций с применением ультразвуковой и эндоскопической техники.
По мере накопления опыта малоивазивного (без полостных операций) лечения отработаны современные методики лечения панкреатических кист:
- наружное дренирование – чрескожное наружное дренирование кисты под ультразвуковым контролем
- внутреннее дренирование – формирование цистогастроанастомоза (сообщения между кистой и желудком) под эндоскопическим, ультразвуковым и рентгенологическим контролем.
- пункционный метод – повторные пункции кисты под ультразвуковым контролем (проколы через кожу с удалением содержимого) с введением различных жидкостей, вызывающих склерозирование (склеивание полости) кисты.
Ранее применявшиеся аналогичные методы наружного и внутреннего дренирования при помощи лапаротомии (разреза брюшной стенки) уходят в историю и в специализированных центрах, как правило, не используются.
Операции внутреннего дренирования наряду с минимальной травматичностью имеют следующие недостатки:
- проникновение инфекции в полость кисты с нагноением,
- аррозивные кровотечения,
- рубцевание соустья с рецидивированием (повторным образованием) кисты.
Рубцевание происходит из-за того, что соединяются разнородные ткани организма.
Пункционному лечению подлежат кисты, не имеющие сообщения с главным панкреатическим протоком. При пункционном склерозировании кисты может возникнуть обострение панкреатита и панкреонекроз (омертвение участка поджелудочной железы — очень тяжелое состояние).
Оптимальным методом малоинвазивного лечения кист поджелудочной железы является чрескожное наружное дренирование под ультразвуковым контролем. Операции подлежат кисты более 3 см в диаметре. При этом при помощи ультразвукового аппарата через прокол кожи под наркозом в кисту вводится тонкая дренажная трубка. Содержимое кисты удаляется и проводится его цитологический (клеточный) и биохимический анализ. Далее через дренаж вводится контрастный препарат и определяется связь кисты с главным панкреатическим протоком, выполняется эндоскопическая папиллотомия (эндоскопическое рассечение большого дуоденального сосочка места впадения протока поджелудочной железы в кишку) для улучшения оттока панкреатического сока в двенадцатиперстную кишку. В результате проводимого лечения кисты, несвязанные с главным панкреатическим протоком, излечиваются и дренажная трубка после прекращения выделения панкреатического сока удаляется.
Если киста связана с главным панкреатическим протоком и сокоотделение по трубке продолжается, то образуется наружный искусственный панкреатический свищ (см. далее). Образование наружного свища благотворно сказывается на течении хронического панкреатита, так как ликвидируется повышенное давление в протоках поджелудочной железы, устраняется болевой синдром, уменьшается воспаление.
Хирургическое лечение свищей поджелудочной железы
В специализированных клиниках возможно малоинвазивное (без полостной операции) лечение наружных панкреатических свищей под ультразвуковым и рентгенологическим контролем – формирование фистулогастрооанастомозов (сообщение свища с желудком), но данный метод имеет ограничения, не физиологичен и не всегда радикален.
Для хирургического лечения наружных панкреатических свищей применяют различные дренирующие операции. Наиболее оптимальной мы считаем медиальную (срединную) резекцию поджелудочной железы с формированием надежного физиологичного концевопетлевого панкреатоэнтероанастомоза. Операция разработана выдающимся отечественным хирургом проф. В.И. Оноприевым и его учениками. Операция заключается в выделении свищевого хода до устья, которым является главный панкреатический проток на уровне перешейка или тела поджелудочной железы. Далее железа поперечно пересекается по перешейку и формируется концевопетлевой панкреатоэнтероанастомоз (сообщение между главным панкреатическим протоком и кишкой). При этом соустье не рубцуется и панкреатический сок беспрепятственно поступает в кишечник, участвуя в пищеварении.
Хирургическое лечение «головчатого» панкреатита
Резекции поджелудочной железы. В настоящее время при хроническом панкреатите с воспалительным инфильтратом в головке поджелудочной железы (фибропластический панкреатит, «головчатый» панкреатит) используются дуоденумохраняющие резекции головки поджелудочной железы (резекции поджелудочной железы с сохранением двенадцатиперстной кишки).
Предложены различные варианты резекции головки поджелудочной железы по H.G.Beger и Ch.F.Frey.
Операция Frey получила наибольшее распространение в США. Операция весьма эффективна при лечении хронического панкреатита, но обладает многими недостатками. Небольшой объем резекции (всего 5-6 г) головки ограничивает возможности операции по лечению осложнений хронического панкреатита, таких как механическая желтуха в результате сужения внутрипанкреатического отдела общего желчного протока ипортальная гипертензия. Значительный объем оставляемой ткани головки поджелудочной железы не исключает продолжения воспалительного процесса в оставшейся ткани головки.
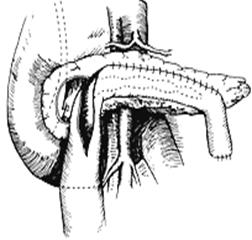
Рис. 2. Этапы панкреатоеюностомии по Frey [C.F.Frey, 1995].
Операция H.Beger предполагает обширную резекцию головки поджелудочной железы, это определяет большую радикальность операции Beger, так как обширная резекция головки поджелудочной железы позволяет ликвидировать воспалительный процесс, предотвратить развитие осложнений хронического панкреатита и добиться хороших отдаленных результатов.
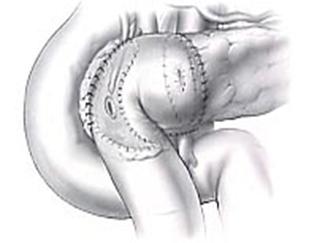
Рис.3. Реконструктивный этап дуоденумсохраняющей резекции головки поджелудочной железы [H.G.Веgег et al., 2002].
Отечественные хирурги тоже внесли вклад в лечение головчатого панкреатита. В нашей клинике применяется методика, разработанная авторским коллективом Российского центра функциональной хирургической гастроэнтерологии проф. Оноприевым В.И. и Рогаль М.Л.
Рис. 4. Вид гастропанкреатодуоденального комплекса после дуоденумсохраняющей резекции головки поджелудочной железы.
В наиболее тяжелых случаях хронического панкреатита выполняется пилоросохраняющая панкреатодуоденальная резекция, когда полностью удаляется головка поджелудочной железы, двенадцатиперстная кишка, часть желчного протока.
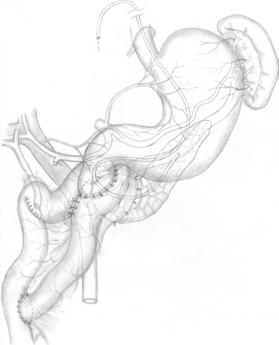
Рис. 5. Вид гастропанкреатодуоденального комплекса после панкреатодуоденальной резекции (В.И.Оноприев с соавт., (1982).
Лечение панкреатической протоковой гипертензии
Надо сказать, что протоковая гипертензия наиболее частая причина болей при хроническом панкреатите.
Операции внутреннего дренирования протоков – способ снижения повышенного давления в протоках поджелудочной железы, позволяющий ликвидировать связанный с этой причиной болевой синдром.
Оперативное снижение давления в панкреатических протоках у больных ХП с 17 до 7 – 10 мм рт.ст. избавляет пациентов от болей. Вовремя проведенная дренирующая операция позволяет затормозить прогрессирование панкреатита, добиться стабилизации в течение заболевания.
Внутреннее дренирование более оправдано при сохраненной в той или иной степени функции железы, при отсутствии инсулинпотребного сахарного диабета; операция оказывается тем эффективнее, чем более полноценна разгрузка протоковой системы.
За более чем вековую историю хирургии хронического панкреатита разработаны разнообразные варианты операций, дренирующих протоки поджелудочной железы. Большинство из них имеют историческое значение и полностью оставлены по различным причинам.
Среди малоинвазивных методик применяются эндоскопическая папилловирсунготомия и эндоскопическое стентирование вирсунгова протока.
Эндоскопическая папилловирсунготомия – под наркозом производится эндоскопическое рассечение большого дуоденального сосочка и выходного отдела главного панкреатического протока. Эта методика выполняется как пробное лечение осложненного панкреатита и снижает давление только в случае заболеваний сосочка (папиллит, аденомиоз, невыраженных стриктурах (сужениях) выходного отдела главного панкреатического протока).
Эндоскопическое стентирование вирсунгова протока применяется при продленных стриктурах (сужениях) выходного отдела главного панкреатического протока – под наркозом производится бужирование (расширение) суженного участка протока, затем в него устанавливается стент (специальная дренажная трубочка). Таким образом отток панкреатического сока восстанавливается и боль ликвидируется.
Если малоинвазивными вмешательствами не удается ликвидировать повышенное давление в протоках, то выполняются полостные операции на поджелудочной железе.
В настоящее время наиболее распространенным дренирующим вмешательством является продольная панкреатоеюностомия (анастомоз между продольно рассеченным протоком поджелудочной железы и тощей кишкой) в модификациях различных авторов. При этом удается максимально сохранить инсулярную и ацинарную ткань железы, предотвратить развитие сахарного диабета, улучшить перевариваемость пищи.
Для выполнения данного анастомоза диаметр протока поджелудочной железы должен превышать 5мм.
Этот способ хирургического лечения имеет недостатки:
- данный тип анастомоза склонен к рубцеванию, что приводит к возобновлению болей;
- формируется широкая камера анастомоза, в которую открываются сегментарные протоки поджелудочной железы, в связи этим происходит беспрепятственный рефлюкс (заброс) кишечного содержимого в протоки поджелудочной железы и прогрессирование панкреатита;
- при малом диаметре главного панкреатического протока возникает необходимость в корытообразном иссечении передней поверхности поджелудочной железы, при этом при анастомозировании нарушается отток из сегментарных протоков;
- не ликвидируется портальная гипертензия (повышенное давление в венозной системе брюшной полости).
Органосохраняющая технология ликвидации протоковой панкреатической гипертензии разработанная проф. В.И.Оноприевым, д.м.н. М.Л.Рогалем, к.м.н. Макаренко А.В. защищена патентами Российской Федерации (В.И.Оноприев с соавт., 2003; А.В.Макаренко, 2005) и включена в реестр высокотехнологичной хирургической помощи.
На реконструктивном этапе применяется надежный концевопетлевой панкреатоэнтероанастомоз.
Во время операции поджелудочная железа полностью пересекается на уровне перешейка (производится медиальная резекция), удаляются нефиксированные камни из протоков, образовавшиеся половинки железы анастомозируются (сшиваются) с тощей кишкой – таким образом формируется билатеральный (двухсторонний) концевопетлевой панкреатоэнтероанастомоз.
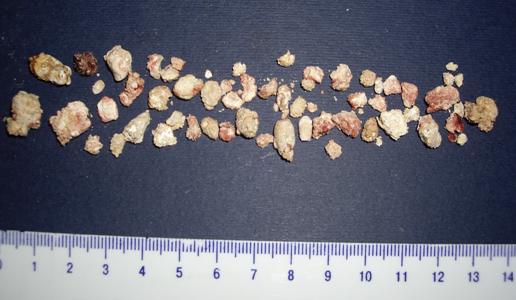
Фото 2. Камни, удаленные во время медиальной резекции поджелудочной железы, у пациентки с наследственным калькулезным панкреатитом.
К преимуществам такой методики относится:
- анастомозы не рубцуются, так как сшиваются однородные ткани — слизистые кишки и панкреатического протока,
- складки слизистой кишки вокруг анастомозов предотвращают рефлюкс (заброс) кишечного содержимого в протоки поджелудочной железы,
- срезы поджелудочной железы циркулярно перитонизированы (обернуты и защищены) петлей тощей кишки и погружены в ее просвет, что гарантирует высокую надежность анастомоза,
- операция выполнима при любом диаметре главного панкреатического протока,
- ликвидация портальной гипертензии (повышенного венозного давления в органах брюшной полости) путем освобождения из фиброзных сращений воротной и селезеночной вен.
Хорошие клинические и функциональные результаты, полученные у более чем 40 пациентов, оперированных по данной методике (А.В.Макаренко, 2005), определили данное вмешательство, как операцию выбора в ликвидации панкреатической протоковой и портальной гипертензии.
Лечение осложнений хронического панкреатита остается одной из самых сложных проблем современной хирургической гастроэнтерологии. Однако успехи отечественных и зарубежных хирургов позволяют с успехом лечить таких пациентов с хорошим функциональным результатом. Главное обратиться за помощью вовремя и обязательно в специализированную клинику.
к.м.н. Макаренко А.В.
Задать вопросы автору Вы можете по тел. 89615172073
Источник
Гидравлические теории (теории обструкции протоков поджелудочной железы)
Теория общего протока (common channel) была предложена Е, Opie (1901) после обнаружения им конкремента в фатеровом соске у пациента, умершего от ОП. Автор предположил, что анатомическая близость мест впадения жёлчного и панкреатического протоков в ДПК может приводить к рефлюксу жёлчи в ГПП и повреждению ПЖ детергентами, содержащимися в жёлчи.
Теория была воспринята неоднозначно. Во-первых, в большинстве случаев камень блокирует оба протока. Во-вторых, давление в ГПП выше, чем в общем жёлчном протоке. В обоих случаях рефлюкс жёлчи в ГПП не должен происходить.
В-третьих, существующее предположение, что для развития ХП необходимы патологические изменения самой жёлчи (например, значительное содержание в жёлчи продуктов перекисного окисления липидов при холелитиазе, придающей ей особые агрессивные свойства при рефлюксе в ГПП) до сих пор не подтверждено. Наиболее вероятно, что билиарные конкременты блокируют только ГПП, что приводит к протоковой гипертензии и развитию ОП либо, при длительной неполной обструкции, — к развитию ХП.
Частичная обструкция панкреатических протоков в экспериментах на собаках, крысах и свиньях приводит к повреждениям панкреатической паренхимы, весьма похожим на те, которые наблюдают при ХП у человека.
Хроническое злоупотребление алкоголем утяжеляет повреждения ПЖ, ускоряет их начало и способствует их необратимости. В дальнейших экспериментальных исследованиях было обнаружено следующее:
• продолжительность обструкции протоков прямо коррелирует с тяжестью повреждений ПЖ;
• протоковая обструкция потенцирует развитие конкрементов в протоковой системе у половины экспериментальных животных;
Таким образом, большинство авторов представляют реализацию множества этиологических факторов в патогенезе ХП аналогично тому, как это происходит в эксперименте при блоке панкреатических протоков. Действительно, панкреатостаз облегчает осаждение кристаллов кальция в протоковой системе ПЖ с последующей кальцификацией белкового секрета, развитием вторичного блока и ухудшением обструкции.
В присутствии литогенных факторов (алкоголь, курени) либо у больных с наследственной предрасположенностью (наследственный панкреатит) процесс прогрессирования ХП может быть ускорен. Характерно раннее начало кальцификапии, развитие внешнесекреторной и инкреторной недостаточности ПЖ.
При наличии мутаций гена CFTR у больных с ХП заболевание прогрессирует на фоне блокады протоков различного порядка слизистыми пробками в результате сгущения секрета.
Классический и наиболее известный пример разновидности гидравлической теории «малых протоков» — теория Н. Sarles (теория интрадуктального литиаза или нарушенной секреции). Так, алкоголь способствует повышению содержания белка и увеличению вязкости панкреатического секрета. В этих условиях происходит преципитация белка во внутридольковых или вставочных протоках.
Образовавшиеся камни (бляшки), содержащие различные протеины (ферменты), гликопротеиды, кислые мукополисахариды, заполняют протоки. Развивается обструкция внутридольковых или вставочных протоков с последующим повреждением эпителия, его атрофией, развитием локального стеноза или образованием фиброзных рубцов.
Затем в ткани, дренируемой повреждёнными протоками, возникают паренхиматозные изменения (кистозное перерождение или атрофия ацинарных долек). В конечном итоге прогрессирующий фиброз, начавшийся вокруг протока, распространяется на всю дольку, вызывает замещение ацинарной ткани и приводит к хроническому кальцифицирующему панкреатиту. Данные о том, что бляшки преимущественно состоят из десквамированного эпителия, а не протеинов, отчасти опровергают эту теорию.
Итак, недостаточный отток панкреатического сока в сочетании с повышением концентрации белка и вязкости секрета приводит к преципитации белка с образованием «белковых пробок», которые вызывают частичную или полную закупорку различных отделов панкреатических протоков.
Как известно, теория соотношения некроза и фиброза была сформулирована в 1946 г. M.W. Comfort и соавт. В соответствии с ней образующиеся при ОП воспалительные медиаторы вызывают некроз ПЖ. В дальнейшем, по мере подключения иммунных механизмов, нарушения окислительных процессов и развития ишемии, процесс становится персистирующим (хроническим) и приводит к фиброзным изменениям в ПЖ.
M.W. Comfort и соавт., выдвигая собственную теорию, в большей степени опирались на гипотезу Н. Chiari, который ещё в 1896 г. предложил рассматривать ОП как комплекс клинических признаков, развившихся вследствие самопереваривания ПЖ (разрушения ткани ПЖ её собственными пищеварительными ферментами). Итак, трипсиноген, химотрипсиноген, проэластаза и профосфолипаза А под действием различных факторов (эндо- и экзотоксинов, инфекционных агентов, ишемии, прямой травмы и др.
Повреждение ацинарных клеток приводит к дальнейшему высвобождению зимогенов, которые также каскадно активируются. Кроме того, активация и высвобождение медиаторов воспаления усугубляет отёк. Таким образом, последовательно происходят события, кульминацией которых служит развитие острого некротизирующего панкреатита.
При благоприятном исходе формируется фиброз, свойственный уже ХП. Несмотря на то что в настоящее время механизм интрапанкреатической активации трипсина детально не установлен, именно несвоевременную активацию трипсина считают инициирующим моментом в патогенезе ОП.
Теория о первично- и вторично-рецидивирующих формах ХП — комбинация из всех вышеуказанных теорий. С рядом её положений можно не соглашаться, но в ней предпринят принципиально верный подход — совершён анализ современных теорий патогенеза ХП. Все противоречия разведены в две принципиально различные формы ХП, в каждой из которых удалось объединить универсальные патологические механизмы. Выделяют две клинические формы заболевания, каждой из которых свойственны различные патогенетические особенности.
9. Сцинтиграфия, совмещенная с тестом Дебрея
визуализировали | у | отток | Амилнитрит и |
Дуодено-панкреатический рефлюкс
Полагают, что начальный этап развития панкреатита — нарушение взаимоотношений между панкреатической секрецией, давлением в ГПП и ДПК. Повышение давления в просвете ДПК приводит к рефлюксу её содержимого в ГПП с последующей активацией в нём протеаз, что может послужить толчком к развитию ОП. В эксперименте ОП вызывали путём образования петли Пфеффера из ДПК, внутрипросветное давление в которой превышает таковое в ГПП.
Вследствие этого возникает рефлюкс дуоденального содержимого в проток. В физиологических условиях у собак во время третьей фазы межпищеварительного комплекса и после кормления давление в ДПК может превышать таковое в протоке ПЖ. В это время небольшое количество (менее 1%) дуоденального содержимого забрасывается в панкреатический проток.
Таким образом, хотя потенциальная возможность возникновения ОП в физиологических условиях существует, рефлюкс очень непродолжителен, незначителен по объёму, и неизвестно, происходит ли при этом внутрипротоковая активация протеаз. Кроме того, на протяжении большей части времени сфинктер панкреатического протока эффективно предотвращает рефлюкс дуоденального содержимого в ГПП.
Однако если давление в ДПК значительно или на протяжении длительного периода (большое количество пищи, дуодсностаз, динамическая кишечная непроходимость и др.) превышает таковое в ГПП (рвота), то возникновение рефлюкса и активация протеаз более вероятны, особенно при совпадении времени повышения секреции панкреатических ферментов с рефлюксом.
В подобной ситуации одновременное нарушение взаимоотношений между давлением в ДПК, давлением в ГПП и секреторной активностью ПЖ может служить фактором, предрасполагающим к ОП. Увеличение внутрибрюшного давления на 1 мм рт.ст. способствует повышению риска развития тяжёлого ОП в 2,23 раза. Существует корреляционная связь между уровнем внутрибрюшного давления и тяжестью панкреатита, развитием бактериальных осложнений и летальных исходов.
10. Ультразвуковое исследование пж
Уменьшение | Структура ПЖ | Чередование зон | Кальцинаты ПЖ | Кисты ПЖ | ||||
Ультразвуковое | ||||||||
После жирной | выделяется ХЦК | расслабляется | диаметр общего | увеличивается | ||||
Увеличение | Признак ГСО | |||||||
Внутрипротоковая | ||||||||
ультразвуковой | ||||||||
11. Чрезкожная
пункционная биопсия ПЖ
под контролем КТ и УЗИ
Литостатиновая теория
Открытие на рубеже 90-х гг. прошлого века белка панкреатических камней — литостатина, обнаруженного в панкреатическом соке и конкрементах ПЖ, привлекло внимание многих научных групп, занимающимися проблемами обструктивных (на фоне панкреатолитиаза) и кальцифицирующих панкреатитов. Этот интерес был обусловлен выдвинутой гипотезой о способности литостатина ингибировать образование нерастворимых солей кальция в среде, перенасыщенной последним.
Один из основных фактов, положенных в основу гипотезы — обнаружение сниженных концентраций литостатина в панкреатическом соке у больных с алкогольным ХП и некоторых пациентов с неалкогольным ХП. С учётом того, что панкреатическая жидкость в норме содержит значительное количество кальция и бикарбонатов (а для ХП как раз характерна гиперсскреция кальция), вполне логично предположение, что дефицит литостатина может играть важную роль в образовании конкрементов и кальцификации ПЖ.
Поскольку литостатин рассматривают как один из стабилизаторов кальция, т.е. в качестве субстрата, поддерживающего кальций в растворимом состоянии, основную роль литостатина связывают с ингибированием нуклеации, агрегации и образования кристаллов солей кальция.
Литостатиновую теорию можно рассматривать как модификацию рассмотренной выше теории малых протоков Н. Sarles (теория интрадуктального литиаза).
Ни одно из множества проведённых исследований не смогло ясно оценить функцию или механизм действия литостатина, поэтому понятна волна интереса, возникшая при открытии панкреатит-ассоциированного белка, который синтезирует и секретирует ПЖ. По своей аминокислотной последовательности он весьма близок к литостатину (идентичность — 43%, подобие — 54%) и соответствует основным особенностям лектинов.
К настоящему моменту не обнаружено ни одной публикации, в которой было бы представлено интибирующее влияние панкреатит-ассоциированного белка на кристаллообразование или рост кристаллов кальция. Его функция остаётся неизвестной, хотя доказано, что секреция литостатина и панкреатит-ассоциированного белка увеличивается в ответ на негативное воздействие на ПЖ.
12. Лапароскопия с прицельной биопсией
Лечение пакреатита
стол | механическое | |
Прием пищи 5-6 раз | малыми порциями | гипокалорийная |
ЛЕЧЕНИЕ В ПЕРИОД
ВЫРАЖЕННОГО ОБОСТРЕНИЯ
Голод | прием |
холод на эпигастрий | аспирация через |
1.Периферические м-холинолитики
Атропин | 1 мл 0,1% раствора | 2-3 раза в день | побочные |
Метацин | 1 мл 0,1% раствора | 2-3 раза в день | |
Платифиллин | 1 мл 0,2% раствора | 2-3 раза в день | |
Пробантин | в таблетках по | 3-4 раза в день | |
Хлорозил | по 4 мг (2 табл.) | 3-4 раза в день | |
Гастроцепин | — | 2-3 раза в день | без побочных |
Первично-рецидивирующая форма (первый тип) иронического панкреатита
Воспалительный процесс (подобно ОП) начинается в паренхиме с интраацинарной активации трипсина из трипсиногена. Порции трипсина, высвобождающиеся при этом из ацинарных клеток, активируют новые молекулы трипсиногена; возникает цепная реакция. Повышение активности трипсина в крови стимулирует нейтрофилы, которые первыми устремляются в очаг воспаления.
Выделяемые ими оксиданты и лизосомальные ферменты оказывают на клеточные элементы и соединительную ткань цитотоксическое и деструктивное воздействие. Активируется процесс перекисного окисления липидов клеточных, митохондриальных, микросомальных мембран с нарушением их целостности и проницаемости и высвобождением из ацинарных клеток в окружающие ткани и кровь протсолитических пищеварительных и лизосомальных ферментов. Последние, обладая агрессивными свойствами, активно включаются в механизм воспаления (повреждения) тканей ПЖ.
Снижение активности антиоксидантов связано с их расходованием на нейтрализацию свободных радикалов и деструктивным влиянием на них лизосомальных ферментов, что приводит к развитию оксидативного стресса. В очаге воспаления происходит накопление мононуктеарных фагоцитов с выделением фибронектина, что знаменует собой переход острого воспалительного процесса в ПЖ в фазу репаративной регенерации с развитием фиброзных изменений.
Итак, обострение первично-рецидивирующей формы ХП происходит вследствие активации (самоактивации) находящихся в очаге хронического воспаления мононуклеарных фагоцитов с высвобождением ИЛ-8 — хемоаттрактанта и стимулятора продукции оксидантов нейтрофилами. Последние, концентрируясь в очаге хронического воспаления, вызывают рецидив заболевания. Цитокиновый механизм обострения считают альтернативным механизмом интраацинарной активации трипсина из трипсиногена.
2. Миотропные спазмолитики
Папаверин | 2 | 2-4 раза в день |
Но-шпа | 2-4 | 2-4 раза в день |
Феникаберан | 2 | 2-4 раза в день |
3. Ненаркотические
анальгетики
при | |||
Анальгин | 2 | 2-3 раза в день | |
Баралгин | 5 мл внутримышечно | 2-3 раза в день | |
4.Антигистаминные
препараты
Фенкорол | по 0,025 г внутрь | 3 раза в день | |
Димедрол | 1 | 0,025–0,05 г внутрь | 2-3 раза в день |
Диазолин | по 0,05 г внутрь | 3 раза в день | |
Супрастин | 1 мл 2% раствора | 0,025 г внутрь | 2-3 раза в день |
5. Анестетики
Новокаин | 100 мл 0,25% раствора |
6. Спазмолитики,
устраняющие спазм сфинктера Одди
Эуфиллин | 10 мл 2,4% р-р в 10-20 | ||
Нитроглицерин | по 0,0005 г под язык | ||
7. Наркотические
анальгетики
Промедол | 1 мл 1-2% раствора | Обезболивает, | |
Морфин вызывает | Протвопоказан | ||
8. Нейролептаналгезия
Фентанил | 1-2 мл 0,005% раствора | наркотический |
Дроперидол | 1-2 мл 0,25% раствора | нейролептик |
Подавление секреции
поджелудочной железы
9. БлокаторыН-2-гистаминовых
рецепторов
циметидин | ранисан | ранитидин |
10. Блокаторы
“протоновой помпы”
Подавление
активности ферментов поджелудочной
железы
11. Естественные | ||
Трасилол | не менее 100 000 ЕД | В/в |
Контрикал | 20 000 – 40 000 ЕД/ | |
Гордокс | не менее 50 000 ЕД | |
Апротинин | не менее 50 000 ЕД | |
Фой | по 0,1 г | |
-аминокапроновая | 5% р-р по 150-200,0 мл | 10-12 дней |
Вторично-рецидивирующая форма (второй тип) хронического панкреатита
Воспалительный процесс длительное время персистирует в интерстициальной ткани ПЖ (подобно хроническим интерстициальным воспалительным заболеваниям лёгких) при активном участии мононуклеарных фагоцитов и незначительном участии полинуклеарных фагоцитов. Инициацию воспаления осуществляют иммунные комплексы, вырабатывающиеся на неизвестные антигены и имеющие сродство к ткани ПЖ.
Взаимодействуя с Fc-рецепторами мононуклеарных фагоцитов, они стимулируют выделение из их цитоплазмы цитокинов и различных медиаторов, повреждающих паренхиму (оксиданты), активирующих фибробласты (фибронектин) и усиливающих фиброгенез. У больных эта фаза воспаления протекает латентно, без выраженных клинических симптомов, т.е.
соответствует хроническому моноцитарно-инфильтративному (первично-хроническому) воспалению. На определённом этапе латентного течения, вследствие инициации мононуклеарных фагоцитов иммунными комплексами или самоактивации, интенсивно выделяется ИЛ-8, обладающий хемотаксическим и стимулирующим нейтрофилы действием.
При этом нейтрофилы проникают в зону мононуктеарной инфильтрации (в очаг хронического воспаления ПЖ) и, благодаря выделению активных медиаторов воспаления (оксиданты, лизосомальные ферменты, миелопероксидаза), вызывают обострение. Момент вовлечения в иоспаление паренхимы ПЖ знаменует переход латентной формы в клиническую.
Распространённый фиброз ПЖ и атрофия её паренхимы ограничивают развитие высокой активности перекисного окисления липидов и объём высвобождающегося их ацинарных клеток трипсиногена. И в период обострения, и в фазу ремиссии происходит выделение мононуклеарными фагоцитами фибронектина, а следовательно, фиброзирующий процесс в ПЖ не прекращается.
Маев И.В., Кучерявый Ю.А.
Источник