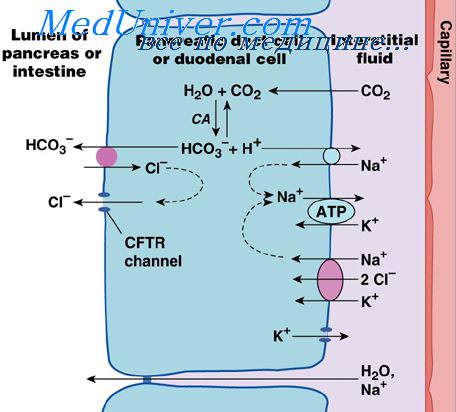
Регулирование секреции поджелудочной железы
Регуляция секреции поджелудочной железы. Этапы панкреатической секрецииПоявление панкреатической секреции обусловлено тремя важными основными стимулами. Первые два стимула (ацетилхолин и холецистокинин) стимулируют ацинарные клетки поджелудочной железы, вызывая продукцию большого количества панкреатических пищеварительных ферментов и, соответственно, небольших количеств воды и электролитов, сопутствующих ферментам. Без воды большинство ферментов временно сохраняются в ацинусах и протоках до тех пор, пока не образуется более жидкий секрет, который может поступить в двенадцатиперстную кишку. Секретин в противоположность первым двум основным стимулам вызывает секрецию эпителием протоков поджелудочной железы большого количества водного раствора бикарбоната натрия. Усиливающие эффекты различных стимулов. Когда различные стимулы панкреатической секреции возникают одновременно, общая секреция гораздо больше, чем сумма секретов, вызванных каждым из них по отдельности, поэтому говорят, что разные стимулы усиливают друг друга. Таким образом, панкреатическая секреция является обычно результатом действия не одного, а комбинированных влияний перемноженных основных стимулов.
Фазы панкреатической секрецииПанкреатическая секреция аналогично желудочной секреции проходит три фазы: мозговую, желудочную и кишечную. В течение желудочной фазы продолжается нервная стимуляция ферментной секреции, составляя еще другие 5-10% панкреатических ферментов, выделяемых после приема пищи. Но опять только малые количества достигают двенадцатиперстной кишки из-за продолжающегося недостатка значимой секреции жидкости. Кишечная фаза. После того, как химус покидает желудок и поступает в тонкий кишечник, панкреатическая секреция становится обильной, главным образом в ответ на гормон секретин. Секретин стимулирует секрецию значительного количества ионов бикарбоната. Нейтрализация кислого химуса из желудка. Секретин представляет собой полипептид, содержащий 27 аминокислот (молекулярная масса около 3400). Он присутствует в слизистой двенадцатиперстной кишки и тощей кишки в неактивной форме просекретина в так называемых S-клетках. Когда кислый химус с рН менее 4,5-5,0 поступает в двенадцатиперстную кишку из желудка, это вызывает выделение дуоденальный слизи и активацию секретина, который затем абсорбируется в кровь. Единственной действительно важной составляющей химуса является соляная кислота желудка, которая вызывает выброс секретина. Секретин, в свою очередь, вызывает секрецию поджелудочной железой большого количества жидкости, содержащей высокую концентрацию иона бикарбоната (вплоть до 145 мэкв/л), но низкую концентрацию ионов хлора. Механизм образования секретина является особенно важным по двум причинам: (1) секретин начинает высвобождаться из слизистой тонкого кишечника, когда рН дуоденального содержимого падает ниже 4,5-5,0; (2) выброс секретина резко увеличивается, когда рН падает до 3,0. Это немедленно вызывает обильную секрецию панкреатического сока, содержащего существенное количество бикарбоната натрия. Конечным итогом является следующая реакция в двенадцатиперстной кишке: Затем угольная кислота немедленно диссоциирует на двуокись углерода и воду. Углекислый газ абсорбируется в кровь и выводится через легкие, оставляя нейтральный раствор хлорида натрия в двенадцатиперстной кишке. Таким способом немедленно нейтрализуется кислое содержимое, опорожняющееся в двенадцатиперстную кишку из желудка. Слизистая тонкой кишки не может противостоять переваривающему действию кислого желудочного сока, и это является существенным защитным механизмом, предотвращающим развитие дуоденальных язв. Секреция иона бикарбоната поджелудочной железой обеспечивает подходящий рН для работы панкреатических пищеварительных ферментов, действие которых оптимально в слабощелочной или нейтральной среде при рН от 7,0 до 8,0. К счастью, рН секреции натрия бикарбоната в среднем равняется 8,0. Холецистокинин и его вклад в регуляцию секреции пищеварительных ферментов поджелудочной железы. Присутствие пищи в верхнем отделе тонкого кишечника вызывает также выделение из I-клеток, находящихся в слизистой двенадцатиперстной кишки и верхней части тощей кишки, второго гормона — холецистокинина. Это полипептид, содержащий 33 аминокислоты. Такое выделение холецистокинина происходит в результате присутствия протеоз, пептонов (продуктов частичного переваривания белков) и длинноцепочечных жирных кислот в химусе, поступающем из желудка. Холецистокинин, как и секретин, с кровью доставляется к поджелудочной железе, но вместо стимуляции секреции бикарбоната натрия обусловливает преимущественное выделение ацинарными клетками пищеварительных ферментов, причем в больших количествах. Этот эффект подобен тому, который вызывает вагусная стимуляция, но только он более выраженный и составляет от 70 до 80% общей панкреатической секреции ферментов после приема пищи. Различия между эффектами панкреатической стимуляции секретином и холецистокинином показаны на рисунке, который демонстрирует: (1) интенсивную секрецию бикарбоната натрия в ответ на кислоту в двенадцатиперстной кишке, стимулированную секретином; (2) двоякий эффект в ответ на жир (мыла); (3) сильную пищеварительную секрецию ферментов, вызванную холецистокинином (когда пептоны поступают в двенадцатиперстную кишку). — Также рекомендуем «Физиология секреции желчи. Физиологическая анатомия секреции желчи» Оглавление темы «Пищеварительные соки. Переваривание углеводов, белков, жиров»: |
Источник
Регуляция поджелудочной экзокринной секреции осуществляется нервными и гуморальными механизмами. Блуждающий нерв усиливает секрецию поджелудочной железы. Симпатические нервы уменьшают количество секрета, но усиливают синтез органических веществ (бета-адренергический эффект). Снижение секреции происходит также и за счет уменьшения кровоснабжения поджелудочной железы путем сужения кровеносных сосудов (альфа-адренергический эффект). Напряженная физическая и умственная работа, боль, сон вызывают торможение секреции. Гастроинтестинальные гормоны, секретин и ХЦК-ПЗ усиливают секрецию поджелудочного сока. Секретин стимулирует выделение сока, богатого бикарбонатами, ХЦК-ПЗ — богатого ферментами. Секрецию поджелудочной железы усиливают гастрин, серотонин, бомбезин, инсулин, соли желчных кислот. Химоденин стимулирует секрецию химотрипсиногена. Тормозящее действие оказывают ЖИП, ПП, глюкагон, кальцитонин, соматостатин, энкефалин.
Пищеварение в 12-п кишке:
Пищеварения в двенадцатиперстной кишке проходит в два этапа: сначала происходит активация ферментов: трипсиноген под действием фермента кишечного сока энтерокиназы переходит в активный трипсин, который в свою очередь активирует химотрипсиноген. На втором этапе происходят процессы пищеварения.
В 12-п кишке продолжается процесс гидролиза пищ в-в. В полость кишки выд-ся соки поджелудочной кишечных желез, содерж-е ферменты для гидролиза БЖУ. Щелочная среда.
10. Роль печени в пищеварении. Регуляция образования желчи, выделения ее в двенадцатиперстную кишку. Желчно-кишечный кругооборот желчных кислот. Пищеварение в двенадцатиперстной кишке.
Печень принимает участие благодаря желчи, кот поступает из общего протока в полость 12-п кишки.
Регуляция желчеобразования. Желчеобразование осуществляется непрерывно, но интенсивность его изменяется за счет регуляторных влияний. Усиливают желчеобразование акт еды, принятая пища. Рефлекторно изменяется желчеобразование при раздражении интероцепторов пищеварительного тракта, других внутренних органов и условнорефлекторном воздействии.
Парасимпатические холинергические нервные волокна (воздействия) усиливают, а симпатические адренергические — снижают желчеобразование. Имеются экспериментальные данные об усилении желчеобразования под влиянием симпатической стимуляции.
Желчевыделение. Движение желчи в желчевыделительном аппарате обусловлено разностью давления в его частях и в двенадцатиперстной кишке, состоянием сфинктеров внепеченочных желчных путей. В них выделяют следующие сфинктеры: в месте слияния пузырного и общего печеночного протока (сфинктер Мирисси), в шейке желчного пузыря (сфинктер Люткенса) и концевом отделе общего желчного протока и сфинктер ампулы, или Одди. Тонус мышц этих сфинктеров определяет направление движения желчи. Давление в желчевыделительном аппарате создается секреторным давлением желчеобразования и сокращениями гладких мышц протоков и желчного пузыря. Эти сокращения согласованы с тонусом сфинктеров и регулируются нервными и гуморальными механизмами. Давление в общем желчном протоке колеблется от 4 до 300 мм вод. ст., а в желчном пузыре вне пищеварения составляет 60—185 мм вод. ст., во время пищеварения за счет сокращения пузыря поднимается до 200—300 мм вод. ст., обеспечивая выход желчи в двенадцатиперстную кишку через открывающийся сфинктер Одди.
Пищеварение в 12-п кишке:
Пищеварения в двенадцатиперстной кишке проходит в два этапа: сначала происходит активация ферментов: трипсиноген под действием фермента кишечного сока энтерокиназы переходит в активный трипсин, который в свою очередь активирует химотрипсиноген. На втором этапе происходят процессы пищеварения.
В 12-п кишке продолжается процесс гидролиза пищ в-в. В полость кишки выд-ся соки поджелудочной кишечных желез, содерж-е ферменты для гидролиза БЖУ. Щелочная среда.
11. Состав и свойства кишечного сока. Регуляция секреции кишечного сока. Полостной и мембранный гидролиз пищевых веществ в различных отделах тонкой кишки.
Дата добавления: 2018-01-21; просмотров: 571; Опубликованный материал нарушает авторские права? | Защита персональных данных | ЗАКАЗАТЬ РАБОТУ
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Да какие ж вы математики, если запаролиться нормально не можете??? 8547 — | 7400 — или читать все…
Источник
Секреция ПЖ находится под контролем нервных и гуморальных механизмов. Начальную секрецию ПЖ вызывают вид, запах пищи и другие раздражители (условнорефлекторные сигналы), а также жевание и глотание (безусловнорефлекторные сигналы). При этом нервные сигналы, формирующиеся в рецепторах полости рта и глотки, достигают продолговатого мозга, и затем эфферентные влияния по волокнам блуждающего нерва поступают к железе и вызывают её секрецию.
У человека с фистулой ГПП выделение панкреатического сока начинается через 2—3 мин после того, как он увидел пищу или услышат о ней. Это пример условнорефлекторного пути возбуждения панкреатической секреции. Симпатические волокна, иннервирующие ПЖ, тормозят её секреторную активность и в то же время изменяют реактивность железы по отношению к другим воздействиям, усиливая синтез органических веществ.
Торможение панкреатической секреции происходит при раздражении многих чувствительных нервов, при болевых реакциях, во время сна, при напряжённой физической и умственной работе.
Для стимуляции панкреатической секреции прямые нервные влияния имеют меньшее значение, нежели гуморальные. Ведущее значение в гуморальной регуляции секреции ПЖ принадлежит желудочно-кишечным гормонам.
Большинство регуляторов секреции ферментов ПЖ действуют на рецепторы мембраны ацинарных клеток, расположенные на их базолатеральной поверхности. Выделяют рецепторы ХК, бомбезина, ацетилхолина, субстанции Р, ВИП, секретина.
Стимуляторы панкреатической секреции. ВИП и секретин стимулируют панкреатическую секрецию, активируя аденилатциклазу. Как и в других типах клеток, аденилатциклаза способствует образованию циклического аденозинмонофосфата, в результате чего протеинкиназа А, усиливающая секрецию панкреатического сока, богатого бикарбонатами, переходит в активную форму. Другие стимуляторы поджелудочной секреции (ХК, ацетилхолин, гастрин-рилизинг пептид, субстанция Р) действуют на специфические рецепторы, во внутриклеточной передаче сигнала от которых задействованы альтернативные вторичные мессенджеры.
Эти вещества повышают внутриклеточное содержание циклического гуанозинмонофосфата, что приводит к увеличению внутриклеточного содержания инозитолтрифосфата, диацилглицерола, арахидоновой кислоты и кальция. Эти промежуточные вещества-посредники активируют различные протеинкиназы, в результате этого повышается секреция ферментов. Данные, полученные в опытах на животных, свидетельствуют, что действие комбинации агонистов на различные мембранные рецепторы может вызывать синергический, но не суммарный (аддитивный) эффект. Например, ХК увеличивает секрецию бикарбонатов, стимулированную секретином, но секретин не повышает секреторный ответ на действие ХК.
Ингибиторы секреции поджелудочной железы. Различные вещества, ответственные за подавление панкреатической секреции, действуют по принципу отрицательной обратной связи во время и после приёма пищи.
Панкреатический полипептид (ПП) представляет собой пептидный гормон, образующийся в островках Лангерганса и подавляющий панкреатическую секрецию воды, бикарбонатов и ферментов. Концентрация ПП в плазме крови возрастает после мнимого кормления, после приёма пищи, после экспериментального закисления среды ДПК, а также при стимуляции блуждающего нерва, при действии ХК, секретина, ВИП. ПП может выступать как антагонист мускариновых рецепторов и способен ингибировать выделение ацетилхолина из постганглионарных нейронов ПЖ; его конечный эффект проявляется на уровне ацинарных клеток.
Пептид YY высвобождается в дистальной части подвздошной кишки и и толстой кишке в ответ на поступление пищи смешанного характера, по жиры, находящиеся в просвете кишки, в большей степени способны стимулировать его секрецию. Пептид YY уменьшает чувствительность ПЖ к действию секретина и ХК, возможно, за счёт уменьшения секреции ацетилхолина и норадреналина и ингибирования выделения ХК слизистой оболочкой ДПК.
Соматостатин ингибирует секрецию секретина слизистой оболочкой ДПК, а также уменьшает чувствительность к секретину рецепторных полей. Единственный эффект соматостатина — снижение секреции ферментов и бикарбонатов ПЖ. Соматостатин синтезируют клетки слизистой оболочки желудка и кишечника, а также D-клетки островков Лангерганса. Его активность составляет только около 25% от активности гипоталамического соматостатина. Но только соматостатин, продуцируемый слизистой оболочкой тонкой кишки, оказывает угнетающее действие на секрецию ПЖ.
Выделение соматостатина происходит при участии автономной нервной системы в ответ на поступление жиров и аминокислот с пищей.
Соматостатин блокирует панкреатическую секрецию несколькими способами. Во-первых, он действует путём угнетения продукции стимулирующих пептидов (ХК). Во-вторых, посредством угнетающего воздействия на ЦНС и регулируя работу интрапанкреатических ганглиев, соматостатин ингибирует поступление ацетилхолина в пресинаптическую щель и, возможно, ингибирует выработку инсулина. Хотя рецепторы к соматостатину найдены также в ацинарных клетках, эти рецепторы скорее способствуют увеличению секреции, чем блокируют её.
Другие ингибиторы, представленные среди гормонов эндокринных клеток островков Лангерганса, включают панкреатический глюкагон и панкреастатин, а также нейропептиды: кальцнтонин-генерирующий пептид и энкефалины (табл. 1-3). Панкреатический глюкагон ингибирует секрецию ПЖ, стимулированную ХК, секретином или пищей; угнетает секрецию бикарбонатов, воды и ферментов. Панкреастатин ингибирует панкреатическую секрецию, тормозя высвобождение ацетилхолина эфферентными окончаниями блуждающего нерва. Кальцитонин-генерирующий пептид может проявлять свою активность через стимуляцию выделения соматостатина. Энкефалины и подобные им опиоиды снижают выделение секретина слизистой оболочкой ДПК и могут также ингибировать высвобождение ацетилхолина.
Таблица 1-3. Ингибиторные нейромодуляторы

Маев И.В., Кучерявый Ю.А.
Опубликовал Константин Моканов
Источник
Регуляция секреции поджелудочной железы . Секреция поджелудочной железы регулируется нервными и гуморальными механизмами.
Нервная регуляция . И. П. Павлов показал, что раздражение блуждающего нерва вызывает выделение большого количества сока поджелудочной железы , богатого ферментами. Холинергические волокна блуждающих нервов с помощью АХ действуют на М-холинорецепторы панкреацитов. Затем высвобождающиеся ион Са2+ и комплекс ГЦ — цГМФ в роли вторичных мессенджеров стимулируют секрецию панкреоцитами ферментов и гидрокарбонатов. Холинергические нейроны, кроме того, потенцируют секреторные эффекты секретина и ХЦК. Хирургическая ваготомия существенно снижает секрецию поджелудочной железы.
Симпатические волокна, иннервирующие поджелудочную железу через β-адренорецепторы, тормозят ее секрецию , усиливают синтез органических веществ в ней. Адренергические эффекты снижения секреции обеспечиваются также уменьшением кровоснабжения поджелудочной железы путем сужения кровеносных сосудов через их α-адренорецепторы.
Торможение секреции вызывают болевые раздражения, сон, напряженная физическая и умственная работа и др.
Поджелудочная железа имеет также пептидергическую иннервацию. Окончания этих нейронов выделяют ряд нейропептидов, одни из которых стимулируют, другие — тормозят секрецию поджелудочной железы .
Гуморальная регуляция . Первым открытым (и на званным гормоном) явился секретин — стимулятор обильного сокоотделения и секреции гидрокарбонатов. Высвобождение этого гормона в кровь S-клетками двенадцатиперстной кишки происходит при действии на ее слизистую оболочку перешедшего в кишку кислого желудочного содержимого. Секретин стимулирует секрецию в большей мере через соответствующие мембранные рецепторы и вторичные мессенджеры АЦ — цАМФ центроацинозные и протоковые клетки, в меньшей мере — ацинозные клетки, поэтому выделяется секрет с высокой концентрацией гидрокарбонатов и низкой ферментативной активностью.
Вторым гормоном, усиливающим секрецию поджелудочной железы , является холецистокинин (ХЦК). Высвобождение гормона в кровь из ССК-клеток слизистой оболочки двенадцатиперстной и тощей кишки происходит под влиянием пищевого химуса (особенно продуктов начального гидролиза пищевых белков и жиров, углеводов, некоторых аминокислот). Стимулируют высвобождение ХЦК присутствие ионов Са2+ и снижение рН в двенадцатиперстной кишке.
ХЦК действует преимущественно на ацинусы поджелудочной железы , поэтому выделяющийся в ответ на стимуляцию этим гормоном сок богат ферментами. Вторичными мессенджерами являются ионы Са2+ и комплекс ГЦ — цГМФ. Одновременное действие на железу секретина и ХЦК (при приеме пищи) усиливает их стимуляторный эффект. Секретин и ХЦК применяются в клинике как стимуляторы секреции при диагностике заболеваний поджелудочной железы . Пептид химоденин стимулирует секрецию химотрипсиногена.
Секреция поджелудочной железы усиливается также гастрином, серотонином, инсулином, бомбезином, солями желчных кислот. Тормозят выделение поджелудочного сока глюкагон, соматостатин, вазопрессин, вещество Р, АКТГ, энкефалин, кальцитонин, ЖИП, ПП, УУ. ВИП может возбуждать и тормозить секрецию поджелудочной железы .
Фазы секреции поджелудочной железы . Секреция сока поджелудочной железы резко усиливается через 2—3 мин после приема пищи и продолжается 6—14 ч. От количества и качества пищи зависят объем, состав выделяющегося сока, динамика выделения. Чем выше кислотность пищевого содержимого желудка, поступающего в двенадцатиперстную кишку, тем больше выделяется сока поджелудочной железы и тем больше гидрокарбонатов в его составе. Поэтому кривая секреции поджелудочной железы в некоторой мере повторяет кривую желудочного сокоотделения. Отличия кривых секреции желудка и поджелудочной железы определяются в основном буферными свойствами пищи, которая частично нейтрализует кислоту желудочного сока, и скоростью эвакуации содержимого желудка в двенадцатиперстную кишку.
Фазы секреции поджелудочной железы при стимуляции ее приемом пищи те же, что были описаны для желудочной секреции , но в отличие от них более выражены гормональные влияния на поджелудочную железу , особенно в кишечную фазу. Секреция имеет характерную динамику, зависящую от вида принятой пищи (рис. 9.15).
Первая, или мозговая, фаза секреции поджелудочной железы обусловлена видом, запахом пищи и другими раздражителями, связанными с приемом пищи (условнорефлекторные раздражения), а также воздействиями на рецепторы слизистой оболочки рта, жеванием и глотанием (безусловно-рефлекторные раздражения). Нервные импульсы, возникающие в рецепторах, достигают продолговатого мозга и затем по волокнам блуждающего нерва поступают к железе и вызывают ее секрецию .
У человека с фистулой протока поджелудочной железы наблюдали условнорефлекторное выделение сока поджелудочной железы через 2—3 мин после того, как испытуемому говорили о пище, которую ему дадут. В реализации первой фазы секреции принимают участие и регуляторные пептиды, высвобождение которых стимулировалось рефлекторными механизмами блуждающих нервов.
Вторая, или желудочная, фаза характеризуется тем, что секреция во время нее стимулируется и поддерживается путем ваговагального рефлекса с механо- и хеморецепторов желудка и с помощью гастрина.
С переходом желудочного содержимого в двенадцатиперстную кишку начинается третья, или кишечная, фаза секреции поджелудочной железы . В эту фазу секреция стимулируется ваговагальным дуоденопанкреатическим рефлексом, но ведущее значение имеет высвобождение в кровь секретина и ХЦК. Высвобождение их происходит при действии на слизистую оболочку двенадцатиперстной кишки кислого ее содержимого. Чем больше свободных ионов Н+, тем больше высвобождается секретина и тем выше объем сока поджелудочной железы и секреция гидрокарбонатов. Гидрокарбонаты связывают ионы Н+, что приводит к повышению рН среды и уменьшает высвобождение секретина и соответственно объем сока и секрецию гидрокарбонатов. Секреция ферментов в кишечную фазу стимулируется ХЦК и рефлекторно за счет ваговагального рефлекса.
В кишечную фазу велика роль саморегуляции секреции поджелудочной железы по принципу отрицательной обратной связи в зависимости от свойств содержимого двенадцатиперстной кишки. Установлено, что отведение сока поджелудочной железы из двенадцатиперстной кишки вызывает гиперсекрецию поджелудочной железы , обратное введение сока в кишку тормозит эту секрецию . Введение в кишку гидрокарбонатов снижает объем секреции , концентрацию и дебит (выделение) гидрокарбонатов в составе сока. Введение сока поджелудочной железы в двенадцатиперстную кишку особенно выраженно тормозит секрецию поджелудочной железой ферментов. При этом повышение триптической активности химуса двенадцатиперстной кишки тормозит секрецию протеаз, повышение амилолитической активности химуса тормозит секрецию амилазы, повышенная липолитическая активность в наибольшей мере тормозит секрецию панкреатической липазы. Тормозные эффекты ферментов снимаются или снижаются их специфическими ингибиторами и пищевыми субстратами (Г. Ф. Коротько).
Таким образом, свойства секрета поджелудочной железы в кишечную фазу в большой мере определяются соотношением в химусе двенадцатиперстной кишки ферментов и гидролизуемых ими субстратов: избыток ферментов селективно тормозит их секрецию , избыток субстрата снимает эти тормозные влияния, и продукты гидролиза субстрата стимулируют секрецию соответствующих ферментов поджелудочной железой . Этот механизм направлен на срочную адаптацию секреции ферментов поджелудочной железы к виду принятой пищи. Его реализация обеспечивается М-холинергическими и (β-адренергическими влияниями, ХЦК, секретином.
В целом нервные влияния при приеме пищи обеспечивают пусковые воздействия на поджелудочную железу , в последующей коррекции ее секреции большую роль играют гуморальные механизмы. Однако высвобождение гормонов двенадцатиперстной кишкой и действие их на поджелудочную железу более выражены при сохраненной ее иннервации, что подчеркивает единство нервных и гуморальных механизмов регуляции секреции поджелудочной железы . При стимуляции секреции поджелудочной железы усиливается ее кровоснабжение, что важно для поддержания секреции на высоком уровне.
Секреция гуморально корригируется и всосавшимися питательными веществами. Эти влияния осуществляются непосредственно на панкреоциты, выражено влияние на них некоторых аминокислот и глюкозы, опосредуются через центральные нервные механизмы (например, гипоталамический и бульварный центры автономной нервной системы) и регуляторные пептиды.
Влияние пищевых режимов на секрецию поджелудочной железы . Прием пищи вызывает увеличение выделения всех ферментов в составе сока, но для разных видов пищи это увеличение выражено в разной мере. В случае приема пищи с большим содержанием углеводов в наибольшей мере увеличивается секреция амилазы, белков — трипсина и химотрипсина, прием жирной пищи вызывает секрецию сока с более высокой липолитической активностью. Спектр ферментов сока поджелудочной железы срочно адаптируется к виду принимаемой пищи во все три фазы секреции и особенно в кишечную фазу.
Существуют и медленные адаптации секреции ферментов в зависимости от длительного режима питания. Суть адаптации состоит в том, что поджелудочная железа синтезирует и секретирует больше того фермента, который гидролизует преобладающие в рационе питательные вещества. Преобладание в рационе белков повышает выделение в составе сока поджелудочной железы протеаз, преимущественное углеводное питание вызывает увеличение выделения с соком амилазы, а большое количество жира в рационе — выделение с соком липазы.
Эти изменения носят согласованный с изменениями функционирования других отделов пищеварительного тракта характер, составляя часть интегрированных адаптации всего пищеварительного конвейера.
Источник