Сколько живут после химиотерапии на поджелудочной железе
Химиотерапия при раке поджелудочной железы обладает некоторыми особенностями по сравнению с той, которая используется при онкологии других органов. Проанализируем основные отличия этого медикаментозного метода, с какой целью назначается, как проводится и насколько может быть эффективным.
Значение химиотерапии при онкологическом поражении ПЖ
Химиотерапия при онкологии поджелудочной железы не способна полностью подавить жизнедеятельность раковых клеток, так как новообразования, развивающиеся в этом органе, относятся к опухолям химиорезистентного типа, малочувствительные либо вообще не чувствительные к влиянию цитостатических медикаментов.
Возникает естественный вопрос, зачем тогда она используется, если не оказывает полноценного лечебного действия? Целесообразность ее применения объясняется следующим:
- После хирургической операции на органе существует опасность сохранения некоторого количества злокачественных клеток в смежных тканях. Их жизнедеятельность подавляется цитостатиками.
- С присутствующими клетками намного проще бороться после операции, чем когда они подпитываются от опухоли.
- Микроскопические зоны метастазирования поддаются уничтожению посредством химиотерапии.
- Позволяет продлить период ремиссии.
- Длительность жизни увеличивается в 1,5-2 раза по сравнению с теми больными, которым была сделана только одна операция.
Способы проведения в зависимости от стадии рака
Химиотерапия относится к системным видам лечения, особенности которого зависят от степени тяжести патологического процесса.
| Стадии рака ПЖ | Основная цель цитостатической терапии |
| Вторая | Осуществляется в комбинации с операцией. Применяется после хирургического вмешательства для подавления роста оставшихся раковых клеток. |
| Третья | Используется для приостановления активного распространения метастазов. |
| Четвертая | Назначается с целью улучшения качества жизни больного. |
При раке ПЖ применяется два вида цитостатического лечения:
- Монохимиотерапия.
- Полихимиотерапия.
Помимо этого существует несколько подвидов химиотерапии:
| Подвиды химиотерапии | Особенности |
| Адъювантная | Рекомендуется в послеоперационный период. Предупреждает раковые рецидивы. |
| Неоадъювантная | Используется только до операции с целью удаления единичных метастазов. |
| Таргетная | Воздействует на генетические нарушения в клетках. Уменьшает объем опухоли, не допуская ее дальнейшего увеличения, а в отдельных эпизодах наблюдается полное исчезновение новообразования. |
| Гипертермическая | В брюшную область вводятся лекарства, подогретые до 41 градуса. Практикуется при метастазах, которые из ПЖ начали распространяться по брюшным органам. |
| Высокодозная | Применяется повышенная доза цитостатиков. Назначается при лимфомах ПЖ. |
| Паллиативная | Используется не для лечения, а для облегчения мучительной симптоматики (чаще на 4 стадии рака с активными метастазами). |
| Щадящая | Рекомендуется больным пожилого возраста, у которых диагностированы очень негативные параметры крови. Отличается низким эффектом. |
Когда требуется прохождение химиотерапии
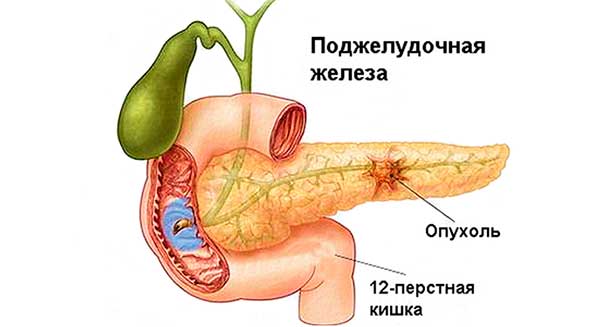
Прохождение химиотерапии при раковом образовании в поджелудочной железе назначается:
- До и после хирургической операции.
- При распространении метастазов на соседние ткани.
- При выявлении метастазов на других участках организма.
- Если новообразование располагается очень близко к крупным кровеносным сосудам, что делает невозможным операционное лечение.
- Присутствует нерезектабельная опухоль.
- Как самостоятельный терапевтический метод в сочетании с сеансами облучения.
- Пациент отказался от хирургического метода лечения.
Когда химиотерапия противопоказана
Химиотерапия при раке ПЖ является недопустимой процедурой, если у пациента:
- Опухоль устойчива к назначенному химиопрепарату.
- Отмечается гиперчувствительность к составляющим медикамента.
- Анализы подтвердили дисфункцию почек, дыхательных органов, печени и сердечно-сосудистой системы.
- Психические расстройства.
- Стабильно высокая температура (более 38 градусов).
- Общее самочувствие организма определяется как тяжелое.
- Отмечается кровотечение или наличие острой инфекции.
- Стремительное понижение массы тела.
- Существенные отклонения в составе кровяной жидкости.
Самые востребованные препараты и их комбинации
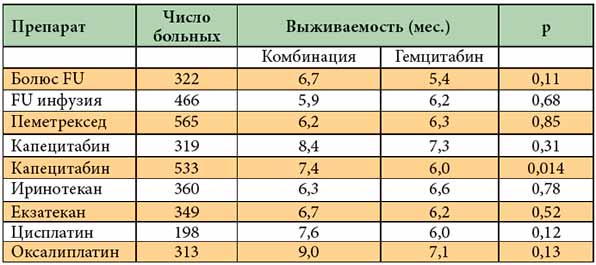
Современная онкология использует различные цитостатические средства, при этом выбор конкретного препарата обусловливается следующими параметрами:
- Тип раковой опухоли.
- Особенности локализации.
- Степень распространенности.
- Общее состояние организма.
Цитостатические препараты при раке поджелудочной железы разделены на первую и вторую линию.
| Линия препаратов | Названия лекарств и схемы | Особенности |
| Первая | Гемцитабин. | Контролирует раковый процесс. Снижает выраженность симптомов. Назначается как самостоятельно, так и в совмещении с другими медикаментами. Используется при местно-распространенной или метастатической онкологии ПЖ либо в послеоперационный период. При значительном ослаблении организма применяется только один Гемцитабин. При удовлетворительном состоянии пациента используется в схеме с другими средствами. |
| FOLFIRINOX: — Иринотекан. — Лейковорин. — Оксалиплатин. — 5-Фторурацил. | Подойдет пациентам с удовлетворительным самочувствием, так как FOLFIRINOX отличается крайне агрессивным характером и провоцирует значительное количество побочных явлений. | |
| GemCap: — Капециатиб. — Гемцитабин. | Практикуется при местно-распространенной злокачественной форме ПЖ. При метастазах применяется изредка, чаще всего назначается Наб-паклитаксел. | |
| Гемцитабин в совмещении с Наб-паклитакселом. | Прописывается на последних стадиях местно-распространенной онкологииПЖ. | |
| Вторая | Комбинация: 5-Фторурацил. Оксалиплатин. | Проводится в тех ситуациях, когда снижается эффективность химиотерапии при раке поджелудочной железы посредством лекарств и схем первой линии. |
| Капецитабин или 5-Фторурацил. | Назначаются после применения Гемцитабина больным с болезненным самочувствием или при опасности проявления серьезных отрицательных эффектов. | |
| Гемцитабин самостоятельно или в совмещении с Капецитабином. | Прописывается онкобольным после прохождения схемы FOLFIRINOX, здоровье которых позволяет получать химиотерапию. |
Варианты приема химиопрепаратов:
- Внутривенно.
- Капельно.
- Комбинация.
- Перорально.
Назначение предварительной диагностики организма
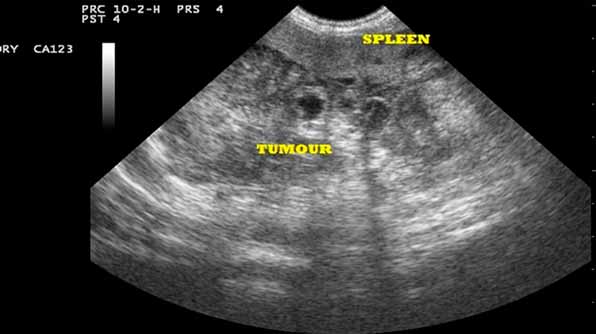
Перед каждым новым циклом химиотерапии больной должен пройти обследование организма.
Лабораторные анализы:
- Полный тест крови.
- Опухолевые маркеры.
- Почечный анализ.
- Печеночный тест.
Проводится мониторинг сердечно-сосудистой и дыхательной системы. Необходимость дальнейшего продолжения химиотерапии определяется по результатам анализа крови.
Помимо сдачи лабораторных тестов, пациент находится под постоянным наблюдением специалистов:
- Регулярная проверка веса.
- КТ — каждые 3 месяца.
- Контроль общего самочувствия пациента, которое может иметь тенденцию к улучшению, хотя снимки не фиксируют положительных изменений в раковом процессе.
- Уточнение присутствия и характера негативной симптоматики, возникшей после последнего цикла химиотерапии.
Для сохранения полной информации о течении химиотерапии врачи рекомендуют вести дневник, в котором фиксировать характер проявляемой отрицательной клиники. Далее специалист проводит их оценку по шкале от 0 до 4, где:
- 0 – полное отсутствие побочной симптоматики.
- 4 – тяжелой степени проявления, опасные для жизни.
Подобный анализ позволяет определить степень эффективности проводимого лечения и при необходимости отрегулировать его схему и дозировку цитостатиков либо назначить дополнительный препарат.
Особенности прохождения химиотерапии
Сколько курсов химиотерапии назначают при раке поджелудочной железы? Для каждого пациента разрабатывается индивидуальная лечебная схема и подбирается оптимальный вариант медикамента и дозировки.
Курс химиотерапии состоит из циклов, каждый из них содержит в себе один либо несколько сеансов с обязательным отдыхом, позволяющим организму восстановиться от воздействия препаратов. На сегодняшний день самыми практикующими являются циклы длительностью в 2-4 недели.
Перед проведением каждого курса делается анализ крови для установления показателей тромбоцитов и лейкоцитов. При их низком показателе продолжительность цикла пересматривается.
Сеансы цитостатической терапии выполняются:
- Амбулаторно.
- Стационарно.
- В онкологическом отделении.
- С госпитализацией.
- Без госпитализации.
Лечение до операции
Неоадъювантная химиотерапия прописывается как самостоятельно, так и в совмещении с радиооблучением. Ее проведение целесообразно при отсутствии метастазирования или нерезектабельной опухоли.
Методика позволяет уменьшить объем новообразования, и тем самым достигается возможность выполнения операции. В большинстве ситуаций рекомендуется тем больным, которые находятся в группе пограничных кандидатов на возможное радикальное вмешательство.
Если злокачественное образование расположено в головке ПЖ, перед химиотерапией делается декомпенсация желчных каналов, обеспечивая корректный отток желчи.
Лечение после хирургии
После хирургического удаления раковой опухоли практикуется химиотерапия адъювантного типа, которая применяется при следующей клинике:
- Начальная стадия рака ПЖ.
- После полного устранения новообразования и отсутствия метастазов в организме.
Уменьшает вероятность возвращения болезни в послеоперационный период и позволяет:
- Предотвратить или замедлить повторное метастазирование.
- Предупредить либо затормозить последующее проявление основной опухоли.
- При наличии метастазов подавить их активность.
Если применение препаратов первой линии при адъювантной терапии оказалось малоэффективным, назначаются цитостатики второй линии.
Популярные схемы:
| Методика | Особенности |
| Гемцитабин | Показаны внутривенные инъекции, которые проводятся в 1-ый, 8-ой и 15-ый день лечения. Повторное прохождение — через 28 суток. |
| Схема Мейо | На протяжении 5-ти дней делаются внутривенные уколы медикаментозной комбинации – Фторурацила и Фолината. |
| Капецитабин | Каждодневное внутривенное впрыскивание на протяжении 14 дней. Повторение терапии через 3 недели. |
Обычно химиотерапия при онкологии ПЖ проводится через 3 месяца после оперативного вмешательства, а ее продолжительность растягивается на 6 месяцев.
Терапия при невозможности выполнения хирургии
Когда раковая опухоль ПЖ имеет местно-распространенный характер, проведение операции маловероятно. Однако химиотерапия может быть применена и при тяжелых стадиях рака, что позволяет добиться снижения размера образования до тех параметров, при которых можно провести резекцию.
Эффективные схемы:
| Методика | Особенности |
| Гемцитабин | Схема применения такая же, как и при адъювантном лечении либо внутривенно 1 раз в 7 дней на протяжении семи недель. Затем делается недельный перерыв и лечение повторяют. Далее показано чередование трехнедельных циклов с перерывом в 28 дней. |
| GemCap | Курс: 1-ый и 8-ой день – Гемцитабин. Далее ежедневно в течение 14 дней – Капецитабин. Длительность цикла – 3 недели. |
| GemOx | Схема: 1-ый и 8-ой день – Гемцитабин. 1-ый день – Оксалиплатин. Повторяется спустя 21 день. |
| FOLFOXIRI | Комбинация: Кальция фолинат, Иринотекан, 5-Фторурацил и Иринотекан. Вводится струйно, а далее капельно на протяжении 46 часов. Повторное прохождение через 2 недели. |
| Эрлотибин в совмещении с Гемцитабином | Первый препарат используется ежедневно и постоянно, а Гемцитабин по одному из вариантов, указанных выше. |
В сочетании с лучевой терапией
Как уже упоминалось выше, при некоторых проявлениях химиотерапия практикуется в сочетании с сеансами лучевой терапии. В этом случае дозировка цитостатика уменьшается вместе с суточной дозировкой радиооблучения.
Основная цель лечебного подхода – повысить восприимчивость злокачественной опухоли к лучевому воздействию.
Химиолучевые сеансы назначаются пациентам, у которых присутствует пограничное показание к проведению операции или местно-распространенная форма рака, поддающаяся воздействию химиотерапии, однако сама опухоль не сократилась до нужных размеров, позволяющих провести хирургическое лечение.
Прохождение реабилитационного периода
Восстановительный период является важной частью комплексной терапии злокачественной патологии ПЖ. Реабилитация позволяет возобновить функциональность органов, пострадавших от агрессивного влияния цитостатиков.
После химиотерапии рака поджелудочного органа прописываются симптоматические медикаменты и диетстол. Немаловажное значение имеет коррекция образа жизни.
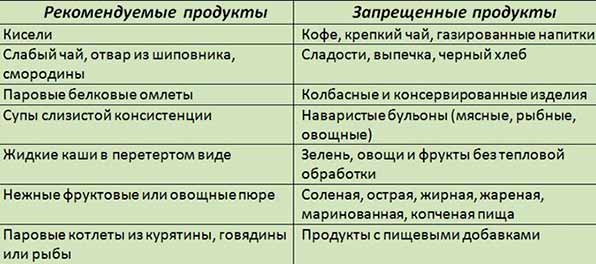
Важно соблюдать все предписания по диетическому питанию до, при и после химиотерапии:
- За два-три дня до сеанса следует снизить общий объем потребляемой еды и перейти на дробное питание. Запрещается употреблять соленую, жирную и острую пищу, а также избегать различных пряностей и приправ. Предпочтительно кушать высококалорийную пищу.
- При прохождении курса химиотерапии соблюдать правила, рекомендованные в первом пункте. Отдельные поправки в рацион вносятся, если это связано с особенностями используемых медикаментов.
- Питание после химиотерапии поджелудочной железы должно быть калорийным и богатым на витамины и минералы (фрукты, зелень, овощи и прочее).
На всех этапах получения цитостатиков и после них показан усиленный питьевой режим (отвары из брусники, шиповника и березовых почек).
Возможные негативные последствия лечения

Цитостатики, применяемые при химиотерапии крайне агрессивно воздействуют на раковые клетки, однако одновременно с этим затрагивают и абсолютно здоровые ткани, о чем свидетельствует побочная симптоматика:
- Выраженная тошнота.
- Приступы рвоты.
- Значительный упадок сил.
- Активное выпадение волос.
- Повышенная сухость во рту.
- Существенное снижение аппетита.
- Стойкие запоры или диарея.
- Проявление стоматита.
- Гематомы на коже.
- Незаживающие язвы в ротовой полости.
- Резкое проявление анемии.
- Значительное ослабление иммунитета.
- Искажение вкусовых ощущений.
- Сильный кожный зуд и сыпь.
- Истощение костной ткани.
Дальнейший прогноз
Вероятность благоприятного исхода после химиотерапии зависит от особенностей течения рака ПЖ.
| Химиотерапия | Предполагаемый лечебный исход |
| Адъювантная | Уменьшает прогрессирование рака после хирургии на треть. Продлевает срок жизнь на 20-22 месяцев. |
| Неоадъювантная | У 10-17% пациентов снижается активность онкологии. |
| Паллиативная | Эффективно купируется симптоматика онкологии у 20-30% пациентов. У 50% пациентов позволяет добиться уменьшения дозировки обезболивающих наркотической группы в 2 раза. Продолжительность жизни увеличивается до 6 месяцев. Применение FOLFOXIRI позволяет добиться увеличения жизни на 9-11 месяцев. |
Заключение
Химиотерапия при раке паренхимы ПЖ, как системный метод лечения помогает добиться угнетения жизнедеятельности злокачественных клеток с дальнейшим их разрушением. Применение цитостатических препаратов показано на любой стадии болезни, что существенно улучшает самочувствие пациента и продлевает ему жизнь.
Загрузка…
Источник
Российский онкологический научный центр им. Н.Н. Блохина РАМН
Рак поджелудочной железы (РПЖ) относительно редкое заболевание – составляет 3% среди всех злокачественных опухолей, но стоит на 5 месте среди наиболее частых причин смертности от рака. В последние десятилетия отмечен устойчивый рост заболеваемости. В 1999 году в России выявлено 13 тыс. вновь заболевших, умерло 11 тыс. человек [1]. 5–летняя выживаемость при РПЖ самая низкая среди всех опухолей – 3%, медиана жизни нерезектабельных больных около 4 месяцев.
Пик заболеваемости приходится на шестое десятилетие жизни. Факторами риска являются курение, сахарный диабет, хронический панкреатит. Опухоли, главным образом, развиваются из экзокринной части поджелудочной железы и в 80% случаев представлены аденокарциномой.
Главная особенность РПЖ – поздняя диагностика. Опухоль дает раннее обширное метастазирование, у 90% больных в момент постановки диагноза уже имеется местнораспространенный или диссеминированный процесс, когда радикальное хирургическое лечение невозможно.
Таким образом, при местнораспространенном процессе химио– и/или лучевая терапия, а при диссеминированном процессе – химиотерапия, являются единственными методами возможного воздействия, однако из–за низкой чувствительности опухоли стандарта паллиативного лечения РПЖ не существует.
В течение многих лет 5–фторурацил (5ФУ) был препаратом выбора для больных, которым была показана монохимиотерапия. По результатам исследований 1970–80 гг. его эффективность составляет 15–20%, однако более поздний анализ показал активность 5ФУ от 0 до 14% [2]. Эффективность таких цитостатиков, как митомицин С (митС), ифосфамид (ифо), цисплатин (ДДП) при РПЖ около 15% [2,3,4]. Еще меньшей активностью обладают стрептозотоцин и доксорубицин (Dxr) [2]. Все препараты дают только частичные регрессии опухоли. Комбинированные режимы: ФАМ (5ФУ, Dxr, митС) или СМФ (стрептозотоцин, митС, 5ФУ) – увеличивая токсичность лечения, не улучшают его результатов [5, 6]. Гормональное лечение с использованием тамоксифена или аналога соматостатина октреотида не показало какого–либо клинического значения [7].
Еще одна серьезная проблема при РПЖ – оценка эффективности лечения. Такие современные технические средства, как компьютерная томография (КТ) или магнитно-резонансная томография (МРТ), из–за выраженных десмопластических реакций, включающих воспаление и фиброз внутри и вокруг опухоли, не позволяют измерить ее распространенность, уточнить локализацию внутри прилежащих тканей и, следовательно, четко интерпретировать ответ на лечение. Прежде всего, это относится к местнораспространенной опухоли.
Поэтому при РПЖ оценка качества жизни в процессе паллиативного лечения стала одним из параметров его эффективности. При этом учитывается общее состояние пациента, интенсивность боли и количество применяемых анальгетиков, меньшее значение имеет динамика массы тела.
Связанный с опухолью болевой синдром является ведущим симптомом РПЖ и наблюдается у 80% больных при установлении диагноза. Показано, что даже небольшое уменьшение размеров опухоли в процессе лечения, объективно соответствующее стабилизации, может сопровождаться значительным уменьшением болевого синдрома и количества применяемых анальгетиков [8].
Разработанная система оценки паллиативного эффекта при РПЖ включает: ослабление болевого синдрома на 50%, уменьшение суточного потребления наркотиков на 50%, улучшение общего состояния на 20% по шкале Карновского и положительную динамику веса на 7% от исходного [9]. Такая динамика этих показателей или хотя бы одного из них, сроком не менее, чем 4 недели, без ухудшения других, рассматривается как клиническое улучшение или клиническая выгода (КВ). Впервые качество жизни, как критерий эффективности лечения, было использовано при оценке роли гемцитабина в химиотерапии РПЖ.
Гемцитабин – производное дезоксицитидина. Цитостатик из группы антиметаболитов, обладает противоопухолевой активностью при ряде солидных опухолей. Первые сообщения о положительном эффекте гемцитабина при запущенном РПЖ появились в начале 90–х годов. В исследовании Casper с соавт. [10] частичная регрессия опухоли сроком более 6 месяцев зафиксирована у 5 из 39 больных (13%), еще у 3 пациентов (7,7%) отмечена регрессия менее 50%. Наблюдалось уменьшение как первичной опухоли, так и метастазов в печень. Эффект сопровождался уменьшением болевого синдрома и улучшением общего состояния. Международная медицинская экспертиза подтвердила эти результаты.
В 1997 г. опубликованы окончательные результаты кооперативного сравнительного рандомизированного изучения эффективности гемцитабина и 5ФУ у 126 больных, проведенного в США и Канаде [11]. Объективный эффект при лечении гемцитабином составил 5,4%, при 5ФУ – не наблюдался. Симптоматическое улучшение в группе с гемцитабином составило 23,8%, в группе с 5ФУ – 4,8%. Наблюдение за больными в течение года продемонстрировало следующее: живы 18% больных, леченных гемцитабином, в сравнении с 2%, леченных 5ФУ (р = 0,0025).
Результаты проведенных в США других кооперированных исследований показали симптоматический эффект у 17 из 63 больных, получавших гемцитабин (27%) и не ответивших на лечение 5ФУ, при этом объективная регрессия опухоли составила 10,5%. Больше 6 мес. прожили 31%, более 9 мес. – 15% и более 1 года – 4% пациентов [12]. В настоящее время гемцитабин рекомендован в качестве 1 линии химиотерапии при запущенном РПЖ в России и зарубежом. Общепринятая разовая доза препарата в режиме монохимиотерапии – 1000–1200 мг/м2, вводимая 30–минутной внутривенной инфузией 1 раз в неделю в течение 7 недель, затем после 1–недельного перерыва в 1, 8, 15 дни.
Гемцитабин обладает минимальными побочными действиями и хорошо переносится больными. Алопеция наблюдается редко, рвота возникает в среднем у 20% пациентов. Дозолимитирующая токсичность: нейтропения III–IV ст. – 24–30%, тромбоцитопения III–IV ст. – около 5%, анемия III–IV ст. – около 7%.
Комбинированная химиотерапия
Доклинические исследования показали синергизм взаимодействия гемцитабина с 5ФУ, ДДП и рядом других цитостатиков. В связи с этим в клинике изучались двойные комбинации гемцитабина с 5ФУ, ДДП, эпирубицином у больных РПЖ. Эффективность лечения в этих исследованиях варьировала от 5 до 21%, медиана времени до прогрессирования – от 2,4 до 7,4 мес., медиана общей выживаемости – от 4,3 до 10,3 мес., 1–годичная выживаемость – от 9 до 39,5% [13, 14, 15, 16, 17, 18, 19]. Гемцитабин вводился в стандартных дозах в виде 30–минутной инфузии, 5ФУ вводился болюсно, в виде 24–часовой инфузии или длительной внутривенной инфузией (ДВИ) ± лейковорин. Использовались стандартные и высокие дозы 5ФУ, однако преимуществ у комбинации гемцитабина с высокими дозами 5ФУ не отмечено.
Таким образом, продемонстрирован большой разброс результатов. Количество больных, включенных в эти исследования, варьировало от 26 до 66, метастатическая форма заболевания составляла от 46% до 100% всей популяции, поражение печени наблюдалось в 65–87% случаев, в большинстве случаев не учитывалась степень злокачественности опухоли, которая является одним из главных прогностических факторов при протоковой аденокарциноме поджелудочной железы [20]. Интерпретация полученных результатов затруднительна, кроме того, оценка влияния химиотерапии на выживаемость находится за пределами исследований по II фазе.
Активно изучается комбинация гемцитабина с доцетакселом, которая по мнению ряда исследователей является перспективной [21, 22, 23].
Опубликованы предварительные результаты рандомизированного исследования, сравнивающего активность гемцитабина в монотерапии с комбинацией гемцитабин + цисплатин при распространенном РПЖ [24]. В обеих группах гемцитабин вводился в дозе 1000 мг/м2 в 1, 8, 15 дни каждые 29 дней. ДДП вводился в дозе 25 мг/м2 во второй группе в те же дни, что и гемцитабин. У больных, получавших гемцитабин в монорежиме, общая эффективность лечения – 10%, у больных, получавших комбинацию – 42%. Клиническое улучшение практически одинаково в обеих группах (45% и 38%). Изучаются и другие, более сложные схемы полихимиотерапии. Villa с соавт. [25] разработал 4–х компонентный режим PEF–G, включающий гемцитабин (Гем), цисплатин, эпирубицин (эпи) и 5ФУ.
Схема лечения PEF–G:
ДДП – 40 мг/м2 в 1 день.
Эпи – 40 мг/м2 в 1 день.
Гем – 600 мг/м2 1–часовая инфузия в 1, 8 дни.
5ФУ – 200 мг/м2/день длительная инфузия в течение всего курса.
Лечение повторяется каждые 4 недели. Максимально до 6 курсов или до прогрессирования болезни (ПБ) или неприемлемой токсичности. Оценено 43 больных, отмечена 1 полная и 24 частичных регрессии опухоли, общая эффективность лечения – 58% (25 / 43). У 14 пациентов наблюдалась стабилизация (СТ) – 33%. Медиана длительности ремиссий – 8,5 мес., медиана времени до прогрессирования – 7,5 мес., медиана выживаемости – 11 мес. Клиническая выгода лечения оценена как положительная у 22 из 28 пациентов (78%). Токсичность режима PEF–G высока: нейтропения III–IV ст. – 85%, тромбоцитопения III–IV ст. – 59%, анемия III ст. – 7%, стоматит III ст. – 12%, диарея – 6%, рвота – 6%.
Наилучшая симптоматическая терапия
Наилучшая симптоматическая терапия – одна из составляющих всего комплекса паллиативного лечения при распространенном РПЖ, ее основными методами являются лечебное питание, симптоматическое лечение, психологическая помощь.
Лечение симптомов болезни проводится с целью улучшения качества жизни пациентов и включает облегчение абдоминальных болей, прекращение снижения веса, уменьшение анорексии. Очень важна проблема оказания психологической помощи больным, т.к. при РПЖ более высока частота психических нарушений, чем при других формах рака. Больные боятся этого заболевания в связи с его репутацией смертельного и вызывающего боли, тревога и депрессия часто осложняют течение болезни. В таблице 1 представлены лечебные мероприятия, включаемые в термин «наилучшая симптоматическая терапия».
К настоящему времени рядом рандомизированных исследований установлено, что паллиативная химиотерапия превосходит по результатам наилучшую симптоматическую терапию или отсутствие дополнительного лечения (данные представлены в таблице 2).
Итак, паллиативное лечение при распространенном раке поджелудочной железы включает в себя как специфическое противоопухолевое лечение, так и симптоматическую терапию (см. табл. 3).
Заключение
Рак поджелудочной железы – тяжелое заболевание, представляющее собой серьезную проблему в онкологии. Это обусловлено рядом причин:
Рак поджелудочной железы – тяжелое заболевание, представляющее собой серьезную проблему в онкологии. Это обусловлено рядом причин:
- рост заболеваемости;
- поздняя диагностика (80% больных имеют запущенный опухолевый процесс);
- низкая 1–годичная и 5–летняя выживаемость;
- низкая чувствительность опухоли к химио– и лучевой терапии.
В последнее десятилетие повысился интерес к паллиативному лечению при распространенном РПЖ. Это связано с появлением новых препаратов и подходов к комбинированной химиотерапии, а также с введением новых критериев оценки результатов лечения, учитывающих такие параметры как качество жизни (КЖ), и клиническую выгоду (КВ).
Доказано, что химиотерапия увеличивает выживаемость и улучшает качество жизни больных по сравнению с наилучшей симптоматической терапией. Максимальная эффективность химиотерапии достигается при использовании гемцитабина, который является препаратом I линии при этом заболевании.
В настоящее время химиотерапия обладает наибольшим потенциалом в паллиативном лечении распространенного РПЖ, одновременно воздействуя на опухоль и качество жизни больных.
Литература:
1. Н.Н. Трапезников, Е.М. Аксель, Статистика злокачественных новообразований в России и странах СНГ (состояние онкологической помощи, заболеваемость и смертность). Москва 2001, 295 с.
2. O’Connell M.J. «Current status of chemotherapy for advanced pancreatic and gastric cancer». J. Clin Oncol 1985; 3: 1032–1039.
3. Loehrer P. et al. «Ifosfamide: an active drug in the treatment of adenocarcinoma of the pancreas». J. Clin Oncol 1985; 3:367–372.
4. Wils J., Kok T., Wagener D. et al. «Activity of cisplatin in adenocarcinoma of the pancreas». Eur. J. Cancer 1993; 29 A (2): 203–204.
5. Smith F.P., Hoth D.F., Levin B., et al. «5–fluorouracil, Adriamycin and mitomycin C (FAM) chemotherapy for advanced adenocarcinoma of the pancreas». Cancer 1981; 46: 2014–2018.
6. Wiggaus R.G., Wooley P.V., Mac Donald J.S., et al. «Phase II trial of streptozotocin, mitomycin C, and 5–fluorouracil (SM7) in the treatment of advanced pancreatic cancer». Cancer 1978; 41: 387–391.
7. Cascinu S., DelFerro E., Catalano G. «Arandomized trial of octreotide vs best supportive care only in advanced gastrointestinal cancer patients refractory to chemotherapy». Br. J. Cancer 1995; 71: 97–101.
8. Glimelius B., Hoffman K., Sjoden P.–O., et al. «Chemotherapy improves survival and quality of life in advanced pancreatic and biliary cancer». Ann Oncol 7: 593–600, 1996.
9. Fink U., Russel R.C., Spittle M.E., et al. « Phase II study of gemcitabine in patients with advanced pancreatic cancer». Eur. J. Cancer 1993; 29 (suppl 6): 101.
10. Casper E.S., Green M.R., Kelsen D.F., et al. «Phase II trial of gemcitabine in patients with adenocarcinoma of the pancreas». Invest New Drugs 12: 29–34, 1994.
11. Burris H.A. III, Moore M.J., Andersen J., et al. «Improvement in survival and clinical benefit with gemcitabine as first–line therapy for patients with advanced pancreatic cancer: A randomized trial». J. Clin Oncol 15: 2403–2413, 1997.
12. Rothemberg M.L., Moore M.J., Cripps M.C., et al. «A phase II trial of gemcitabine in patients with 5–FU–refractory pancreas cancer». Ann Oncol 7: 347–353, 1996.
13. Heinemann V., Wilke H., Mergenthaler H.–G., et al. « Gemcitabine and cisplatin in the treatment of advanced or metastatic pancreatic cancer». Ann Oncol 11: 1399–1403, 2000.
14. Scheitauer W., Kornek G.V., Raderer M., et al. «Phase II trial of gemcitabine 4, epirubicin and granulocyte cololny–stimulating factor in patients with advanced pancreatic adenocarcinoma». Br. J. Cancer 80: 1797–1802, 1999.
15. Hidalgo M., Castellano D., Paz–Ares L., et al. « Phase II study of gemcitabine 4 and fluorouracil as a continious infusion in patients with pancreatic cancer». J. Clin Oncol 17: 585–592, 1999.
16. Oettle H., Arning M., Pelzer U., et al. «A phase II trial of gemcitabine in combination with 5–fluorouracil (24 hour) and folinic acid in patients with chemonaive advanced pancreatic cancer». Ann Oncol 11: 1267–1272, 2000.
17. Berlin J.D., Adak S., Vaughn D.J., et al. « A phase II study of gemcitabine and 5–fluorouracil in metastatic pancreatic cancer: An Eastern Cooperative Oncology Group study (E3296)». Oncology 58: 215–218, 2000.
18. Cascinu S., Silva R.R., Barni S., et al. «A combination of gemcitabine and 5–fluorouracil in advanced pancreatic cancer: A report from the Italian Group for the study of Digestive Tract Cancer (GISCAD)». Br. J. Cancer 80: 1595–1598, 1999.
19. Cascinu S., Frontini L., Labianca R., et al. « A combination of a fixed dose– rate infusion of gemcitabine associated to a bolus 5–fluorouracil in advanced pancreatic cancer: A report from the Italian Group for the study of Digestive Tract Cancer (GISCAD)». Ann Oncol 11: 1309–1311, 2000.
20. Luttges J., Schemm S., Vogel I., et al. «The grade of pancreatic ductal carcinoma is an independent prognostic factor and is saperior to the immunohistochemical assessment of proliferation». J. Pathol 191: 154–161, 2000.
21. Cascinu S., Graziano F., Catalano G., et al. « A phase I–II study of gemcitabine and docetaxel in advanced pancreatic cancer: A report from the Italian Group for the study of Digestive Tract Cancer (GISCAD)». Ann Oncol 10: 1377–1379, 1999.
22. Kakolyris S., Stathopulos G., Tsavaris N., et al. « First–line treatment with docetaxel (D) and gemcitabine (G) in patients with unresactable pancreatic cancer: A multy–center phase II study». Proc. ASCO, 1999.
23. Jacobs A.D., Otero H., Picozs V., et al. « A phase I/II study of gemcitabine (G) and docetaxel (D) in patients (Pts) with unresactable pancreatic cancer». ASCO 2000; Educational Book.
24. Colucci G., Riccardi F., Giuliani F., et al. «Randomized trial of gemcitabine above or with cisplatin in treatment of advanced pancreatic cancer: A phase II multicentre study of the Southeru Italy Oncology Group». Proc. ASCO 18: 961, 1999.
25. Reni M., Passoni P., Panucci M.G., et al. «PE7–g (cisplatin, epirubicin, 5–fluorouracil continuous infusion, gemcitabine): A new combination in advanced pancreatic adenocarcinoma. Phase II study». J. Clin Oncol 19: 2679–2686, 2001.
26. Mallison C.N., Rake M.O., Cocking J.B., et al. «Chemotherapy in pancreatic cancer. Results of a controlled, prospective, randomized multicentre trial». Br. Med. J. 1980; 281: 1589–1591.
Источник



