Сниженная секреция бикарбонатов поджелудочной железой при нормальной секреции липазы и
Предотвращение самопереваривания поджелудочной железы. Секреция ионов бикарбоната
Необходимо подчеркнуть, что протеолитические ферменты поджелудочного сока не активируются до тех пор, пока не будут выделены в кишечник, поскольку трипсин и другие ферменты могли бы переварить саму поджелудочную железу. К счастью, клетки, которые секретируют протеолитические ферменты в ацинусах поджелудочной железы, выделяют одновременно вещество, названное ингибитором трипсина. Эта субстанция образуется в цитоплазме железистых клеток и предотвращает активацию трипсина как внутри секреторных клеток, так и в ацинусах и протоках поджелудочной железы. Вследствие того, что трипсин активирует другие панкреатические протеолитические ферменты, ингибитор трипсина в той же степени предотвращает их активацию.
При повреждении поджелудочной железы или блокировании протока в поврежденных участках поджелудочной железы может собираться большое количество панкреатического секрета. В таких условиях часто подавляется действие ингибитора трипсина, и происходит стремительная активация панкреатического секрета, который может буквально полностью переварить поджелудочную железу в течение нескольких часов. Такое состояние называют острым панкреатитом. Это состояние может быть смертельным, т.к. сопровождается циркуляторным шоком. Даже если оно не привело к смерти, то в дальнейшем обычно возможна хроническая недостаточность поджелудочной железы.
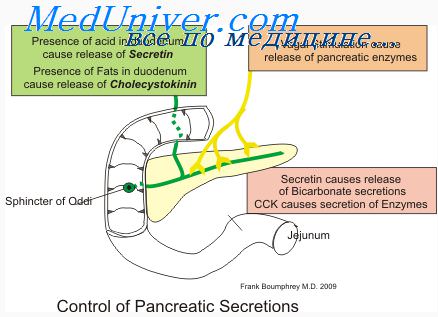
Секреция ионов бикарбоната
Хотя ферменты поджелудочного сока полностью выделяются ацинусами поджелудочной железы, два других важных компонента панкреатического сока — ионы бикарбоната и вода — выделяются главным образом эпителиальными клетками канальцев и протоков, которые выходят из ацинусов. Когда поджелудочная железа начинает выделять большие количества панкреатического сока, концентрация иона бикарбоната может повышаться вплоть до 145 мэкв/л. Это приблизительно в 5 раз больше, чем количество ионов бикарбоната в плазме, что создает большое количество щелочи в панкреатическом соке и обеспечивает нейтрализацию соляной кислоты, поступающей из желудка в двенадцатиперстную кишку.
Основные моменты клеточных механизмов секреции раствора бикарбоната натрия в канальцы и протоки поджелудочной железы показаны на рисунке. Они заключаются в следующем.
1. Углекислый газ диффундирует внутрь клетки из крови и под влиянием карбоангидразы соединяется с водой, образуя угольную кислоту (Н2СО3). Угольная кислота, в свою очередь, диссоциирует на ионы бикарбоната (НСО3~) и ионы водорода (Н+). Затем ионы бикарбоната в комплексе с ионами натрия (Na+) активно транспортируются через клеточную мембрану в просвет протока.
2. Ионы водорода, образованные путем диссоциации угольной кислоты внутри клетки, обмениваются на ионы натрия через базалъную часть мембраны клетки путем вторичного активного транспорта. Поступившие ионы натрия транспортируются через клеточную мембрану в просвет панкреатического протока, обеспечивая электрическую нейтральность секретируемым бикарбонатам.
3. Суммарное движение натрия и бикарбонатов из крови в просвет протока создает осмотический градиент давления, который обусловливает также осмотический перенос воды в проток, создавая таким образом почти изоосмолярный раствор бикарбоната натрия.
— Вернуться в оглавление раздела «Физиология человека.»
Оглавление темы «Желудочная и поджелудочная секреция»:
1. Регуляция функции желез пищеварительного тракта. Нервная регуляция секреции желез
2. Секреция воды и электролитов в ЖКТ. Физиология слизи желудочно-кишечного тракта
3. Физиология слюны. Секреция слюны
4. Гигиенические свойства слюны. Нервная регуляция слюноотделения
5. Секреция в пищеводе. Физиология желудочной секреции
6. Физиология секреции пепсиногена. Секреция желудочной слизи и гастрина
7. Стимуляция секреции кислоты в желудке. Стимуляция секреции гастрина
8. Физиология и фазы желудочной секреции. Торможение и регуляция желудочной секреции
9. Строение гастрина. Физиология секреции поджелудочной железы
10. Предотвращение самопереваривания поджелудочной железы. Секреция ионов бикарбоната
Источник
Комментарии
Опубликовано в журнале:
«Клинические перспективы гастроэнтерологии, гепатологии»; №2; 2010; стр. 1-5.
В.Д. Пасечников, И.Л. Литвиненко
Ставропольская государственная медицинская академия
Цель исследования. Проверка предположения об улучшении эффективности заместительной терапии хронического панкреатита ферментами в энтеросолюбильной оболочке посредством совместного назначения с ингибитором протонной помпы.
Материал и методы. Экзокринная недостаточность поджелудочной железы диагностировалась посредством определения фекальной эластазы-1 и уровня фекального жира/24 часа методом кислотного стеатокрита. По результатам клинических и лабораторных исследований проанализирована эффективность комбинированной терапии панкреатином в форме мини-микросфер и омепразолом (Омез, Dr. Reddy’s).
Результаты. Установлено, что назначение панкреатина в энтеросолюбильной оболочке в форме мини-микросфер эффективно компенсирует признаки экзокринной недостаточности у части больных и не требует дополнительного назначения омепразола.
Выводы. Комбинированная терапия панкреатином в форме мини-микросфер и омепразолом обусловливает значительное улучшение и даже нормализацию усвоения жира у большинства пациентов с экзокринной недостаточностью поджелудочной железы.
Ключевые слова: хронический панкреатит, экзокринная недостаточность поджелудочной железы, заместительная терапия, мини-микросферы панкреатина, омепразол.
Improvement of treatment of exocrine pancreatic insufficiency by combination of enteric-coated pancreatin and proton pump inhibitor
V.D. Pasechnikov, I.L. Litvinenko
Aim of investigation. To evaluate the assumption of improvement of efficacy of substitution therapy of chronic pancreatitis by enteric-coated enzymes in combination to proton pump inhibitor.
Methods. Exocrine pancreatic insufficiency was diagnosed by assessment of fecal elastase-1 and level of fecal fat for 24 hours by acid steatocrit method. By results of clinical and laboratory studies efficacy of combined treatment by pancreatin mini-microspheres and omeprazole (Omez, Dr. Reddy’s) was analyzed.
Results. It was found, that prescription of pancreatin as enteric-coated mini-microspheres efficiently compensates signs of exocrine insufficiency in part of patients and does not require additional prescription of omeprazole.
Conclusions. The combined therapy by pancreatin mini-microspheres and omeprazole (Omez) causes significant improvement and even normalization of fat digestion at the majority of patients with exocrine pancreatic insufficiency.
Кеу words: chronic pancreatitis, exocrine pancreatic insufficiency, substitution therapy, mini-microspheres of pancreatin, omeprazole.
Мальдигестия и мальабсорбция жира с развитием стеатореи являются основной проблемой в лечении экзокринной недостаточности поджелудочной железы [1, 2]. У пациентов с экзокринной недостаточностью поджелудочной железы часто снижена секреция бикарбоната поджелудочной железой, который неспособен нейтрализовать кислотность химуса, опорожняющегося из желудка [16]. Когда для заместительной терапии используются ферменты, не защищенные кислотоустойчивой оболочкой, ингибирование секреции соляной кислоты желудком является необходимым условием сохранения ферментов (в особенности липазы), легко разрушающихся в кислой среде [10]. Кроме того, кислая среда является причиной преципитации желчи в просвете двенадцатиперстной кишки (ДПК), что также снижает пищеварение жира. Современные лекарственные формы (мини-микросферы) имеют защитную энтеро-солюбильную оболочку, позволяющую предотвратить инактивацию ферментов [12]. Однако при низком уровне рН (<5) в просвете ДПК их энтеросолюбильная оболочка не растворяется, ферменты высвобождаются в дистальных отделах тонкой кишки, эффективность заместительной терапии снижается вследствие быстрой инактивации липазы [4, 9]. У здорового человека содержание липазы за пределами связки Трейтца составляет всего 8% от ее уровня в ДПК [5].
Известно, что существуют две группы пациентов, различным образом реагирующих на заместительную терапию ферментами. Более чем у половины пациентов стеаторея исчезает вследствие улучшения расщепления и всасывания жира [7]. Это может быть объяснено сохранением продукции бикарбонатов или редуцированной секрецией кислоты у этих пациентов. Другая часть пациентов неудовлетворительно воспринимает заместительную терапию ферментами в энтеросолюбильной оболочке, а значительное увеличение эффективности наступает после дополнительного назначения ингибиторов протонной помпы (ИПП). У этих пациентов нормальная или высокая желудочная секреция сочетаются со снижением продукции бикарбоната поджелудочной железой [7]. В двенадцатиперстной кишке уровень рН снижается вследствие поступления химуса, пропитанного кислотой из желудка, желчные кислоты преципитируются, а ферменты не высвобождаются из энтеросолюбильной оболочки. Добавление в терапию ИПП приводит к нормализации или к существенному улучшению мальдигестии жира и коррекции ответа на заместительную терапию ферментами [7].
Цель нашего исследования -проверка гипотезы о повышении эффективности заместительной терапии ферментами в энтеросолюбильной оболочке посредством совместного назначения с ингибитором протонной помпы.
Материалы и методы
Дизайн исследования
По дизайну исследование квалифицируется как рандомизированное, проспективное, последовательное, сравнительное, открытое по клиническим и лабораторным критериям оценки эффективности терапии ферментами в энтеросолюбильной оболочке (30 000 ЕД липазы с каждым приемом пищи) в двух группах пациентов с хроническим панкреатитом, получавших только ферментные препараты или их комбинацию с омепразолом (Омез, Dr. Reddy’s) в режиме 20 мг дважды в сутки за 30 мин до приема пищи в течение месяца.
Критерии включения: пациенты (мужчины и женщины) в возрасте от 18 до 60 лет с хроническим панкреатитом различной этиологии, проявляющимся экзокринной панкреатической недостаточностью.
Все пациенты, удовлетворявшие критериям включения, прекращали принимать медицинские препараты, способные влиять на желудочную секрецию и замещать функцию железы, обычно за 2 нед до начала исследования.
Критерии исключения: пациенты с экзокринной недостаточностью поджелудочной железы, обусловленной опухолями органа, резекцией части железы или желудка, муковисцидозом, синдромом Золлингера-Эллисона, целиакией, с избыточным бактериальным ростом в тонкой кишке и лямблиозом.
После проведения обследования все больные подлежали рандомизации. Используя метод генерации случайных чисел каждому пациенту, с критерием включения присваивали номер, который соответствовал назначению терапии по схеме, включающей либо только панкреатины, либо комбинацию панкреатина с омепразолом.
Первая группа (20 человек) пациентов принимали защищенные панкреатины в виде мини-микросфер во время каждого приема пищи (минимум 25 000 ЕД липазы на каждый прием 3-4 раза в сутки) в течение месяца, вторая группа (20 человек) — защищенные панкреатины в том же режиме приема, что и первая группа, в комбинации с омепразолом (Омез, Dr. Reddy’s), принимаемым в суточной дозе 40 мг в два приема за 30 мин до завтрака и за 30 мин до ужина также в течение месяца.
Эффективность терапии (через месяц от начала) оценивалась по клиническим и лабораторным критериям. Клинические критерии включали увеличение массы тела, уменьшение вздутия, и/или абдоминальной боли, и/или диареи. Лабораторными критериями служило уменьшение (прекращение) стеатореи (определение нейтрального жира в фекалиях).
Перед началом исследования от пациентов получали письменное информированное согласие на участие в исследовании, разрешенное местным научным этическим комитетом в соответствии с принципами Хельсинкской декларации.
Методы исследования
Пациентам проводили эндоскопическое исследование верхних отделов желудочно-кишечного тракта, ультразвуковое или магнитно-резонансное исследование поджелудочной железы.
Для оценки нарушения экзокринной функции использовали определение уровня фекальной эластазы-1 иммуноферментным методом с помощью тест-наборов фирмы ScheBo-Tech [6] и уровня фекального жира/24 часа методом кислотного стеатокрита [3, 8].
Для исключения целиакии проводили исследование антител к глиадину иммуноферментным методом, лямблиоза — микроскопией мазков из фекалий и дуоденального содержимого, синдрома избыточного роста бактерий -дыхательным водородным тестом с лактулозой при помощи газового анализатора «Gastrolyzer» (Великобритания).
Диагноз хронического панкреатита устанавливался в соответствии с критериями Римско-Марсельской классификации [13], основывался на клинических симптомах и подтверждался ультра-сонографией, компьютерной или магнитно-резонансной томографией, эндоскопической ретроградной холангиопанкреатографией.
Результаты исследования
В исследование включено 40 пациентов (32 мужчины, 8 женщин) в возрасте от 23 до 65 лет (средний возраст 52,3±11,4 года) с подтвержденным диагнозом хронического панкреатита.
Экзокринная недостаточность поджелудочной железы у пациентов, включенных в исследование, была установлена на основании определения эластазы-1 в фекальном содержимом у пациентов обеих групп (рис. 1). Выраженность экзокринной недостаточности в обеих группах была одинаковой (уровни эластазы-1 в фекальном содержимом не имели достоверных различий).
Рис. 1. Концентрация эластазы-1 в фекальном содержимом у больных, получавших заместительную терапию ферментами (мини-микросферы в энтеросолюбильной оболочке) и комбинацию ферментов с омепразолом (Омез, Dr. Reddy’s)
Известно, что определение фекальной эластазы является полноценной клинической альтернативой прямым методам исследования экзокринной функции поджелудочной железы вследствие высокой чувствительности и специфичности [11]. Тест с использованием эластазы пригоден для долговременного мониторирования экзокринной функции поджелудочной железы и решения вопроса о времени начала заместительной терапии [14].
Установлено, что уровень фекальной эластазы-1 менее чем 100 мкг/г стула свидетельствует о тяжелой, уровень 100-200 — об умеренной недостаточности функции поджелудочной железы, а свыше 200 мкг/г стула считается нормальным уровнем [11].
При сравнении динамики показателя фекального жира до и после терапии выявлено (рис. 2А), что назначение защищенного панкреатина не привело к достоверному изменению этого показателя (9,45±4,1 г/24 часа и 6,45±4,1 г/24 часа соответственно [95% интервал для разности от -6,736 до 14,74; t=0,517, p=0,608]). Следует отметить, что у части пациентов группы, получавшей только заместительную терапию, показатели стеатореи снизились (11 из 20, 55%), у некоторых не изменились (2 из 20, 10%) и у части (7 из 20, 35%) повысились.
Напротив, в группе, получавшей комбинированную терапию (рис. 2 B), достоверно снизился показатель фекального жира (11,23±3,6 г/24 часа и 2,26±2,1 г/24 часа соответственно [95% интервал для разности от 0,5329 до 17,41; t=2,152, p=0,036]). В этой группе у подавляющего числа пациентов (15 субъектов, 75%) показатели фекального жира уменьшились по сравнению с показателями до начала терапии, а у 5 больных (25%) повысились.
Рис. 2. Концентрация жира в фекальном содержимом у больных, получавших заместительную терапию: А. Ферменты (мини-микросферы в энтеросолюбильной оболочке); В. Комбинация ферментов с омепразолом (Омез, Dr. Reddy’s)
Dominguez-Munoz J.E. и соавт. [7], используя дыхательный тест с субстратом в виде смеси триглицеридов, меченных изотопом углерода (13C-MTG), показали, что заместительная терапия мини-микросферами панкреатина (40 000 Eur Ph U/прием пищи) в энтеросолюбильной оболочке в течение трех месяцев привела к нормализации абсорбции жира у 57% пациентов. Дополнительное назначение 40 мг эзомепразола за 30 мин до завтрака в течение 2 нед этим субъектам не повысило эффект заместительной терапии. У оставшейся части пациентов (43%) с персистирующей мальдигестией жира, несмотря на проведенную заместительную терапию ферментами в том же режиме и дозе, назначение 40 мг эзомепразола за 30 мин до завтрака в течение 2 нед обеспечило нормализацию усвоения жиров у 67%, значительное улучшение у 14,3%.
У части пациентов (13,7% от общего числа всех пациентов) мальдигестия жира персистировала, несмотря на комбинированную терапию панкреатином совместно с эзомепразолом.
Результаты исследования Dominguez-Munoz J.E. и соавт. [7] совпадают с полученными нами (соотношение лиц, ответивших на заместительную терапию, 57 и 55% соответственно). В группе больных, получавших комбинированную терапию, пропорции больных, ответивших на терапию, также были сравнимы: 75 и 81,3% соответственно.
Таким образом, собственные результаты и данные исследования Dominguez-Munoz J.E. и соавт. [7] выявили наличие двух различных популяций пациентов с различным ответом на заместительную терапию ферментами в энтеросолюбильной оболочке. С одной стороны, более чем у половины пациентов заместительная терапия обусловила нормализацию пищеварения. Это может быть объяснено наличием у них сохраненной продукции бикарбонатов и(или) сниженной желудочной секреции. С другой стороны, у значительной части пациентов терапия не привела к отчетливому улучшению пищеварения. В случае изначального применения комбинированной терапии ферментами и омепразолом пропорция ответивших на лечение пациентов существенно увеличивается — до 75%. При неудовлетворительном ответе на заместительную терапию ферментами дополнительное назначение эзомепразола также увеличивает пропорцию респондеров — до 81%.
Вероятно, у этой популяции пациентов имелись нормальная или увеличенная желудочная секреция совместно с недостаточной продукцией бикарбоната поджелудочной железой, что привело к закислению химуса и снижению эффективности заместительной терапии.
При сравнении частоты стула до и после терапии установлено (рис. 3), что назначение защищенного энтеросолюбильной оболочкой панкреатина не привело к достоверному изменению этого показателя (6,2±2,8/сутки и 4,5±2,6/сутки соответственно [95% интервал для разности от -6,035 до 9,435; t=0,445, p=0,659]).
Рис. 3. Частота стула у больных, получавших заместительную терапию ферментами (мини-микросферы в энтеросолюбильной оболочке) и комбинацию ферментов с омепразолом (Омез, Dr. Reddy’s)
Напротив, в группе, получавшей комбинированную терапию панкреатина и ИПП, достоверно снизилась частота стула (7,6±2,1/сутки и 2,5±1,4/сутки соответственно [95% интервал для разности от -0,00934 до 10,21; t=2,021, p=0,0495]).
Хотя согласно лабораторным критериям улучшилась мальдигестия, клинические признаки эффективности (снижение частоты стула) не были достоверно значимыми в группе больных, получавших только заместительную терапию ферментами. В то же время комбинированная терапия ферментами и омепразолом обусловила достоверное снижение этого показателя, что ассоциировалось с улучшением пищеварения жира (снижением фекального жира). На наш взгляд, это также свидетельствует о необходимости комбинированной терапии у части пациентов, нуждающихся в коррекции экзокринной функции поджелудочной железы.
Заключение
Использование теста с фекальной эластазой позволяет диагностировать экзокринную недостаточность поджелудочной железы, что предопределяет необходимость назначения заместительной терапии панкреатинами. Комбинированная терапия панкреатином в форме мини-микросфер и омепразолом (Омез, Dr. Reddy’s) значительно улучшает и даже нормализует усвоение жира частью пациентов с экзокринной недостаточностью поджелудочной железы. Терапия панкреатином в энтеро-солюбильной оболочке в форме мини-микросфер эффективна для части больных и не требует дополнительного назначения омепразола. В целях оптимизации терапии (выбор моно- или комбинированной терапии) до ее проведения необходимо установление рН в просвете ДПК; при невозможности определения этого показателя в случае неэффективности терапии панкреатинами рекомендуем комбинацию мини-микросфер ферментов с омепразолом (Омез, Dr. Reddy’s) при повторении курса заместительной терапии.
Список литературы
1. Буклис Э.Р., Ивашкин В. Т. Хронический панкреатит: этиология, патофизиология и консервативная терапия // Рос. журн. гастроэнтерол., гепатол. колопроктол. — 2006. — № 6. — С. 79-86.
2. Попова Т.Н., Джанашия Е.А., Логинов А.Ф., Селезнев А.В., Калинин А.В. Эффективность препарата «Микразим 10 000 ЕД» в лечении обострения хронического панкреатита с преобладанием болевого синдрома) // Клин. перспект. гастроэнтерол., гепатол. — 2007. — № 2. — С. 1-8.
3. Bijoor A.R., Geetha S., Venkatesh T. Faecal F at Content In Healthy Adults By The ‘Acid Steatocrit Method’ // Indian Journal of Clinical Biochemistry. — 2004. — Vol. 19. — P. 20-22.
4. Delchier J.C., Vidon N., Saint-Marc Girardin M.F. et al. Fate of orally ingested enzymes in pancreatic insufficiency: comparison of two pancreatic enzyme preparations // Aliment Pharmacol Ther. — 1991. — Vol. 5. — P. 365-378.
5. DiMagno E.P.,Malagelada J.R., Go V.L., Moertel C.G. Fate of orally ingested enzymes in pancreatic insufficiency. Comparison of two dosage schedules // N Engl J Med 1977. — 296. — P. 1318-1322.
6. Dominguez-Munoz J.E. Pancreatic Enzyme Therapy for Pancreatic Exocrine Insufficiency // Current Gastroenterology Reports. — 2007. — Vol. 9. — P. 116-122.
7. Dominguez-Munoz J.E., Iglesias-Garcia J., Iglesias-Rey M., Vilarico-Insua M. Optimising the therapy of exocrine pancreatic insufficiency by the association of a proton pump inhibitor to enteric coated pancreatic extracts // Gut. — 2006. — Vol. 55. — P. 10561057.
8. Dumasu V., Delhaye M., Cotton F. Fat Malabsorbtion Screening in Chronic Pancreatitis // Am. J. Gastroenterol. — 2004. -Vol. 99. — P. 1350 — 1354.
9. Guarner L., Rodriguez R., Guarner F. et al. Fate of oral enzymes in pancreatic insufficiency // Gut. — 1993. — Vol. 34. — P. 708712.
10. Holtmann G., Nelly D.G., Sternby B, DiMagno E.P.: Survival of human pancreatic enzymes during small bowel transit: effects of nutrients, bile acids and enzymes // Am J Physiol — 1997. — Vol. 273. — P. G553-G558.
11. Lieb II J.G., Draganov P. V. Pancreatic function testing: Here to stay for the 21st century // World J Gastroenterol. — 2008. — Vol. 14. — P. 3149-3158.
12. Lohr J.-Matthias. Therapy of exocrine pancreatic insufficience. // Exocrine pancreatic insufficience /1-st edition, Bremen:UNI-MED. — 2007. — P. 33-41.
13. Sarles H, Adler G., Dani R. et al. The pancreatitis classification of Marseilles-Rome // Scand J. Gastroenterol. — 1989. — Vol. 24. — P. 641-642.
14. Walkowiak J., Nousia-Arvanitakis S., Agguridaki C. et al. Longitudinal follow-up of exocrine pancreatic function in pancreatic sufficient cystic fibrosis patients using the fecal elastase-1 test // J. Pediatr Gastroenterol Nutr. — 2003. — Vol. 36. — P. 474-478.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник

