Внутренняя секреция поджелудочной железы
Поджелудочная железа осуществляет внешнюю (экзокринную) и внутреннюю (эндокринную) секрецию. Клетки, собранные в составе ацинусов и протоков, секретируют пищеварительные ферменты и выделяют их в просвет кишки. Однако в паренхиме органа располагается особая ткань, морфологически оформленная в виде островков и выполняющая эндокринную функцию. Панкреатические островки, занимающие от 2 до 10 % общей массы органа, не имеют выводных протоков, а выделяют продукты секреции в кровь. Островки, названные по имени описавшего их автора островками Лангерганса, имеют округлую или овальную форму и сравнительно небольшие размеры (50…500мкм). Среди клеток островков Лангерганса выделяют несколько типов, различающихся по величине, форме и окраске.
Ацидофильные клетки (А-клетки, а-клетки) располагаются обычно по периферии островка, имеют округлую, реже полигональную форму. Характерной особенностью А-клеток является наличие в их цитоплазме многочисленных секреторных гранул, представляющих собой округлые тельца высокой электронной плотности, окруженные электронопрозрачным ободком и четко различимой гладкой мембраной. Секреторные гранулы могут располагаться по всей цитоплазме, но чаще концентрируются на полюсе клетки, обращенном к кровеносным сосудам. Секретпродуци-
рующие структурные компоненты А-клеток представлены незначительно шероховатым эндоплазматическим ретикулумом: немногочисленные каналы, свободных рибосом в гиалоплазме немного, и они собраны в небольшие полисомные группы. Комплекс Гольджи обнаруживается не во всех А-клетках, а при наличии этой структуры внутри уплощенных пузырьков (в расширенных концевых отделах) находятся локальные сгущения материала, идентичного содержимому секреторных гранул. По данным иммуногистохимии, А-клетки имеют непосредственное отношение к продукции одного из гормонов поджелудочной железы — глюкагона.
Базофильные клетки (В-клетки, (3-клетки) составляют клеточную основу, имеют полигональную или призматическую форму и занимают центральную часть островка. Цитоплазма В-клеток содержит многочисленные секреторные гранулы, отличающиеся от соответствующих гранул А-клеток своими размерами; они несколько крупнее (диаметр около 350 нм) и имеют меньшую электронную плотность. Секреторные гранулы располагаются в секреторных везикулах эксцентрично и окружены более широким электронопрозрачным ободком, причем мембрана везикулы обычно имеет извилистые контуры. Морфологической особенностью секреторных гранул В-клеток у кошек и собак является характерный вид кристаллоида — прямоугольные палочки. Сек-ретпродуцирующие структурные компоненты клеток — эндоплаз-матический ретикулум и комплекс Гольджи — представлены в В-клетках более совершенно, чем в А-клетках, они занимают большую площадь клетки, да и сами клетки значительно превышают А-клетки по своим размерам. Исследования В-клеток у различных видов животных с помощью методов меченых атомов и иммуногистохимии выявили, что они обеспечивают продукцию основного гормона поджелудочной железы — инсулина.
Дефинитивные клетки (Д-клетки, 8-клетки) в островках встречаются довольно редко, располагаются поодиночке или небольшими группами, имеют длинные цитоплазматичес-кие отростки, придающие им звездчатую форму. Характерной особенностью Д-клеток является наличие в их цитоплазме специфических секреторных гранул, отличающихся по своей ультраструктуре от А и В-гранул: размеры гранул значительно варьируют (200…400нм), распределены они довольно равномерно, иногда концентрируются в отростках клеток, обращенных к кровеносным сосудам. Д-клетки содержат немногочисленные и слаборазвитые клеточные органеллы, эндоплазматический ретикулум представлен небольшим количеством канальцев, комплекс Гольджи развит незначительно. Функции Д-клеток окончательно не выяснены, но данные иммуногистологического исследования позволяют предполагать возможность в них синтеза гастрина, однако не исключается и образование в них соматостатина, аналог которого продуцируют нейросекреторные образования гипоталамуса.
Рис. 12.10. Схема секреторного процесса в инсулиноците
У млекопитающих поджелудочная железа вырабатывает гормон инсулин — полипептид с молекулярной массой 6000. Для образования инсулина особенно необходим цистеин, на который в молекуле инсулина приходится 12 % всего аминокислотного состава. Образовавшийся в В-клетках инсулин либо сразу поступает в кровоток, либо депонируется в секреторных гранулах с участием цинка (рис. 12.10). В крови инсулин способен связываться с а-, р- и у*гл°бу-линами и достигать тканей, которые способны связывать гормон и специфически реагировать на его присутствие. Вследствие довольно быстрого исчезновения инсулина из кро
веносного русла 20 % его выделяется в неизмененном виде с мочой, остальные 80 % разрушаются инсулиназой печени, почек и мышц — поджелудочная железа должна постоянно продуцировать этот гормон для поддержания определенного уровня углеводного обмена.
Инсулин действует на углеводный, жировой, белковый и минеральный обмены, а также на процессы окислительного фосфорили-рования. В основном его действие проявляется в повышении потребления глюкозы тканями, в результате чего значительно понижается содержание сахара в крови. Развитие гипогликемии при введении инсулина связано с тем, что усиливается утилизация глюкозы: две трети ее количества связывается в печени, а треть в других органах и тканях, где глюкоза либо сгорает с образованием АТФ, либо используется для синтеза гликогена или липидов. Инсулин является единственным гормоном, который понижает содержание глюкозы в крови, тогда как повышение уровня глюкозы может быть вызвано несколькими гормонами, образующимися в различных эндокринных органах. При воздействии инсулина усиливается проникновение глюкозы в скелетные мышцы через клеточную мембрану, при этом активируется деятельность специфических переносчиков. Инсулин способен принимать участие в регуляции обмена белков: стимулирует транспорт аминокислот через клеточные мембраны и включение их в полипептидные цепи, а также повышает биосинтез белка, усиливая нуклеиновый обмен (за счет интенсификации процессов образования информационной РНК и ускорения считывания информации с иРНК в момент образования полисом). Под влиянием инсулина в жировой ткани возрастает количество триглицеридов, обмен глюкозы в ней характеризуется преобладанием пентозофосфатного шунта — источника НАДФ Н2, который необходим для синтеза жирных кислот.
Под влиянием инсулина в крови снижается содержание летучих жирных кислот (ЛЖК), которые используются для образования жира в печени и в других тканях, причем в молочной железе значительно увеличивается содержание молочного жира и белков в образующемся молоке.
При недостатке или отсутствии инсулина в организме возникают серьезные изменения, вызванные прежде всего тем, что клетки печени, мышечной ткани перестают извлекать глюкозу из крови за счет нарушения мембранной транспортной системы. Содержание глюкозы в крови значительно повышается, и поскольку гипергликемия обусловливает повышение содержания глюкозы в первичной моче, то почки не справляются с процессом реабсорб-ции и часть Сахаров выделяется с мочой — развивается глюкозо-урия («сахарное мочеизнурение»). Вследствие повышения осмотического давления мочи ее объем увеличивается, что приводит к полиурии. В результате развивается дегидратация организма, уменьшается объем циркулирующей крови, снижается артериальное давление и нарушается микроциркуляция. Несмотря на повышенное содержание глюкозы в крови ткани за счет невозможности ее использовать, испытывают недостаток в источниках энергии («голод среди изобилия»).
В ходе глнжонеогенеза в тканях начинается распад белков, аминокислоты используются для построения глюкозы, уровень которой в крови еще более повышается. Наряду с этим происходит мобилизация депонированного жира и, как следствие, увеличение содержания в крови жирных кислот, которые в печени превращаются в кетоновые тела — ацетон, ацетоуксусную и бета-оксимасляную кислоты. Обычно эти соединения могут использоваться клетками, за исключением клеток головного мозга, но при интенсивном образовании кетоновых тел организм не способен окислить или метаболизировать их и кетоновые тела меняют рН крови, приводя к ацидозу и исчерпанию щелочных резервов бикарбонатов плазмы. Даже при усиленном дыхании и гипервентиляции легких в крови накапливается углекислота; если рН крови падает ниже 7,0, то развивается коматозное состояние, ведущее к смерти. Кроме того, ацидоз подавляет поступление глюкозы в клетки головного мозга, снижается почти в два раза и потребление ими кислорода, в результате нарушается синтез АТФ, уменьшается содержание кальция и фосфора, происходит потеря сознания, снижение артериального давления и ослабление сердечной деятельности.
Другой гормон поджелудочной железы — глюкагон, природный антагонист инсулина, имеет полипептидную структуру, состоящую из 29 аминокислотных остатков. Глюкагон (молекулярная масса 3485) участвует в регуляции углеводного обмена за счет интенсификации распада гликогена печени до глюкозы, одновременно подавляет синтез гликогена и значительно повышает содержание глюкозы в крови в противоположность инсулину.
Вместе с этим гипергликемический эффект усиливается за счет глюконеогенеза — превращения дезаминированных аминокислот в глюкозу. Влияние глюкагона на липидный обмен проявляется в активации липаз, расщепляющих триглицериды с образованием свободных жирных кислот. Участвуя в минеральном обмене, глю-
кагон усиливает выведение натрия, калия, кальция и хлора с мочой и снижает количество неорганического фосфата в плазме крови. На примере внутриклеточных эффектов глюкагона впервые была выяснена роль аденилатциклазы и циклических нуклеотидов (цАМФ) в реализации действия пептидных гормонов. При активации аденилатциклазы и увеличении содержания внутриклеточной цАМФ происходит усиление активности фосфорилазы печеночных клеток, что приводит к увеличению содержания глю-козо-1 -фосфата и глюкозо-6-фосфата.
Хотя островки Лангерганса секретируют два гормона противоположного действия, последствия поражения островковой ткани в результате вирусной инфекции или после удаления поджелудочной железы оказываются фатальными за счет прекращения физиологического действия инсулина, так как глюкагон может помимо поджелудочной железы синтезироваться в желудочно-кишечном тракте. Кроме того, аналогичным глюкагону действием обладают гормон роста, кортизол, адреналин и тироксин.
Нарушение транспорта глюкозы через клеточные мембраны может происходить и при неизменной продукции инсулина: из-за нарушения рецепторного связывания инсулина клетки гормонзависи-мых тканей нечувствительны к «команде», исходящей из бета-клеток инкреторного отдела поджелудочной железы.
Гормоны поджелудочной железы выделяются в кровь непрерывно, однако интенсивность их поступления может существенно изменяться в соответствии с физиологическим состоянием организма. Островковая ткань находится под контролем вегетативной нервной системы, и парасимпатические нервные влияния, воспроизводимые раздражением блуждающих нервов, приводят к выбросу инсулина и развитию гипогликемии. Однако денервация железы либо ее пересадка не приводят к прекращению продукции инсулина, что свидетельствует о наличии и другого регуляторного механизма. Основным фактором, определяющим уровень секреции инсулина, является концентрация глюкозы в притекающей к поджелудочной железе крови. При повышении содержания глюкозы в крови увеличивается выделение инсулина и снижается секреция глюкагона, причем выделение глюкагона определяется концентрацией Сахаров в крови по принципу обратной связи. Выделение инсулина в кровь может начинаться в результате срабатывания опережающей связи: когда глюкоза еще находится в тонком кишечнике, местная эндокринная система желудочно-кишечного тракта до повышения концентрации Сахаров в крови за счет влияния секретина и панкреозимина способна активизировать продукцию инсулина.
Концентрация глюкозы в крови существенно меняется в зависимости от типа пищи. При поступлении в организм углеводистых кормов повышение содержания инсулина способствует отложению питательных веществ в виде гликогена в печени и мышцах, жира — в жировых депо. Торможение секреции глюкагона и высокая концентрация глюкозы в крови предотвращают глюко-неогенез, и большая часть аминокислот участвует в белковом синтезе. При преобладании в рационе белков и дефиците углеводов возникает угроза гипогликемии, что особо опасно для тканей мозга, использующих в качестве энергетического метаболита глюкозу.
Благодаря секреции глюкагона в этой ситуации повышается уровень глюкозы в крови.
При приеме пищи, богатой жирами, также необходима интенсификация секреции глюкагона. Активируя липазу, за счет расщепления триглицеридов повышается в крови уровень свободных жирных кислот, которые в печени превращаются в ацетилКоА и участвуют в синтезе глюкозы. В условиях голодания образование инсулина подавляется, а увеличивается влияние глюкагона. Жировая ткань подвергается липолизу, свободные жирные кислоты либо используются непосредственно в тканях, либо преобразуются в печени в кетоновые тела, также участвующие в энергетическом метаболизме. Расщепление гликогена до глюкозы обеспечивает большую часть потребностей тканей мозга, и в последующем при продолжении голодания для обеспечения питательными веществами жизненно важных органов при совместном действии глюкагона, адреналина, АКТГ и кортикостероидов начинается расщепление белков тканей и образование глюкозы из аминокислот.
Таким образом, инсулин и глюкагон вместе осуществляют гормональный контроль обмена веществ. За счет изменения соотношения этих гормонов предотвращается расточительная трата питательных веществ после приема пищи: излишняя глюкоза не выводится с мочой, а запасается в виде гликогена и жиров. Между приемами пищи соотношение инсулин — глюкагон устанавливается таким образом, чтобы обеспечивались потребности жизненно важных органов. Интенсивные мышечные нагрузки вызывают выделение в кровь глюкагона, необходимого для срочного обеспечения мышечной ткани повышенным количеством глюкозы. Таким образом, при всей противоположности влияния этих гормонов на уровень глюкозы синергизм инсулина и глюкагона обеспечивает наиболее полное усвоение и окисление углеводов.
Совместная локализация инсулин- и глюкагон-продуцирующих клеток в пределах островка Лангерганса предопределяет наличие функциональной связи, которая проявляется в том, что глюкагон способен стимулировать секрецию инсулина, а выделяющийся из Д-клеток соматостатин тормозит секрецию и инсулина, и глюкагона. Наряду с соматостатином выделение инсулина тормозят физиологически активные вещества симпатического отдела вегетативной нервной системы и мозгового вещества надпочечников — адреналин и норадреналин. В то же время катехоламины оказывают стимулирующие воздействия на альфа-клетки поджелудочной железы, продуцирующие глюкагон.
studopedia.su — Студопедия (2013 — 2019) год. Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав
Источник
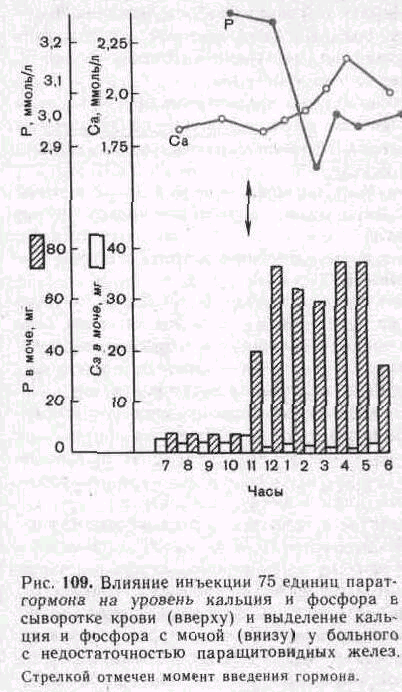
желез
обусловлены нарушением состояния ЦНС.
После перерезки двигательных нервов
судороги денервированных мышц не
возникают.
Паратиреопривная
тетания развивается вследствие
понижения уровня кальция в крови и
спинномозговой жидкости. Введение
солей кальция таким животным предупреждает
развитие тетании. При тетании нарушаются
также функции печени; в крови обнаруживается
токсичный карбаминово-кислый аммоний.
При
недостаточности внутрисекреторной
функции околощитовидных желез у человека
(гипопаратиреоз) вследствие падения
уровня кальция в крови резко повышается
возбудимость ЦНС и возникают приступы
судорог. При скрытой тетании, возникающей
при легкой недостаточности околощитовидных
желез, судороги мышц лица и рук появляются
только при надавливании на нерв,
иннервирующий эти мышцы.
У
детей с врожденной недостаточностью
паращитовидных желез содержание кальция
в крови снижено, нарушен рост костей,
зубов и волос, наблюдаются длительные
сокращения мышечных групп (предплечья,
грудной клетки, глотки и др.).
Избыточная
функция (гиперпарати-реоз) околощитовидных
желез наблюдается довольно редко,
например при опухоли околощитовидной
железы. При этом содержание кальция
в крови увеличено, а количество
неорганического фосфата уменьшено.
Развивается остеопороз, т. е. разрушение
костной ткани, мышечная слабость
(вынуждающая больного постоянно лежать),
боли в спине, ногах и руках. Своевременное
удаление опухоли восстанавливает
нормальное состояние.
Околощитовидные
железы продуцируют паратгормон.
При недостатке паратгормона понижается,
а при избытке повышается содержание
кальция в крови. Одновременно в первом
случае увеличивается содержание в крови
фосфатов и уменьшается их выделение
с мочой, а во втором случае
—
понижается количество фосфатов в крови
и повышается их выделение с мочой.
Паратгормон активирует функцию
остеокластов, разрушающих костную
ткань.
В
организме паратгормон вызывает разрушение
костной ткани с выходом из нее ионов
кальция (вследствие чего и повышается
их концентрация в крови). Паратгормон
усиливает всасывание кальция в кишечнике
и процессы его реабсорбции в канальцах
почди. Все это ведет к значительному
нарастанию уровня кальция в крови
(вместо нормальных
9—11
мг% до
18
мг% и выше). Одновременно снижается
концентрация неорганических фосфатов
в крови и увеличивается их выделение с
мочой (рис.
109).
В
норме концентрация ионов
Ca2’1′
в плазме крови поддерживается на
постоянном уровне, являясь одним из
наиболее точно регулируемых параметров
внутренней среды. Падение уровня кальция
в крови, омывающей железу, приводит к
усилению секреции паратгормона и,
следовательно, к увеличению поступления
кальция в кровь из его костных депо.
Наоборот, повышение содержания этого
электролита в крови, омывающей
паращитовидные железы, непосредственно
угнетает выделение паратгормона (и
усиливает образование тирокальцитонина),
в результате чего количество кальция
в крови снижается. Таким образом,
между содержанием кальция в крови и
внутренней секрецией околощитовидных
желез (и парафолликулярных клеток
щитовидной железы) имеется непосредственная
двусторонняя связь: смещение концентрации
кальция в омывающей их крови вызывает
изменения секреции тирокальцитонина
и паратгормона, а последние регулируют
содержание кальция в крови.
Указанные
реакции железы на изменение содержания
Са24″
в крови не опосредованы какими-либо
нервными или гуморальными механизмами.
Они являются прямыми и возникают не
только в целом организме, но и при
перфузии изолированной железы кровью,
содержащей .большее или меньшее по
сравнению с нормой количество кальция.
Гистологическими
исследованиями поджелудочной железы
установлено, что в ней наряду с секреторным
эпителием, выделяющим пищеварительные
ферменты, существуют особые группы
клеток
—
белые отростчатые эпидермоциты (островки
Лангерганса
— по
имени открывшего их исследователя).
Эти эпидермоциты не имеют выводных
прртоков и выделяют свой секрет
непосредственно в кровь.
Еще
в конце
XIX
в. было установлено, что у собаки через
4—5
ч после удаления поджелудочной железы
начинается выделение сахара с мочой.
Резко повышается содержание глюкозы
в крови. Потеря сахара с мочой приводит
к тому, что животное худеет, пьет
много воды, становится прожорливым.
Все
эти явления оказались аналогичны тем,,
которые наблюдаются у человека при
сахарном диабете. После пересадки
животному поджелудочной железы в
какой-либо другой участок тела,
например под кожу, проявления сахарного
диабета исчезали.
Для
сахарного диабета характерно повышение
содержания глюкозы в крови (гипер-гликемия)
до
10
ммоль/л
(200
мг%) и даже больше, вместо 4,4±1,1 ммоль/л
(100— 120
мг%) в норме. Это связано с тем, что при
диабете поступившая в кровь глюкоза не
полностью утилизируется тканями и не
превращается в гликоген печени.
Повышение
содержания глюкозы в крови, а следовательно,
и в клубочковом фильтрате приводит
к тому, что эпителий почечных канальцев
не реабсорбирует глюкозу полностью,
вследствие чего она выделяется с мочой
(глюкозурия). Возникает потеря сахара
с мочой
—
сахарное мочеизнурение.
Количество
мочи увеличено (полиурия). Причина этого
явления заключается в том, что при
большом содержании глюкозы в моче
почечных канальцев эта нереабсорбиро-ванная
глюкоза, создавая высокое осмотическое
давление мочи, удерживает в ней воду.
Последняя недостаточно всасывается
канальцами, и количество выделяемой
почками мочи оказывается увеличенным.
Обеднение организма водой вызывает у
больных диабетом сильную жажду, что
приводит к обильному приему воды
(полидипсия). В связи с выведением глюкозы
с мочой резко увеличивается расходование
белков и жиров в качестве веществ,
обеспечивающих энергетический обмен
организма. Об усилении процессов
сгорания жиров и белков свидетельствует
снижение дыхательного коэффициента
нередко до
0,7.
В
организме накапливаются продукты
неполного окисления жиров, к числу
которых относятся кетоновые тела:
Р-оксимасляная и ацетоуксусная кислоты.
В
тяжелых случаях интенсивное образование
кислых продуктов расщепления жиров и
дезаминирование аминокислот в печени
вызывают сдвиг активной реакции крови
в кислую сторону
—
ацидоз.
Накопление
кетокислот и ацидоз могут вызывать
тяжелое, угрожающее смертью состояние
—
диабетическую кому, которая протекает
с потерей сознания, нарушением дыхания
и кровообращения.
Описанные
расстройства связаны со снижением
гормональной функции поджелудочной
железы.
Гормоны поджелудочной железы
Белые
отростчатые эпидермоциты (островки
Лангерганса) состоят из клеток трех
типов: а-, |3- и ^-клеток. Среди них больше
всего (З-клеток (у собак около
75 %);
они небольших размеров и имеют
зернистую протоплазму.
Бета-клетки
выделяют инсулин
(от латинского слова
insula—островок).
Альфа-клетки островков вырабатывают
гормон глюкагон.
По
данным некоторых авторов, эпителии
мелких протоков поджелудочной железы
выделяет гормон липокаин. В экстрактах
этой железы найдены еще два гормона
— ваготонин
и центропнеин.
Инсулин.
Попытки извлечь из поджелудочной железы
инсулин долгое время оставались
тщетными, так как этот гормон является
полипептидом и разрушается трипсином,
содержащимся в ткани вырезанной из
организма поджелудочной железы.
В
1902
г. Л. В. Соболев предложил два способа,
позволяющих предотвратить разрушение
инсулина. Один из этих способов
состоит в том, что у животного перевязывают
протоки поджелудочной железы за несколько
дней до ее удаления. Это вызывает
дегенерацию и гибель внешнесекретор-ного
эпителия. Вследствие этого в железе не
содержится более сока, который мог бы
вызвать ферментативное расщепление
инсулина. Второй способ состоит в том,
что инсулин получают из поджелудочной
железы эмбрионов, в которой еще не
образуется пищеварительных ферментов.
В
1922
г. Бантинг и Бест, применив первый из
этих способов, получили активные
препараты инсулина. Инсулин является
лечебным средством при диабете. Он
поддерживает жизнь не менее чем
30
млн. живущих на планете больных
диабетом, причем
30—40%
из них нуждаются в постоянном ежедневном
введении инсулина.
Инсулин
(полипептид) удалось синтезировать
химическим путем. Это был первый белок,
полученный синтетически вне организма.
Инсулин, полученный из поджелудочной
железы разных видов животных, различается
расположением аминокислот в молекуле.
Молекула инсулина не содержит цинка,
однако способна связывать цинк; при
этом эффект действия инсулина удлиняется
и усиливается.
Инсулин
резко повышает проницаемость мембраны
мышечных и жировых клеток для глюкозы.
Вследствие этого скорость перехода
глюкозы внутрь этих клеток увеличивается
примерно в
20
раз по сравнению со скоростью перехода
глюкозы в клетки в среде, не содержащей
инсулина.
Ферментативные
реакции, приводящие к утилизации
глюкозы,—.
фосфорилирование и окисление ее, а также
образование гликогена протекают внутри
клетки. Способствуя транспорту глюкозы
внутрь клетки, инсулин тем самым
обеспечивает ее утилизацию. Вместе с
тем он не оказывает влияния на утилизацию
углеводов бесклеточными гомоге-натами
тканей (гомогенаты получают путем
растирания клеток, при котором разрушаются
клеточные мембраны), так как механизм
влияния инсулина на углеводный обмен
связан именно с действием его на
проницаемость клеточной мембраны.
Увеличение
транспорта глюкозы через мембраны
мышечных волокон при действии инсулина
способствует синтезу гликогена и
накоплению его в мышечных волокнах. В
клетках жировой ткани инсулин стимулирует
образование жира из глюкозы.
Под
влиянием инсулина возрастает проницаемость
клеточной мембраны и для аминокислот,
из которых в клетках синтезируются
белки. Инсулин стимулирует синтез
информационной РНК и этим также
способствует синтезу белков.
Мембраны
клеток печени в отличие от мембраны
клеток жировой ткани и мышечных
волокон свободно проницаемы для глюкозы
и в отсутствие инсулина. Предполагают,
что этот гормон действует непосредственно
на углеводный обмен печеночных клеток,
активируя синтез гликогена.
Возникающий
после введения больших доз инсулина
переход значительного количества
глюкозы из плазмы крови внутрь клеток
скелетной мускулатуры, сердечной мышцы,
гладких мышц, молочной железы и некоторых
других /органов вызывает падение уровня
глюкозы в крови и вследствие этого
недостаточное поступление глюкозы в
клетки
нервной системы (на проницаемость
которых инсулин не действует). Поэтому
головной и спинной мозг начинает
испытывать острый недостаток глюкозы,
которая является основным источником
энергии для нервных клеток. Когда
содержание сахара в крови падает до
2,5
ммоль/л
(45—50
мг%) возникает острое нарушение
деятельности мозга
— гипогликемическая
кома. Появляются периодические приступы
судорог, затем падение мышечного тонуса,
понижение температуры тела, потеря
сознания. Гипогликемическая кома может
возникать даже под влиянием небольшой
дозы инсулина, если он вводится натощак,
когда глюкоза из пищеварительного
тракта в кровь не поступает. Внутривенное
введение раствора глюкозы немедленно
купирует гипогликемическую кому.
Глюкагон.
Второй гормон поджелудочной железы
—
глюкагон
—
выделяется а-клетками белых отростчатых
эпидермоцитов. Глюкагон стимулирует
внутри клетки переход неактивной
фосфорилазы (фермента, принимающего
участие в расщеплении гликогена с
образованием глюкозы) в активную форму
и тем самым усиливает расщепление
гликогена (в печени, но не в мышцах),
повышая уровень сахара в крови.
Одновременно глюкагон стимулирует
синтез гликогена в печени из аминокислот.
Глюкагон тормозит синтез жирных
кислот в печени, но активирует печеночную
липазу, способствуя расщеплению
жиров. Он стимулирует также расщепление
жира в жировой ткани. Глюкагон повышает
сократительную функцию миокарда, не
влияя на его возбудимость.
Источник

