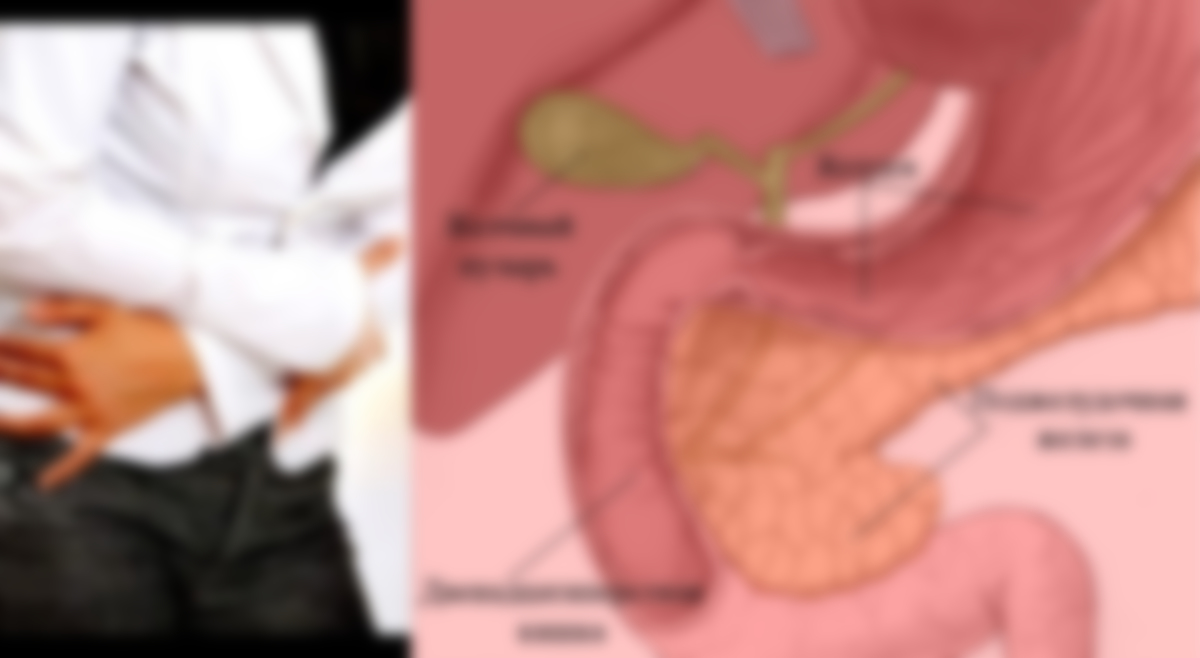
Внутрипротоковый рак поджелудочной железы
Внутрипротоковая папиллярная муцинозная опухоль (ВПМО) – это редкая экзокринная опухоль ПЖ, исходящая из главного панкреатического протока или одной из его ветвей и характеризующаяся секрецией большого количества внеклеточной слизи, сосочковым типом роста, скоплением слизи в панкреатических протоках, высокой степенью резектабельности и хорошим прогнозом, диагноз которой в настоящее время ставится все чаще.
Подобные опухоли продуцируют большое количество муцина, что приводит к прогрессивному расширению главного протока железы и/или кистозному расширению протоков 2–3 порядка в зависимости от локализации опухоли.
ВПМО гистологически различаются и могут представлять собой как малых размеров доброкачественные аденомы, так и инвазивные карциномы с агрессивным типом роста и высокой степенью летальности.
ВПМО имеют более благоприятный прогноз, чем протоковые аденокарциномы ПЖ. Однако они часто предшествуют инвазивной аденокарциноме. Злокачественные опухоли встречаются у 30–90 % пациентов и представляют собой либо карциному in situ , либо инвазивную карциному. ВПМО, являющиеся инвазивной карциномой, имеют значительно худший прогноз, чем другие ВПМО поджелудочной железы.
Клиническая картина и данные объективного исследования
ВПМО встречается на шестом‑седьмом десятилетии жизни у мужчин и женщин приблизительно в равной степени с несколько большей частотой у мужчин. В целом это медленно развивающиеся опухоли с относительно благоприятным прогнозом. От появления первых симптомов до постановки диагноза обычно проходит не меньше года.
От 5 до 30 % ВПМО в момент постановки диагноза имеют злокачественный неинвазивный характер, а 15–40 % – являются инвазивным папиллярно‑муцинозным раком. При этом около половины инвазивных опухолей сопровождается наличием метастазов. Локализация процесса определяет его клиническое течение. До 65 % ВПМО локализуется в головке ПЖ, 30 % – в головке или хвосте железы и в 5‑10 % – отмечено диффузное поражение.
Клиническая картина заболевания определяется избыточной секрецией муцина, что, препятствуя нормальному оттоку панкреатического сока, приводит к постепенному расширению главного протока поджелудочной железы или его ветви, и, как следствие – к постепенно развивающимся явлениям хронического панкреатита. До 70–80 % пациентов предъявляют жалобы на дискомфорт и/или боли в эпигастрии, иррадиацию болей в спину, снижение массы тела. В ряде случаев превалирует клиника острого панкреатита умеренной степени тяжести. Часто встречается длительная гиперамилаземия. Хроническая недостаточность функции ПЖ может приводить к развитию сахарного диабета и/или появлению стеатореи. Нередко развивается желтуха: либо в результате закупорки ампулы фатерового соска вязкой слизью, либо при сдавлении общего желчного протока массивной, обычно злокачественной опухолью, либо при врастании в стенку общего желчного протока солидного компонента опухоли. Тем не менее до 75 % случаев
ВПМО протекает бессимптомно, что может быть обусловлено локализацией вне головки ПЖ или сравнительно низкой степенью продукции муцина.
Диагностика
Трансабдоминальное УЗИ, по данным литературы, считается скрининговым методом исследования при обследовании пациентов с подозрением на ВПМО.
Следует отметить, что использование трех‑и четырехмерной реконструкции ультразвукового изображения значительно повышает диагностическую ценность УЗИ, позволяя более четко дифференцировать сосочковые выросты, а также пристеночные гипоэхогенные массы в просвете протока. При КТ и магнитно‑резонансной томографии ВПМО может иметь веретенообразную форму при поражении ГПП (Вирсунгова протока) или выглядеть как гроздьевидное скопление кистозных структур при долевом и смешанных типах опухоли.
Магнитно‑резонансная холангиопанкреатография (МРХПГ), особенно после введения секретина для расширения протоков ПЖ, может сравниться по точности с результатами классической ретроградной холангиопанкреатографии (РХПГ) и позволяет обнаружить как расширение протоков, так и наличие в их просвете муциновых пробок или папиллярных разрастаний, которых не всегда легко отличить друг от друга. При опухолях боковых ветвей большое значение имеет возможность установить наличие протока, идущего к ГПП, что служит важнейшим диагностическим признаком ВПМО.
Большое значение имеет дифференциальная диагностика с муцинозными кистозными опухолями ПЖ. Они обычно представлены одиночным кистозным образованием с толстой накапливающей контраст фиброзной капсулой, отграничивающей опухоль от остальной ткани железы. При муцинозных кистозных опухолях обычно нет сообщения с протоковой системой железы.
Лечение
Основным методом лечения ВПМО является хирургический. Резектабельность при данном заболевании превышает 80 %, а 5‑летняя выживаемость после резекции составляет 70–80 %, причем в случае доброкачественных или пограничных с морфологической точки зрения образований она приближается к 100 %. Наличие распространения на другие органы ухудшает прогноз.
Опухоль должна быть удалена. Стандартный объем операции – панкреато‑дуоденальная резекция либо дистальная резекция ПЖ, в зависимости от локализации процесса. Экономные резекции ПЖ возможны, но не всегда оправданы и выполнимы технически при доброкачественной опухоли, исходящей из боковых протоков ПЖ.
Тестовые задания для самоконтроля
Выберите один или несколько правильных ответов.
1. Следующие анатомические образования объединяются в понятие «панкреатодуоденальная область»:
1) поджелудочная железа и двенадцатиперстная кишка;
2) большой дуоденальный сосочек, терминальный отдел общего желчного протока;
3) головка поджелудочной железы и большой дуоденальный сосочек;
4) выходной отдел желудка и двенадцатиперстная кишка;
5) поджелудочная железа, двенадцатиперстная кишка и внепеченочные желчные протоки.
2. Наиболее частой патоморфологической формой рака поджелудочной железы является: 1) плоскоклеточный рак;
2) аденокарцинома;
3) гигантоклеточный рак;
4) мелкоклеточный рак;
5) диморфный рак.
3. К инструментальным методам диагностики опухолей панкреатодуоденальной зоны относятся: 1) УЗИ брюшной полости;
2) ФГДС;
3) ЭРХПГ, ЧЧХГ;
4) КТ, МРТ, МРХПГ, ПЭТ;
5) биохимический анализ крови.
4. Максимальная ширина общего желчного протока в норме (визуально и по данным УЗИ) составляет: 1)5 мм и 7 мм соответственно;
2) 8 мм и 6 мм соответственно;
3) 11 мм и 9 мм соответственно;
4) 10 мм и 12 мм соответственно;
5) все перечисленное неверно.
5. Наиболее часто гематогенные метастазы при раке головки поджелудочной железы локализуются: 1) в печени;
2) в плоских костях;
3) в головном мозге;
4) в легких;
5) в почках.
6. Наиболее типичное расположение большого дуоденального сосочка отмечается: 1) в выходном отделе желудка;
2) в тощей кишке;
3) в верхней горизонтальной части 12‑перстной кишки;
4) в нисходящей части 12‑перстной кишки на задневнутренней стенке;
5) в дуоденоеюнальном изгибе.
7. Наиболее характерными симптомами рака головки поджелудочной железы являются: 1) боли в эпигастрии, похудание, расстройства стула;
2) периодическая мелена, рвота застойным желудочным содержимым;
3) повышенная кровоточивость, изжога;
4) желтуха, кожный зуд, лихорадка с ознобами;
5) боли в пояснице, запоры.
8. Основными ультрасонографическими признаками рака головки поджелудочной железы являются: 1) наличие очагового гипоэхогенного узла;
2) расширение главного панкреатического протока;
3) бугристые контуры поджелудочной железы в зоне очагового образования;
4) расширение внутри– и внепеченочных желчных протоков;
5) наличие свободной жидкости в брюшной полости.
9. Обязательным условием для наложения холецистоеюноанастомоза при нерезектабельной опухоли поджелудочной железы является: 1) отсутствие вовлечения в опухолевый процесс воротной вены;
2) ширина холедоха не более 1,5 см;
3) проходимость пузырного протока;
4) отсутствие отдаленных метастазов;
5) отсутствие высокой желтухи.
10. Наиболее информативным инструментальным методом диагностики рака большого дуоденального сосочка является: 1) УЗИ брюшной полости;
2) ФГДС;
3) МРХПГ;
4) релаксационная дуоденография;
5) ЧЧХГ.
11. Основными источниками кровоснабжения головки поджелудочной железы и 12‑перстной кишки являются: 1) аа. gastricae dextra et sinistra;
2) a. lienalis, a. hepatica propria;
3) a. gastroduodenalis, a. mesenterica superior;
4) a. mesenterica inferior, a. hepatica dextra;
5) a. renalis sinistra.
12. Пальпация увеличенного напряженного безболезненного желчного пузыря в сочетании с безболевой желтухой носит название: 1) симптом Воскресенского;
2) симптом Курвуазье;
3) симптом Кохера;
4) симптом Ортнера‑Грекова;
5) симптом Щеткина‑Блюмберга.
13. Дифференциальный диагноз опухоли терминального отдела общего желчного протока следует проводить со следующими заболеваниями: 1) псевдотуморозный головчатый панкреатит;
2) холедохолитиаз;
3) рубцовая стриктура холедоха;
4) опухоль поджелудочной железы;
5) опухоль поперечного отдела ободочной кишки.
14. Радикальная операция уиппла при раке головки поджелудочной железы включает в себя удаление: 1) головки поджелудочной железы;
2) 12‑перстной кишки;
3) дистального отдела общего желчного протока;
4) выходного отдела желудка;
5) поперечного отдела ободочной кишки.
15. Характерным симптомом для проксимальной опухоли внепеченочных желчных протоков является: 1) симптом Курвуазье;
2) желтуха;
3) лихорадка;
4) увеличение печени;
5) кожный зуд.
16. Основным источником кровоснабжения тела и хвоста поджелудочной железы является: 1) правая желудочно‑сальниковая артерия;
2) левая желудочно‑сальниковая артерия;
3) селезеночная артерия;
4) верхняя брыжеечная артерия;
5) общая печеночная артерия.
17. К особенностям клинической картины рака крючковидного отростка поджелудочной железы относится: 1) опухоль рано прорастает в воротную вену и забрюшинную клетчатку;
2) опухоль поздно распространяется на общий желчный проток и осложняется желтухой;
3) как правило, не развивается обтурационный панкреатит ввиду позднего вовлечения главного панкреатического протока;
4) раннее лимфогенное метастазирование;
5) возникновение аррозионных кровотечений.
18. Ультрасонографическими признаками нерезектабельной опухоли панкреатодуоденальной зоны является: 1) расширение внутрипеченочных желчных протоков, увеличение желчного пузыря;
2) асцит, значительное расширение вен портальной системы;
3) наличие опухолевого узла в средней трети холедоха;
4) полость распада в проекции опухолевого узла;
5) расширение Вирсунгова протока.
19. Восстановительный этап панкреатодуоденальной резекции включает следующие элементы: 1) формирование гастро– или дуоденоеюноанастомоза;
2) восстановление пассажа желчи с помощью формирования холедохоеюноанастомоза;
3) обработка культи поджелудочной железы с формированием панкреатикоеюноанастомоза;
4) наложение холецистоеюноанастомоза;
5) наложение илеотрансверзоанастомоза.
20. Радикальная операция при раке большого дуоденального сосочка – это: 1) эндоскопическая папиллэктомия;
2) трансдуоденальная папиллэктомия;
3) панкреатодуоденальная резекция;
4) дуоденэктомия;
5) наложение билиодигестивного анастомоза.
21. Отток венозной крови от органов панкреатодуоденальной области осуществляется в систему: 1) воротной вены;
2) нижней полой вены;
3) верхней полой вены;
4) непарной и полунепарной вен;
5) нижней брыжеечной вены.
22. Наиболее частыми симптомами рака тела и хвоста поджелудочной железы являются: 1) желтуха, диспепсия;
2) боли в верхних отделах живота и спине, потеря массы тела;
3) запоры, кожный зуд, повышенная кровоточивость;
4) систолический шум в эпигастральной области, изжога;
5) ферментативный перитонит.
23. Основным рентгенологическим признаком рака поджелудочной железы при эндоскопической ретроградной холангиопан‑креатикографии является: 1) обрыв тени контрастированного терминального отдела холедоха в виде «кончика сигары»;
2) сужение терминального отдела холедоха в виде «мышиного хвостика»;
3) заброс контрастного вещества в Вирсунгов проток;
4) наличие дефекта наполнения в просвете холедоха;
5) сужение главного панкреатического протока на ограниченном участке.
24. К опухолям поджелудочной железы из нейроэндокринных клеток относится: 1) гастринома;
2) инсулинома;
3) глюкагонома;
4) аденокарцинома;
5) липома.
25. В качестве I этапа оперативного вмешательства по поводу рака большого дуоденального сосочка (БДС) холецистостомия выполняется при: 1) сочетании опухоли БДС и холедохолитиаза;
2) высокой желтухе и резектабельной опухоли;
3) высокой желтухе и нерезектабельной опухоли;
4) наличии отдаленных метастазов;
5) отрицательном симптоме Курвуазье.
Рекомендуемая литература
Основная
Хирургические болезни / ред. Кузин М.И. 3‑е изд., перераб. и доп. М.: Медицина, 2002.
Дополнительная Блохин Н.Н., Итин А. Б., Клименков А. А. Рак поджелудочной железы и внепеченочных желчных путей. М.: Медицина, 1982. 272 с. Данилов М. В., Федоров В. Д. Руководство по хирургии поджелудочной железы. М.: Медицина, 1995. 510 с.
Кубышкин В. А., Вишневский В. А. Рак поджелудочной железы. М.: Медпрактика, 2003. 375 с.
Лапкин К В., Пауткин Ю. Ф. Билиопанкреатодуоденальный рак. М.: Изд‑во Ун‑та дружбы народов, 1991.
Патютко Ю.И., Котельников А. Г. Хирургия рака органов билио‑панкреатодуоденальной зоны. М.: Медицина, 2007. 448 с.
Путов Н.В., Артемьева Н.Н., Коханенко Н.Ю. Рак поджелудочной железы. СПб: Питер, 2005. 395 с.
Общая онкология. Руководство для врачей / Под ред. Н.П. Напалкова. Л.: Медицина, 1989. 468 с.
Источник
Впервые опухоль описана в 1982 г. как новообразование с гиперпродукцией муцина, располагающееся внутри протоков ПЖ с экзофитным ростом в виде сосочков (триада К. Охеши). В течение последующего десятилетия появлялись единичные сообщения о выявлении муцинозных злокачественных опухолей ПЖ, однако отсутствие единого определения не позволяло классифицировать эти находки. Только в 1994 г. для таких опухолей было предложено вышеуказанное название, которое вошло в общепринятую терминологию и сохранилось и по сей день. С тех пор число публикаций, посвященных этой проблеме, резко увеличилось.
Эпидемиология
Внутрипротоковые папиллярные муцинозные опухоли относительно редки, их доля составляет до 3% от всех экзокринных опухолей ПЖ и 18% среди кистозных опухолей ПЖ. Несколько чаще болеют мужчины; возрастной диапазон при первичной диагностике составляет 37—80 лет (чаще 60—70 лет), средний возраст — 64 года. Вероятно, истинная частота внутрипротоковых папиллярных муцинозных опухолей значительно выше, поскольку многим больным выставляют диагноз острого или хронического панкреатита, что обусловлено рядом причин.
Во-первых, средний возраст клинической манифестации этой опухоли составляет 60-70 лет, когда подавляющее большинство больных имеет тяжелые сопутствующие заболевания, каждое из которых может привести к смерти. Во-вторых, аутопсию проводят не у всех больных, а если и выполняют, то при очевидной причине смерти (например, при остром инфаркте миокарда), поэтому ПЖ не уделяют должного внимания. По нашему опыту работы с различными отечественными патоморфологами при отсутствии макроскопически или пальпаторно определяемой опухоли, вскрытие ПЖ по её протоку практически не проводят.
Поскольку опухоль папиллярная, пропальпировать её невозможно, в ряде случаев невозможно даже увидеть её при осмотре макропрепарата (на поперечном срезе протока). Только лишь в том случае, если больной скончался от диагностированного обструктивного панкреатита, причина которого не ясна, есть хороший шанс диагностировать эту опухоль на аутопсии. В-третьих, внутрипротоковая папиллярная опухоль склонна к медленному прогрессированию. Аналогично (с длительно сохраняющимися симптомами) протекает и ХП.
При адекватной лекарственной терапии и отсутствии серьёзного мониторинга (с использованием всех доступных методик визуализации) как исходно, так и в динамике, течение заболевания может продолжаться несколько лет, пока не произойдёт озлокачеетвление со всеми вытекающими последствиями. В-четвёртых, как ни печально это признавать, значительный вктад в гиподиагностику внутрипротоковых папиллярных муцинозных опухолей вносит низкая осведомлённость как практических врачей, так и некоторых морфологов о существовании этой опухоли.
Патоморфология
Опухоль характеризуется внутрипротоковой пролиферацией муцинпродуцирующих клеток, располагающихся в виде сосочков. Гиперсекреция муцина и затруднение оттока секрета при большом количестве сосочков в пределах одного протока может приводить к его кистозному расширению. Если очагов опухолевого роста несколько (фокальный или диффузный тип опухоли), расширение протоков ПЖ выше места сужения может носить ограниченный характер.
Клеточная атипия варьирует от минимальной до тяжёлой, что предполагает подразделение этих опухолей на аденомы, пограничные опухоли и интрацуктальные карциномы (т.е. на доброкачественные, пограничные и злокачественные опухоли). Кроме того, кпеточная дифференцировка может быть различной — интестинальной, панкреатобилиарной и онкокистозной. В основном внутрипротоковые папиллярные муцинозные опухоли растут медленно, однако в 30% случаев они прорастают окружающие ткани и метастазируют. Наиболее частое расположение опухоли — проток ПЖ в проекции её головки. Предполагают, что опухоли, возникшие из второстепенных протоков, имеют лучший прогноз, нежели те, что происходят из основного протока ПЖ.
До сих пор отсутствуют иммуногистохимические и молекулярные маркёры опухоли, не совсем изучены механизмы изменчивости папиллярного компонента, степени секреции муцина, причин вариабельного распространения опухоли и т.п. В ряде случаев эту опухоль крайне трудно отличить от других новообразований, в частности от панкреатической интраэпителиальной неоплазии (PanlNs), поэтому в последние годы в действующую классификацию внесены поправки, благодаря которым можно разграничить эти опухоли.
Этиопатогенез
Этиопагогенез внутрипротоковых папиллярных муцинозных опухолей в настоящее время остаётся загадкой. Интересен следующий факт — такая опухоль, ассоциированная с цистадеиокарциномой, гистологически характеризуется наличием инвазивного компонента с трубчатой или муцинозной структурой. Тубулярная инвазия имеет сходство с протоковой цистадеиокарциномой, в то время как муцинозная часть опухоли представлена коллоидом (муцинозная некистозная карцинома). Кроме того, внутрипротоковые папиллярные опухоли с тубулярной, подобной протоковой иистаденокарциноме, инвазией, характеризуются панкреатобилиарным типом дифференцировки клеток, в то время как опухоль с муцинозноподобной инвазией характеризуется гастроинтестинальным фенотипом.
Исследования последних лет, в некоторой степени приоткрывающие завесу таинственности над патогенезом этой опухоли, посвящены изучению продукции муцина опухолевыми клетками. Было обнаружено, что опухоли с различной дифференцировкой клеток (разным фенотипом) продуцируют разные муцины. Так, опухоли с гастроинтестинальным фенотипом, продуцируют MUC-2, а опухоли с панкреатобилиарным фенотипом — только MUC-1. Кроме того, был обнаружен третий тип опухоли, способный к одновременной продукции муцинов обоих типов — MUC-1 и MUC-2.
Эта разновидность в последствии была названа онкокистозным подтипом внутрипротоковой папиллярной муцинозной опухоли. Результаты этих исследований наводят на мысль, что термин внутрипротоковая папиллярная муцинозная опухоль — собирательное понятие, объединяющее, по крайней мере, три разновидности опухолей, достаточно близких по строению, но различных по иммунофенотипу секретируемого ими муцина. Наиболее часто выявляют гастроинтестинальный MUC-2- фенотип.
Гастроинтестинальный MUC-2+ фенотип составляет одну иммунофенотипическую группу с MUC-2+ коллоидной (муцинозной некистозной) карциномой, что предполагает возможность превращения внутрипротоковой папиллярной муцинозной опухоли в эту разновидность злокачественного новообразования. MUC-l+ панкреатобилиарный тип связан, возможно, с протоковой цистадеиокарциномой. Третий тип протоковой папиллярной опухоли — онкокистозный, возможно, может озлокачествляться, трансформируясь в карциному, однако гистологические и биологические особенности последней остаются неизученными.
Молекулярные механизмы, вктючающиеся при нарушении регуляции гена MUC при внутрипротоковой папиллярной опухоли, остаются пока неизвестными. Возможно, они определяются другими клетками, что косвенно подтверждается различным прогнозом при разных типах папиллярной опухоли — как мы отмечали выше, MUC-2+ тип отличается более благоприятным течением. Существует предположение о существовании неидентифицированной в настоящее время мутации, определяющей развитие интрадуктальной папиллярной муцинозной опухоли. Предположение это основано на факте частой ассоциации этих опухолей с другими внепанкреатическими злокачественными новообразованиями, а также с синдромом Пейтца—Егерса. Диагностика
Клиническая картина
Характерны симптомы острого или хронического панкреатита, реже опухоль выявляют случайно. Частота тяжёлых деструктивных панкреатитов при внутрипротоковой папиллярной опухоли не превышает 2%.
Большинство симптомов аналогичны таковым при ХП — боли в эпигастрии с усилением после приёма пищи, диспептические расстройства, астенические симптомы, признаки эндо- и экзокринной недостаточности, похудание.
Механическая желтуха возникает в 20% случаев, сс появление косвенно свидетельствует о злокачественном варианте опухоли. Крайне редко обнаруживают асцит.
Частота встречаемости сахарного диабета при внутрипротоковых папиллярных муцинозных опухолях достигает 11%, однако истинная причина эндокринной недостаточности до сих пор не установлена. Если речь идёт о протоковой аденокарциноме, быстро распространяющейся по паренхиме ПЖ с замещением опухолевой тканью островков Лангерганса, то, как правило, говорят о панкреатогенном сахарном диабете, вторичном по отношению к раку ПЖ. При внутрипротоковых папиллярных опухолях инвазия в паренхиму ПЖ происходит не так часто, и менее выражена, чем при раке, поэтому механизм диабета при этих новообразованиях не совсем понятен. Возможно, сахарный диабет развивается на фоне рецидивирующего обструктивного панкреатита, приводящего к воспалительным, деструктивным, кистозным, фиброзным и атрофическим изменениям как экзо-, так и эндокринной части ПЖ.
Дефицит массы тела обнаруживают у 42% больных. Как и при панкреатите, он обусловлен рядом причин. Во-первых, гиперпродукция муцина на ранних этапах развития опухоли может приводить с временной обструкции выводных протоков ПЖ, что обусловливает болевой абдоминальный синдром после приёма пищи. Дальнейший рост опухоли приводит к уменьшению просвета поражённого протока (или протоков) с нарастанием клинических проявлений. Боль вынуждает больных отказываться от приёма пищи, чтобы предотвратить, таким образом, её повторное возникновение (ситофобия). Во-вторых, растущая, метаболически активная опухоль потребляет для собственных нужд всё необходимое. Нарушение обмена веществ обусловлено и сахарным диабетом, осложняющим течение опухоли.
В-третьих, нарушенный отток панкреатического сока в просвет ДПК приводит к развитию экзокринной недостаточности ПЖ, способствуя нарушению пищеварения и всасывания питательных веществ.
Методы визуализации. Для скрининга, как и при других опухолях ПЖ, используют УЗИ и КТ. Эффективность диагностики существенно повышается при информированности врачей о существовании этой необычной опухоли. На эффективность диагностики влияет также расположение опухоли (в основном протоке ПЖ или в более мелких протоках).
Во всех случаях, когда при скрининговом УЗИ выявляют дилатацию протока ПЖ при отсутствии объективной причины блока (опухоли головки ПЖ больших размеров, камней в общем жёлчном протоке, опухоли БДС и т.п.) и анамнестических данных заранее имевшую место патологию, способствующую развитию Рубцовых изменений БДС и терминального отдела протока ПЖ, в первую очередь надо думать о наличии у больного внутрипротоковой папиллярной опухоли. При диффузной форме опухоли может быть расширено несколько протоков, при сегментарной — как правило, один.
Другой важнейший признак внутрипротоковых папиллярных опухолей — распространённая атрофия паренхимы ПЖ, обычно пропорциональная степени протоковой дилатации. Далеко не всегда при УЗИ можно выявить чёткие зоны внутрипротоковых блоков, а уж тем более определить, чем они вызваны — муциновыми «пробками» или папиллярными разрастаниями. Третий признак опухоли патогномоничен — наличие гипоэхогенных микро- или макрокистозных изменений паренхимы ПЖ по типу «пчелиных сот»; связь этих кист с дилатированными протоками при УЗИ выявляют не всегда.
В ряде случаев у больных обнаруживают кальцификацию и панкреатолитиаз, обусловленные как рецидивирующим панкреатитом, так и отложением солей кальция в муциновых «пробках».
При КТ с контрастированием зона опухоли значительно лучше накапливает контрастное вещество, чем окружающая паренхима. В просвете расширенного протока ПЖ можно выявить гиперэхогенные включения, соответствующие муциновым «пробкам» или папиллярным разрастаниям.
При длительном течении новообразования, расположенного в головке ПЖ, опухолевая инфильтрация вместе с кистозными изменениями протоков может достигать больших размеров, занимая всю головку железы. В результате сдавливается интрапанкреатический отдел общего жёлчного протока с развитием билиарной гипертензии. В ряде случаев у больных возникает асцит, обусловленный пропотеванием жидкостного компонента кист, поскольку стенка кист может быть достаточно тонкой, а давление внутри кист значительно большим, чем в полости брюшины.
Выраженная протоковая дилатация при отсутствии атрофических изменений паренхимы, особенно при наличии чётко определяемых внутрилротоковых папиллярных разрастаний, — признак озлокачествления опухоли. Даже при начальных этапах озлокачесгвления всегда присутствует кистозный компонент, что важно учитывать при дифференциальной диагностике с протоковой аденокарциномой. Наличие кистозного расширения коллатеральных протоков в сочетании с внутрипротоковыми разрастаниями существенно упрощает диагностику диффузных форм. При сегментных формах результаты КТ не столь специфичны.
Несмотря на ряд условно специфичных признаков при УЗИ, КТ и МРТ, необходимо выявить сами внутрипротоковые папиллярные разрастания. Ранее с этой целью применяли только ЭРХПГ, однако совершенствование программ КТ и МРТ, появление ЭУС и МРХПГ позволяет в настоящее время с достаточной точностью выявлять внутрипротоковые разрастания. Достаточно чувствительный метод диагностики внутрипротоковых папиллярных опухолей — проведение МРХПГ с внутривенным ведением карбахола (секретина). Самый современный метод диагностики, позволяющий осуществить визуальный осмотр протока ПЖ и произвести биопсию опухоли. — вирсунгоскопия, дополняющая ЭУС.
Дифференциальная диагностика с первичными панкреатитами основана на возрастном критерии (в среднем 42 года при рецидивируюшем хроническом панкреатите), половом критерии (хроническим панкреатитом, не связанным с очевидной патологией билиарного тракта, страдают преимущественно мужчины), а также на факте отсутствия у многих больных внутрипротоковой папиллярной опухолью отягощенного анамнеза по злоупотреблению алкоголем и табакокурению.
Дифференциальная диагностика с серозной цистаденомой достаточно трудна и основана на возрастных (при пистаденомах средний возраст больных на Шлет меньше), половых (цистаденома встречается у женщин в 7 раз чаще) отличиях и более благоприятном течении (чаше скрытом) цистаденомы. Расположение опухоли, демографические признаки, образ жизни не позволяют разграничить эти кистомы. Внутрипротоковая папиллярная опухоль чаще протекает с клиническими проявлениями и с развитием осложнений, чем при цистаденомах.
Дифференциальная диагностика с муцинозной цистаденомой также трудна, однако она имеет меньшее значение, поскольку в обоих случаях показано радикальное хирургическое лечение. Отмечают некоторые возрастно-половые, клинические и топографические отличия, поскольку мупинозная цистаденома встречается, в подавляющем большинстве случаев, у женщин среднего возраста, в 93% случаев она располагается в теле и хвосте ПЖ, практически всегда протекает бессимптомно.
Лечение
Всем больным внутрипротоковой папиллярной муцинозной опухолью показано хирургическое лечение в виде панкреатодуоденальной резекции либо панкреатэктомии, несмотря на высокий средний возраст больных (65—70 лет), имеющих много сопутствующих заболеваний. До операции должен быть установлен морфологический диагноз.
Ориентация на хирургическое лечение у всех больных в обязательном порядке вполне оправдана, поскольку даже при доброкачественной папиллярной опухоли на момент первичного установления диагноза риск озлокачествления высок; значительна вероятность развития рецидивирующего обструктивного панкреатита, грозного своими осложнениями. В специализированных центрах, занимающихся хирургией ПЖ, летальность после панкреатодуоденальной резекции при внутрипротоковых папиллярных муцинозных опухолях не превышает 5%, при дистальной резекции смертельных случаев, как правило, и вовсе нет.
Маев И.В., Кучерявый Ю.А.
Опубликовал Константин Моканов
Источник