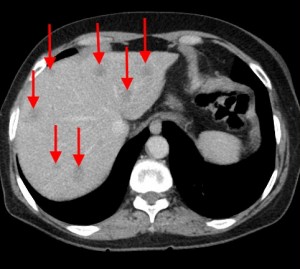
Патологическая физиология поджелудочной железы
Этот
орган расположен под желудком. У
поджелудочной железы есть эндокринная
функция, но она также является экзокринной
железой (железой внешней секреции, с
выводным протоком). Как эндокринная
железа она производит инсулин и
соматостатин, глюкагон — три гормона,
которые контролируют количество сахара
в крови. Эти гормоны производятся
участками железы, называемым островками
Лангерганса. Поджелудочная железа также
выделяет пищеварительные соки в
двенадцатиперстную кишку (тонкую кишку).
Эти соки, которые смешиваются с желчью,
являются смесью ферментов, которые
переваривают пищу. 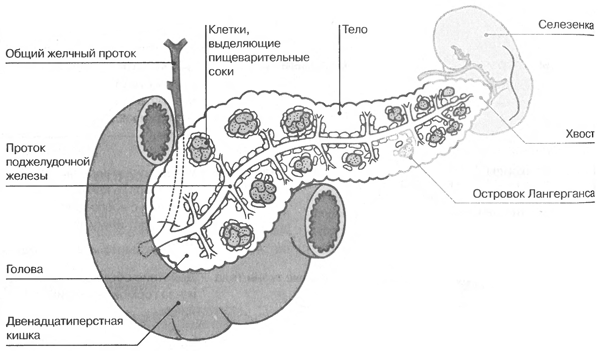
43. Половые железы, внутрисекреторная функция. Физиологическая роль эндокринной части половых желез в организме.
Половые гормоны вырабатываются
половыми железами, которые относятся
к числу смешанных, так как часть их
клеток выполняет внешнесекреторную
функцию, другая часть- внутрисекреторную.
Половые гормоны в течение всей жизни
оказывают мощное влияние на формирование
тела, обмен веществ и половое поведение.
Мужские половые
гормоны(андрогены) вырабатываются
особыми клетками семенников. Они выделены
из экстрактов семенников, а также из
мочи мужчин.
Истинным мужским половым
гормоном является тестостерон и его
производное- андростерон. Они обусловливают
развитие полового аппарата и рост
половых органов, развитие вторичных
половых признаков: огрубление голоса,
изменение телосложения — шире становится
плечи, увеличиваются мышцы, усиливается
рост волос на теле и лице. Совместно с
гормонами гипофиза тестостерон активирует
сперматогенез (созревание сперматозоидов).
Женские половые гормоны-эстрогены
вырабатываются в яичниках. Они оказывают
влияние на развитие половых органов,
выработку яйцеклеток, обусловливают
подготовку яйцеклеток к оплодотворению,
матки- к беременности, молочных желез-
к кормлению ребенка.
Истинным женским половым
гормоном считают эстрадиол. К женским
половым гормонам относится и
прогестерон-гормон беременности(гормон
желтого тела).
Патология половых желез.
При гиперфункции семенников в раннем
возрасте отмечается преждевременное
половое созревание, быстрый рост тела
и развитие вторичных половых признаков.
Поражение семенников или их
удаление(кастрация) в раннем возрасте
вызывает прекращение роста и развития
половых органов; вторичные половые
признаки не развиваются, увеличивается
период роста костей в длину, отсутствует
половое влечение, не растут волосы на
лице, голос сохраняется высоким в течении
жизни.
Гиперфункция яичников
вызывает ранее половое созревание с
выраженными вторичными признаками и
менструацией. Описаны случаи раннего
полового созревания девочек в 4-5 лет.
44. Внутренняя среда организма, компоненты и её значение для жизнедеятельности человека. Кровь. Состав крови. Возрастные особенности строения и функционирования сердечно-сосудистой системы человека.
Внутренней
средой организма
называют совокупность биологических
жидкостей (кровь, лимфа, тканевая
жидкость), омывающих клетки и структуры
тканей и принимающих участие в процессах
обмена веществ. Предложил понятие
«внутренняя среда» в 19 веке Клод
Бернар, подчеркивая тем самым, что в
отличие от изменчивой внешней среды, в
которой существует живой организм,
постоянство жизненных процессов клеток
требует соответствующего постоянства
их окружения, т.е. внутренней среды.
Кровь—
это жидкая ткань, состоящая из плазмы
и взвешенных в ней кровяных клеток.
Кровь заключена в систему сосудов и
находится в состоянии непрерывного
движения.
Возрастные
особенности сердечно — сосудистой
системы.
В
процессе развития ребенка в его
сердечно-сосудистой системе происходят
существенные морфологические и
функциональные изменения. Формирование
сердца у эмбриона начинается со второй
недели эмбриогенеза и четырехкамерное
сердце образуется уже к концу третьей
недели. Кровообращение плода имеет свои
особенности, связанные прежде всего с
тем, что до рождения кислород поступает
в организм через плаценту и так называемую
пупочную вену.
Пупочная
вена разветвляется на два сосуда, один
питает печень, другой соединяется с
нижней полой веной. В результате в нижней
полой вене происходит смешивание крови,
богатой кислородом (из пупочной вены)
и крови, оттекающей от органов и тканей
плода. Таким образом, в правое предсердие
попадает смешанная кровь. Как и после
рождения, систола предсердий сердца
плода направляет кровь в желудочки,
оттуда из левого желудочка она поступает
в аорту, из правого — в легочную артерию.
Однако предсердия плода не обособлены,
а соединяются с помощью овального
отверстия, поэтому левый желудочек
направляет в аорту кровь частично и из
правого предсердия. По легочной артерии
в легкие попадает весьма незначительное
количество крови, так как легкие у плода
не функционируют. Большая же часть
крови, выбрасываемой из правого желудочка
в легочной ствол, по временно
функционирующему сосуду — боталлову
протоку — попадает в аорту.
Важнейшую
роль в кровоснабжении плода выполняют
пупочные артерии, отходящие от подвздошных
артерий. Через пупочное отверстие они
выходят из организма плода и разветвляясь,
образуют в плаценте густую сеть
капилляров, от которой берет начало
пупочная вена. Кровеносная система
плода замкнута. Кровь матери никогда
не попадает в кровеносные сосуды плода
и наоборот. Поступление кислорода в
кровь плода осуществляется путем
диффузии, так как его парциальное
давление в материнских сосудах плаценты
всегда выше, чем в крови плода.
После
рождения пупочные артерии и вена
запустевают и превращаются в связки. С
первым вдохом новорожденного начинает
функционировать малый круг кровообращения.
Поэтому обычно боталлов проток и овальное
отверстие быстро зарастают. У детей
относительная масса сердца и общий
просвет сосудов больше, чем у взрослых,
что в значительной степени облегчает
процессы кровообращения. Рост сердца
находится в тесной связи с общим ростом
тела. Наиболее интенсивно сердце растет
в первые годы жизни и в конце подросткового
периода. С возрастом меняются также
положение и форма сердца. У новорожденного
сердце шаровидной формы и расположено
значительно выше, чем у взрослого.
Различия по этим показателям ликвидируются
только к десяти годам. К 12-летнему
возрасту исчезают и основные функциональные
различия в сердечно-сосудистой системе.
Соседние файлы в предмете Анатомия и физиология
- #
- #
Источник
Патологическая физиология
Экспериментально показано, что острый панкреатит может быть вызван различными путями, большинство из которых имеет определенное патогенетическое значение в развитии этого заболевания у человека. Механическая или химическая травма поджелудочной железы возникает при введении повреждающего агента [желчь, соли кальция, гипертонические растворы, трипсин, энтеропептидаза (энтерокиназа)] в ткань поджелудочной железы или в ее протоки. Функциональные и структурные изменения в поджелудочной железе типа хронического панкреатита в эксперименте можно вызвать нарушением кровообращения путем введения в сосуды поджелудочной железы склерозирующих агентов, искусственных эмболов (воздух, ликоподий, жиры, нагретый парафин, пластмасса) и перевязкой магистральных сосудов; инфекционные панкреатиты — инъекцией бактериальных культур в проток поджелудочной железы, лигированный ниже места инъекции. Патологические изменения в поджелудочной железе можно вызвать также введением тем или иным путем (через рот, подкожно, внутримышечно, внутривенно или внутрибрюшинно) средств, приводящих к нарушению определенных звеньев обмена веществ поджелудочной железы. Наиболее часто используют этионин — аналог метионина, ингибирующий включение в состав белков метионина и глицина. Небольшие дозы этионина вызывают преходящие изменения гипосекреторного типа. При увеличении дозы в поджелудочной железе происходят такие же деструктивные процессы вплоть до панкреонекроза, как и при введении четырех-хлористого углерода, 2-хлораденозина, пропилтиоурацила. Перерезка блуждающих или чревных нервов на фоне усиленной работы поджелудочной железы сопровождается значительными функциональными нарушениями и структурными изменениями ее. Подобный же эффект наблюдается и при хроническом раздражении этих нервов и солнечного сплетения (ликоподий, скипидар, кротоновое масло, взвесь угольного порошка).
Отклонения в функции поджелудочной железы возникают и при нарушениях высшей нервной деятельности. Так, у собак при экспериментально вызванных срывах высшей нервной деятельности наблюдаются обратимые функциональные расстройства поджелудочной железы, проявляющиеся в виде гипо- или гиперсекреции. При
одновременном повреждении поджелудочной железы и аппаратов, регулирующих ее деятельность, отмечаются наиболее значительные нарушения функции поджелудочной железы в эксперименте.
По современным представлениям независимо от внешнеорганного этиологического фактора важнейшую роль в развитии панкреатита играет внутриорганная активация протеолитических ферментов (в первую очередь трипсина), вырабатываемых поджелудочной железой. Активация трипсина может зависеть не только от проникновения в железу активаторов типа энтерокиназы, но и от уменьшения концентрации ингибитора трипсина (который в норме предотвращает самоактивацию) и сдвига в кислую сторону.
Под влиянием внутриклеточно активированных трипсина и химотрипсина, как полагают, происходит гидролиз протеиновых структур, что приводит к нарушению функций клеточных элементов или их гибели, а также нарушению проницаемости сосудов. Не исключено, что такое же значение имеет уменьшение резистентности протеиновых структур больного органа к действию протеолитических энзимов. Благодаря этому создаются условия для последующего диффундирования ферментов за пределы секреторных клеток в межацинозную ткань и дальнейшего разрушения белковых и липидных структур за счет освобождающихся соответственно внутриклеточных протеиназ, липазы, лецитиназы и других ферментов. Следствием этих процессов является развитие аутолиза с геморрагиями и жировыми некрозами. Панкреатит сопровождаются нарушением секретообразовательной и выделительной функций поджелудочной железы. Вследствие затруднения оттока поджелудочного сока и повышения проницаемости экзокринных клеток и сосудов наблюдается усиленный переход панкреатических ферментов в кровь. От тяжести заболевания зависит изменение секреции и инкреции ферментов. Действительно, при разнообразных формах острого панкреатита отмечается резкое повышение уровня панкреатических ферментов в крови и моче (трипсин, липаза, различные пептидазы, амилаза). Выяснено, что амилаза легче других ферментов диффундирует через полупроницаемые оболочки, поэтому в начальных стадиях острого панкреатита при остром отеке поджелудочной железы отмечается увеличение концентрации амилазы в крови, а по достижении определенного порога она появляется и в моче. Гиперамилаземия и гиперамилазурия держатся различное время и зависят от степени поражения железы. Гиперлипаземия обусловливается более глубокими поражениями органа. По мнению многих авторов, изменения содержания липазы в крови являются более чувствительными и специфическими показателями поражений поджелудочной железы, чем содержание амилазы в крови.
В последнее время особое внимание уделяется определению содержания липазы в моче. Установлено, что липаза в моче бывает исключительно панкреатического происхождения и что острые панкреатиты сопровождаются гиперлипазурией. Экспериментально показано, что содержание дезоксирибонуклеазы в сыворотке крови специфически увеличивается при панкреонекрозах, а не при обструкции проточной системы поджелудочной железы. Повышение содержания амилазы, липазы и протеаз в крови и моче отражает не столько состояние секреторного аппарата поджелудочной железы, сколько изменение условий оттока поджелудочного сока. При введении стимуляторов с секретинным механизмом действия (секретин, 0,5% раствор соляной кислоты и др.) в ряде случаев может обнаружиться уменьшение объема секреции поджелудочной железы, низкие величины карбонатной щелочности и отсутствие или извращение реакции на введение раздражителей. При введении веществ, стимулирующих ферментообразование (панкреозимин, мехолил, простигмин и др.), отмечается уменьшение содержания одного или нескольких ферментов в поджелудочном соке. Большую ценность для диагностики ранних форм хронического панкреатита имеет исследование активности ферментов в сыворотке крови после стимуляции секретином или панкреозимином. Считается, что уровень панкреатических ферментов (амилаза, липаза, протеазы) меняется в значительной степени параллельно.
Большой интерес представляют сообщения об изменении соотношений основных ферментов при панкреатите. У здоровых людей при введении секретина наблюдается повышение активности трипсина, амилазы и липазы в дуоденальном содержимом. При острых и хронических панкреатитах бывает нарушение нормальных соотношений между основными группами ферментов. Это явление называется патологической диссоциацией, которая свидетельствует об относительной независимости синтеза ферментов и их секреции. Описано несколько вариантов патологической диссоциации ферментативных свойств панкреатического сока: относительное уменьшение активности амилазы при нормальном содержании трипсина и липазы, липазы при нормальном содержании остальных двух ферментов, трипсина и амилазы при нормальном содержании липазы.
При тяжелых панкреатитах синтез ферментов угнетается, что имеет диагностическое значение. При более легких формах отмечается изменение свойств синтезируемых ферментов (в частности, их электрофоретическая подвижность и специфическая активность). Хотя при панкреатите доминирует поражение ацинарного аппарата, в части случаев наблюдается нарушение функции α- и β-клеток, следствием чего являются кратковременная гипергликемия, глюкозурия и снижение β-липопротеинов сыворотки крови.
Источник
После эвакуации из желудка в тонкую кишку пища подвергается наиболее интенсивному перевариванию.
Чрезвычайно важную роль в этом процессе играет поджелудочная железа, точнее — ее секреты.
Главные компоненты панкреатического сока — это бикарбонат, создающий щелочную среду и нейтрализующий кислый желудочный химус в двенадцатиперстной кишке до рН 6-8 (такой диапазон рН необходим для панкреатических ферментов), и пищеварительные ферменты, расщепляющие основные компоненты пищи.
Поджелудочная железа является экзокринным (секретирующим) и одновременно эндокринным (инкретирующим) органом, участвующим в пищеварении, в регуляции обмена, а также других органов и систем.
Поджелудочная железа, масса которой составляет примерно 110 г, выделяет в сутки от 1,5 до 2,5 л сока. Сок изотоничен плазме крови (независимо от стимуляции), содержит ряд электролитов и солей, а также пищеварительные ферменты. Основные анионы сока — С1- и НСО3-, катионы — Na+ и К+ Кроме того, в соке присутствуют катионы Са2+, Mg2+ и анионы НРО4-. При стимуляции концентрация катионов остается без изменений, а анионов меняется в противоположных направлениях. При максимальной секреции концентрация НСО3-составляет 130-140 ммоль/л, а рН — 8,2.
Экзокринная функция поджелудочной железы имеет исключительно важное значение для пищеварения. Под влиянием психических, алиментарных, гуморальных и других раздражителей клетки ацинусов поджелудочной железы синтезируют и выделяют в двенадцатиперстную кишку более 20 проферментов и ферментов (главным образом гидролаз), которые участвуют в расщеплении в кишечнике различных составных частей пищи.
Пищеварительные ферменты составляют около 90% белков панкреатического сока. Эту функцию поджелудочной железы называют экболической в отличие от второй экзокринной функции — гидрокинетической, заключающейся в секреции воды, бикарбонатов (до 150 ммоль/л) и других электролитов. Гидрокинетическая функция поджелудочной железы обеспечивает нейтрализацию кислого желудочного содержимого и создает в кишечнике щелочную среду, оптимальную для действия панкреатических и кишечных ферментов.
Панкреатические ферменты подразделяются на амилолитические (гидролиз крахмала), протеолитические (гидролиз белков), липолитические (гидролиз жиров) и нуклеолитические (гидролиз нуклеиновых кислот).
Амилолитические ферменты — амилазы
Расщепление крахмала начинает а-амилаза, состоящая из нескольких изоферментов, и составляющая примерно 20% белков в панкреатическом секрете. Основное количество этого фермента выделяется поджелудочной железой в активном виде.
Сходный изофермент синтезируется слюнными железами. а-Амилаза расщепляет полисахариды (крахмал, гликоген) до декстринов, мальтоолигосахаридов, мальтозы и незначительного количества глюкозы. Указанные полимеры далее превращаются в глюкозу кишечными ферментами — мальтазой, у-амилазой, изомальтазой.
Липолитические ферменты — липазы
Липолиз осуществляется панкреатическими ферментами, однако диагностическое значение в настоящее время имеет лишь липаза (гидролизует триглицериды). Из панкреатического сока выделена еще фосфолипаза (гидролиз фосфолипидов, лецитина) и карбоксилэстераза (гидролиз эфиров жирных кислот).
Поджелудочная железа выделяет основное количество липазы (немного липазы содержится также в слюне и кишечном соке), расщепляющей триглицериды до моноглицеридов и жирных кислот, которые проходят через мембрану энтероцита.
Липаза гидролизует водонерастворимый субстрат, что возможно лишь на поверхности мелких эмульгированных частиц жира. Одинаковые количества фермента проявляют различную активность в зависимости от качества эмульсии: чем она тоньше, тем выше активность фермента. Липаза активна в тонкой кишке в присутствии желчных кислот, которые способствуют эмульгированию жиров.
Протеолитические ферменты — протеазы
В панкреатическом соке их много (эндопептидазы — трипсин, химотрипсин, эластаза, экзопептидазы — карбоксипептидазы А и Б). Они относятся к группе сериновых протеаз и составляют 44% от общего белка панкреатического сока. Существуют множественные формы трипсина и химотрипсина, как и желудочных пепсинов. Ацинарные клетки не синтезируют активные протеолитические ферменты (это грозило бы самоперевариванием органа).
Они выделяются в виде неактивных проферментов, которые активируются в кишке. Первым активируется трипсиноген. Под действием кишечного фермента энтерокиназы он превращается в трипсин, а затем активные молекулы трипсина обеспечивают активацию других протеолитических ферментов, включая трипсиноген (процесс активации продолжается уже аутокаталитически).
С панкреатическим соком выделяются фактически два трипсиногена, составляющие около 19% всех его белков, два химотрипсиногена и две проэластазы. Все они называются эндопептидазами, так как при гидролизе белков «разрывают» внутренние связи между аминокислотами в середине их цепей, продуцируя пептиды. Эндопептидазы специфичны.
Например, трипсин гидролизует лишь связи справа от лизина или аргинина, химотрипсин — в основном те, которые рядом с фенилаланином, тирозином и триптофаном. Эластаза способна гидролизовать эластин, белок соединительной ткани, а также другие белки. В отличие от эндопептидаз экзопептидазы разрывают в пептидных цепях С-терминальную, т. е. конечную, связь (карбоксипептидазы) или первую, N-терминальную (аминопептидазы), «освобождая», таким образом, аминокислоты одну за другой.
В панкреатическом соке присутствует ингибитор трипсина — неферментный белок, тесно связанный с протеолизом. Его физиологическое значение заключается в предотвращении преждевременной активации трипсина в протоках поджелудочной железы. Определение его активности в сыворотке крови в динамике имеет значение, свидетельствующее о воспалительно-деструктивных процессах органа при гиперферментемии (синдром «уклонения ферментов»).
Калликреин является протеолитическим ферментом поджелудочной железы. Активированный трипсином, он отвечает за образование в крови каллидина, гипотензивного полипептида, идентичного брадикинину, одному из нейровазоактивных пептидов.
Нуклеолитические ферменты — нуклеазы
Принадлежат к фосфодиэстеразам. В панкреатическом соке они представлены рибонуклеазой, гидролизующей рибонуклеиновую кислоту, и дезоксирибонуклеазой, расщепляющей дезоксирибонуклеиновую кислоту.
Количество и ферментативная активность панкреатического сока зависят от количества и состава принятой пищи. Вне пищеварения, натощак, поджелудочный сок выделяется в небольших количествах.
Секрецию панкреатического сока вызывает объемная и стимулирующая желудочное кислотообразование пища. Твердая, густая и жирная пища долго задерживается в желудке (медленнее эвакуируется), поэтому секреция поджелудочной железы дольше, чем после приема жидкой пищи.
Основная секреция, однако, начинается в кишечной фазе, т. е. после попадания пищи и продуктов ее переваривания в двенадцатиперстную кишку.
Секреция поджелудочного сока усиливается через 2-3 мин после приема пищи и продолжается 6-14 ч (с максимальным выделением сока на 90-й минуте) в зависимости от ее состава. Смешанная пища вызывает больший секреторный ответ, чем отдельные продукты.
Нейтральные жиры и продукты их переваривания больше всего стимулируют продуцирующие ферменты клетки поджелудочной железы. Белки также довольно сильный стимулятор секреции ферментов, в меньшей мере — бикарбонатов и жидкой части панкреатического сока.
Поступление аминокислот в кишку вызывает значительное повышение в крови уровня гормона — холецистокинина (прежние названия — панкреозимин, холецистокинин-панкреозимин), местного стимулятора ферментсинтезирующей деятельности ацинарных клеток поджелудочной железы. Особенно сильно влияют фенилаланин, холин, метионин и другие незаменимые аминокислоты.
Преобладание углеводов в питании «щадит» поджелудочную железу, что необходимо учитывать при обострении хронического панкреатита. Малоконцентрированные растворы глюкозы и сахарозы, введенные в двенадцатиперстную кишку, вызывают кратковременную и небольшую стимуляцию секреции а-амилазы, а концентрированные растворы — резкое угнетение экзокринной секреции.
Соляная кислота является сильным естественным стимулятором внешней секреции поджелудочной железы. Все напитки и продукты, которые возбуждают аппетит, наряду с секрецией желудка усиливают секрецию поджелудочной железы. Так, выраженным сокогонным действием обладают некоторые фруктовые и органические кислоты (яблочная, лимонная, винная, молочная), а также алкоголь.
Зависимость ферментного состава сока поджелудочной железы от качества пищи хорошо известна. Находящиеся в ацинарных клетках гранулы содержат все ферменты, присутствующие в секрете, в постоянном соотношении, так что в панкреатическом соке оно также постоянно.
Однако увеличение в пище доли какого-либо компонента рациона (например, белков) постепенно увеличивает синтез соответствующих гидролизующих ферментов. Эта адаптация к диете дала возможность обсуждать вопрос о возможности диетического излечения некоторых дисфункций поджелудочной железы.
Секреция поджелудочной железы регулируется нервными и гуморальными механизмами.
В стимуляции панкреатической секреции прямые нервные влияния имеют меньшее значение, чем гуморальные. Ведущее значение в гуморальной регуляции секреции поджелудочной железы принадлежит гастроинтестинальным гормонам. Они относятся к числу пептидов и синтезируются специальными клетками желудка и двенадцатиперстной кишки под влиянием соответствующих химических, механических, нервных или иных стимулирующих факторов.
Секрецию поджелудочной железы усиливают секретин, холецистокинин, а также гастрин, серотонин, инсулин, бомбезин, субстанция П и соли желчных кислот. Тормозят выделение поджелудочного сока глюкагон, кальцитонин, парентеральное питание (ПП), соматостатин. Это может возбуждать и тормозить панкреатическую секрецию. Эффекты гормонов частично опосредуются через их влияние на желудочную секрецию: с усилением ее более кислое содержимое поступает в двенадцатиперстную кишку и посредством ее гормонов повышает панкреатическую секрецию.
Патофизиология
При структурно-функциональных нарушениях поджелудочной железы может нарушаться синтез ферментов, в связи с чем возникают дефекты пищеварения в тонкой кишке. Особенно страдает переваривание жира, так как панкреатический сок содержит наиболее активный фермент липазу.
При патологии может не усваиваться до 60-80% жира, который выводится с калом. В меньшей степени нарушается переваривание белков, может не усваиваться до 30-40% их количества. О недостаточном переваривании белков свидетельствует появление большого количества мышечных волокон в каловых массах (креаторея) после приема мясной пищи. Переваривание углеводов также нарушено. Развивается недостаточность пищеварения.
Нарушения внешней секреции поджелудочной железы могут быть обусловлены рядом причин.
Основные из них следующие:
1) развитие в поджелудочной железе воспалительных процессов (острые и хронические панкреатиты);
2) обтурация протока поджелудочной железы конкрементами (желчнокаменная болезнь, калькулез протоков), паразитами кишечника, белково-слизистыми «пробками»;
3) воспалительные процессы в двенадцатиперстной кишке (дуодениты, язвенная болезнь), сопровождающиеся уменьшением образования секретина; вследствие этого понижается секреция панкреатического сока;
4) сдавление протока поджелудочной железы (опухоли, дуодениты, фатериты);
5) развитие тяжелых нарушений обменных процессов организма (ожирение, белково-энергетическая недостаточность, гормональные расстройства и др.) с формированием дистрофических поражений поджелудочной железы (липоматоз, белковая дистрофия, гемохроматоз);
6) аллергическая перестройка организма;
7) неврогенное торможение функций поджелудочной железы (вагальная дистрофия, длительная атропинизация);
8) разрушение опухолью.
В случаях развития обтурационных процессов, затрудняющих или даже прекращающих отток панкреатического секрета в двенадцатиперстную кишку, возникает гипертензия в системе протоков поджелудочной железы, вызывающая не только выраженный болевой синдром, но и внутренние разрывы, разрушения паренхимы органа.
Энтерокиназа лизированных клеток поджелудочной железы в этом случае может катализировать активацию ферментов панкреатического сока непосредственно в протоковой системе (особенно трипсиногена).
Более того, сам трипсин способен активизировать трипсиноген, как бы запуская «цепную» реакцию ферментативной активизации (аутокаталитическая реакция). В результате описываемых явлений ферменты поджелудочной железы могут осуществлять самопереваривание ткани поджелудочной железы с развитием некрозов.
При разрушении поджелудочной железы активные панкреатические ферменты, продукты тканевой деструкции, нарушенного метаболизма могут всасываться в кровь, в окружающие ткани. В тканях в результате действия на них ферментов развиваются некрозы; особенно характерно появление некрозов жировой клетчатки (сальника), возникающих под влиянием липазы панкреатического сока. Формируется синдром интоксикации организма.
А.Ю. Барановский
Источник