Роль поджелудочной железы в регуляции уровня глюкоз в крови
Поджелудочная
железа выполняет две функции: экзокринную
(синтез и секреция пищеварительных
ферментов) и эндокринную (синтез и секре
ция гормонов). Эндокринную функцию
выполняют особые участки поджелудочной
железы — островки Л ангерганса, занимающие
около 1% ее объема. Эндокринные клетки
островков Лангерганса секретируют в
кровь:
—
инсулин ( б ет а -клет ки );
—
глюкагон ( а ль ф а -к лет ки );
—
сомат ост ат ин (делы п а -к лет ки ).
По
химической структуре эти гормоны
относятся к белково-пептидным, а их
основная физиологическая роль — регуляция
углеводного обмена.
5.1. Гормоны поджелудочной железы
I.
Инсулин — основной по количеству и
значению гормон остров ков Лангерганса.
Эффекты
дейст вия инсулина:
1)
гипогликем ическое дейст вие: инсулин
— единственный гормон, снижающий
концентрацию глюкозы в крови . В
частности, инсулин:
• повышает
проницаемость клеточных мембран для
глюкозы; инсулин регулирует поступление
глюкозы во все ткани, исключая ЦНС, нейро
ны которой являются инсулиннезависимыми
— могут потреблять глюкозу в отсутствие
инсулина;
• усиливает
утилизацию глюкозы в клетках — ее
превращение в гликоген и жиры;
2)
анаболическое действие : инсулин
стимулирует синтез и тормозит
распад
гликогена, жиров и белков, РНК, ДНК
(анаболический эффект).
2.
Глюкагон — антагонист инсулина —
повышает концентрацию глюкозы в крови,
усиливая глюконеогенез и расщепление
гликогена в печени. Г люкагон также
стимулирует распад белков и жиров.
Регуляция
секреции инсулина и глюкагона
В
основном, осуществляется глюкозой по
принципу отрицательной обратной связи.
Увеличение концентрации глюкозы в крови
приводит к увеличению секреции инсулина
и снижению секреции глюкагона; наоборот,
снижение концентрации глюкозы тормозит
секрецию инсулина и усиливает
секрецию глюкагона. Таким образом
концентрация глюкозы поддерживается
на постоянном уровне (рис. 11).
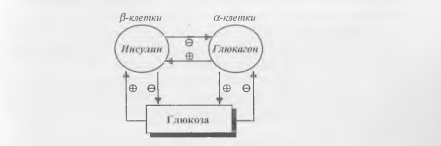
Рис.
11. Регуляция секреции инсулина и
глюкагона.
Дополнительную
петлю отрицательной обратной связи в
этой cистеме образуют инсулин и глюкагон:
глюкагон стимулирует секрецию инсулина,
а инсулин тормозит секрецию глюкагона.
Кроме того, секрецию обоих гормонов
подавляет соматостатин дельта-клеток
островков Лангерганса.
Следует
добавить, что секрецию инсулина усиливают
некоторые гормоны желудочно-кишечного
тракта (гастрин, секретин и др.); 2)
парасимпатические волокна блуждающего
нерва (через Механорецепторы). Наоборот,
секрецию инсулина угнетают 2) симпатические
волокна (через арадренорецепторы).
5.2. Регуляция концентрации глюкозы в крови
Нормальная
концентрация глюкозы в плазме крови
(натощак) составляет 3,5-5,5 ммоль/л. В
регуляции концентрации глюкозы в крови
участвуют несколько гормонов.
Снижает
концент рацию глюкозы единственный
гормон — инсулин. В норме секреция
инсулина повышается после приема пищи,
когда концентрация глюкозы в крови
может возрастать до 8-9 ммоль/л. Инсулин
способствует утилизации глюкозы тканями,
что необходимо для их энергообеспечения
и для создания энергетических запасов
(гликогена и жира).
Повышают
концентрацию глюкозы несколько гормонов
(их называют «контринсулярными»):
глюкагон, глю кокортикоиды, адреналин,
т ироидны е горм оны , соматотропный
гормон. Секреция этих гормонов усиливается
при гипогликемии или при стрессе. В
результате, концентрация глюкозы в
крови повышается за счет гликогенолиза
(распада гликогена) и глюконеогенеза —
синтеза глюкозы из неуглеводных
соединений: жирных кислот (их концентрация
увеличивается вследствие липолиза) и,
в крайнем случае, аминокислот (образуются
при распаде белков). Выходящая в кровь
глюкоза потребляется, в первую очередь,
нейронами ЦНС, которые с одной стороны,
практически не имеют собственных запасов
гликогена и поэтому очень чувствительны
к гипогликемии, а с другой стороны,
способны потреблять глюкозу в отсутствии
инсулина, секреция которого при стрессе
снижена.
Патология.
Нарушение регуляции уровня глюкозы в
крови может приводить к развитию
сахарного диабета, основным признаком
которого является стойкая гипергликемия
(концентрация глюкозы в крови натощак
превышает 7 ммоль/л). Повышается также
концентрация глюкозы в первичной моче,
вследствие чего замедляется реабсорбция
воды в почках, и увеличивается диурез
— количество вторичной мочи может
превышать 5 л/сут.
Механизмы
развития сахарного диабета разнообразны
и могут быть объединены в две группы:
1
) абсолютная недостаточность инсулина
— снижение секреции инсулина вследствие
генетических дефектов, иммунных поражений
(3-клеток островков Лангерганса,
заболеваний и повреждений поджелудочной
железы, недостаточности питания (прежде
всего белкового) и других причин;
2)
относительная недостаточность
инсулина — секреция инсулина в этом
случае не снижается, или даже повышается;
гипергликемия при этом связана со
снижением чувствительности тканей к
инсулину вследствие изменения рецепторов
инсулина, ожирения, гиперсекреции
контринсулярных г ормонов и других
причин. Например, сахарный диабет может
развиваться при акромегалии (гиперсекреция
СТГ), синдроме Иценко-Кушинга (избыток
глюкокортикоидов), гипертирозе
(гиперсекреция Т3, Т4), феохромоцигоме
(опухоль, продуцирующая катехоламины),
глюкагономе (опухоль, продуцирующая
глюкагон).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Поджелудочная
железа
относится к железам со смешанной
функцией. Эндокринная функция
осуществляется за счет продукции
гормонов панкреатическими островками
(островками Лангерганса). Островки
расположены в хвостовой части железы,
и немного в головном отделе. В островках
имеется несколько типов клеток: a, b, d.
a-Клетки вырабатывают глюкагон, b-клетки
продуцируют инсулин, d-клетки синтезируют
соматостатин, который угнетает секрецию
инсулина и глюкагона
Инсулин
влияет на все виды обмена веществ, но
прежде всего на углеводный. происходит
уменьшение концентрации глюкозы в
плазме крови (гипогликемия), способствует
превращению глюкозы в гликоген в печени
и мышцах (гликогенез). Он активирует
ферменты, участвующие в превращении
глюкозы в гликоген печени, и ингибирует
ферменты, расщепляющие гликоген. повышает
проницаемость клеточной мембраны для
глюкозы, что усиливает ее утилизацию;
угнетает активность ферментов,
обеспечивающих глюконеогенез, за счет
чего тормозится образование глюкозы
из аминокислот.;стимулирует синтез
белка из аминокислот и уменьшает
катаболизм белка; регулирует жировой
обмен.
Образование
инсулина регулируется уровнем глюкозы
в плазме крови. Гипергликемия способствует
увеличению выработки инсулина,
гипогликемия уменьшает образование и
поступление гормона в кровь. Некоторые
гормоны желудочно-кишечного тракта
увеличивают выход инсулина. Блуждающий
нерв и ацетилхолин усиливают продукцию
инсулина, симпатические нервы и
норадреналин подавляют секрецию.
Антагонистами
инсулина по характеру действия на
углеводный обмен являются глюкагон,
АКТГ, соматотропин, глюкокортикоиды,
адреналин, тироксин. Введение этих
гормонов вызывает гипергликемию.
Недостаточная
секреция инсулина приводит к заболеванию,
которое получило название сахарного
диабета.
У больных нарушается не только углеводный,
но и белковый и жировой обмен. Усиливается
липолиз с образованием большого
количества несвязанных жирных кислот,
происходит синтез кетоновых тел.
Катаболизм белка приводит к снижению
массы тела. Интенсивное образование
кислых продуктов расщепления жиров и
дезаминирования аминокислот в печени
могут вызвать сдвиг реакции крови в
сторону ацидоза и развитие гипергликемической
диабетической комы, которая проявляется
потерей сознания, нарушениями дыхания
и кровообращения.
Избыточное
содержание инсулина в крови (например,
при опухоли островковых клеток или при
передозировке экзогенного инсулина)
вызывает гипогликемию и может привести
к нарушению энергетического обеспечения
мозга и потере сознания (гипогликемической
коме).
a-Клетки
островков Лангерганса синтезируют
глюкагон,
который является антагонистом инсулина.
Под влиянием глюкагона происходит
распад гликогена в печени до глюкозы.
В результате этого повышается содержание
глюкозы в крови. Глюкагон способствует
мобилизации жира из жировых депо.
Секреция глюкагона также зависит от
концентрации глюкозы в крови. Гипергликемия
тормозит образование глюкагона,
гипогликемия, напротив, увеличивает.
Соседние файлы в предмете Нормальная анатомия
- #
- #
- #
- #
Источник
Гормонами поджелудочной железы являются инсулин и глюкагон.
Глюкагон
Строение
Представляет собой полипептид, включающий 29 аминокислот с молекулярной массой 3,5 кДа и периодом полураспада 3-6 мин.
Синтез
Осуществляется в клетках поджелудочной железы и в клетках тонкого кишечника.
Регуляция синтеза и секреции
Активируют: гипогликемия, адреналин.
Уменьшают: глюкоза, жирные кислоты.
Механизм действия
Аденилатциклазный активирующий.
Мишени и эффекты
Конечным эффектом является повышение концентрации глюкозы и жирных кислот в крови.
Жировая ткань
- повышает активность внутриклеточной гормон-чувствительной ТАГ-липазы и, соответственно, стимулирует липолиз.
Печень
- активация глюконеогенеза и гликогенолиза,
- за счет повышенного поступления жирных кислот из жировой ткани усиливает кетогенез.
Патология
Гиперфункция
Глюкагонома – редко встречающееся новообразование из группы нейроэндокринных опухолей. У больных отмечается гипергликемия и поражение кожи и слизистых оболочек.
Инсулин
Дополнительная, более подробная информация, об инсулине находится на следующей странице.
Строение
Представляет собой полипептид из 51 аминокислоты, массой 5,7 кД, состоящий из двух цепей А и В, связанных между собой дисульфидными мостиками.
Синтез
Синтезируется в клетках поджелудочной железы в виде проинсулина, в этом виде он упаковывается в секреторные гранулы и уже здесь образуется инсулин и С-пептид.
Регуляция синтеза и секреции
Активируют синтез и секрецию:
- глюкоза крови – главный регулятор, пороговая концентрация для секреции инсулина – 5,5 ммоль/л,
- жирные кислоты и аминокислоты,
- влияния n.vagus – находится под контролем гипоталамуса, активность которого определяется концентрацией глюкозы крови,
- гормоны ЖКТ: холецистокинин, секретин, гастрин, энтероглюкагон, желудочный ингибирующий полипептид,
- хроническое воздействие гормона роста, глюкокортикоидов, эстрогенов, прогестинов.
Уменьшают: влияние симпато-адреналовой системы.
Механизм действия
Осуществляется через рецепторы с тирозинкиназной активностью (подробно).
Мишени и эффекты
Основным эффектом является снижение концентрации глюкозы в крови благодаря усилению транспорта глюкозы внутрь миоцитов и адипоцитов и активации внутриклеточных реакций утилизации глюкозы:
- активируя фосфодиэстеразу, которая разрушает вторичный мессенджер цАМФ, инсулин прерывает эффекты адреналина и глюкагона на печень и жировую ткань.
- в мышцах и жировой ткани стимулирует транспорт глюкозы в клетки (активация Глют-4),
- в печени и мышцах ускоряет синтез гликогена (активация гликогенсинтазы).
- в печени, мышцах и адипоцитах инсулин стимулирует гликолиз, активируя фосфофруктокиназу и пируваткиназу.
- полученный в гликолизе пируват превращается в ацетил-SКоА под влиянием активированного инсулином пируватдегидрогеназного комплекса, и далее используется для синтеза жирных кислот. Превращение ацетил-SКоА в малонил-SКоА, первый субстрат синтеза жирных кислот, также стимулируется инсулином (ацетил-SКоА-карбоксилаза).
- в мышцах усиливает транспорт нейтральных аминокислот в миоциты и стимулирует трансляцию (рибосомальный синтез белков).
Ряд эффектов инсулина заключается в изменении транскрипции генов и скорости трансляции ферментов, отвечающих за обмен веществ, за рост и деление клеток.
Благодаря этому индуцируется синтез ферментов метаболизма
- углеводов в печени (глюкокиназа, пируваткиназа, глюкозо-6-фосфатдегидрогеназа),
- липидов в печени (АТФ-цитрат-лиаза, ацетил-SКоА-карбоксилаза, синтаза жирных кислот, цитозольная малатдегидрогеназа) и адипоцитах (ГАФ-дегидрогеназа, пальмитатсинтаза, липопротеинлипаза).
и происходит репрессия фосфоенолпируват-карбоксикиназы (подавление глюконеогенеза).
Инактивация инсулина
Инактивация инсулина начинается после интернализации инсулин-рецепторного комплекса и образования эндосомы, в которой и происходит деградация инсулина. Участвуют две ферментные системы:
- Глутатион-инсулин-трансгидрогеназа, которая восстанавливает дисульфидные связи между цепями А и В, в результате чего гормон распадается.
- Инсулиназа (инсулин-протеиназа), гидролизующая инсулин до аминокислот.
Период полужизни инсулина не превышает 5-6 минут. Происходит деградация в основном в печени и почках, но и другие ткани принимают в этом участие. Также в почках инсулин может фильтроваться, захватываться эпителиоцитами проксимальных канальцев и разрушаться до аминокислот.
Патология
Гипофункция
Инсулинзависимый и инсулиннезависимый сахарный диабет. Для диагностики этих патологий в клинике активно используют нагрузочные пробы и определение концентрации инсулина и С-пептида.
Источник
Поджелудочная железа – железа со смешанной функцией. Морфологической единицей железы служат островки Лангерганса, преимущественно они расположены в хвосте железы. Бета-клетки островков вырабатывают инсулин, альфа-клетки – глюкагон, дельта-клетки – соматостатин. В экстрактах ткани поджелудочной железы обнаружены гормоны ваготонин и центропнеин.
Инсулин регулирует углеводный обмен, снижает концентрацию сахара в крови, способствует превращению глюкозы в гликоген в печени и мышцах. Он повышает проницаемость клеточных мембран для глюкозы: попадая внутрь клетки, глюкоза усваивается. Инсулин задерживает распад белков и превращение их в глюкозу, стимулирует синтез белка из аминокислот и их активный транспорт в клетку, регулирует жировой обмен путем образования высших жирных кислот из продуктов углеводного обмена, тормозит мобилизацию жира из жировой ткани.
В бета-клетках инсулин образуется из своего предшественника проинсулина. Он переносится в клеточные аппарат Гольджи, где происходят начальные стадии превращения проинсулина в инсулин.
В основе регуляции инсулина лежит нормальное содержание глюкозы в крови: гипергликемия приводит к увеличению поступления инсулина в кровь, и наоборот.
Паравентрикулярные ядра гипоталамуса повышают активность при гипергликемии, возбуждение идет в продолговатый мозг, оттуда в ганглии поджелудочной железы и к бета-клеткам, что усиливает образование инсулина и его секрецию. При гипогликемии ядра гипоталамуса снижают свою активность, и секреция инсулина уменьшается.
Гипергликемия непосредственно приводит в возбуждение рецепторный аппарат островков Лангерганса, что увеличивает секрецию инсулина. Глюкоза также непосредственно действует на бета-клетки, что ведет к высвобождению инсулина.
Глюкагон повышает количество глюкозы, что также ведет к усилению продукции инсулина. Аналогично действует гормоны надпочечников.
ВНС регулирует выработку инсулина посредством блуждающего и симпатического нервов. Блуждающий нерв стимулирует выделение инсулина, а симпатический тормозит.
Количество инсулина в крови определяется активностью фермента инсулиназы, который разрушает гормон. Наибольшее количество фермента находится в печени и мышцах. При однократном протекании крови через печень разрушается до 50 % находящегося в крови инсулина.
Важную роль в регуляции секреции инсулина выполняет гормон соматостатин, который образуется в ядрах гипоталамуса и дельта-клетках поджелудочной железы. Соматостатин тормозит секрецию инсулина.
Активность инсулина выражается в лабораторных и клинических единицах.
Глюкагон принимает участие в регуляции углеводного обмена, по действию на обмен углеводов он является антагонистом инсулина. Глюкагон расщепляет гликоген в печени до глюкозы, концентрация глюкозы в крови повышается. Глюкагон стимулирует расщепление жиров в жировой ткани.
Механизм действия глюкагона обусловлен его взаимодействием с особыми специфическими рецепторами, которые находятся на клеточной мембране. При связи глюкагона с ними увеличивается активность фермента аденилатциклазы и концентрации цАМФ, цАМФ способствует процессу гликогенолиза.
Регуляция секреции глюкагона. На образование глюкагона в альфа-клетках оказывает влияние уровень глюкозы в крови. При повышении глюкозы в крови происходит торможение секреции глюкагона, при понижении – увеличение. На образование глюкагона оказывает влияние и передняя доля гипофиза.
Гормон роста соматотропин повышает активность альфа-клеток. В противоположность этому гормон дельта-клетки – соматостатин тормозит образование и секрецию глюкагона, так как он блокирует вхождение в альфа-клетки ионов Ca, которые необходимы для образования и секреции глюкагона.
Липокаин способствует утилизации жиров за счет стимуляции образования липидов и окисления жирных кислот в печени, он предотвращает жировое перерождение печени.
Ваготонин повышает тонус блуждающих нервов, усиливает их активность.
Центропнеин участвует в возбуждении дыхательного центра, содействует расслаблению гладкой мускулатуры бронхов, повышает способность гемоглобина связывать кислород, улучшает транспорт кислорода.
Нарушение функции поджелудочной железы.
Уменьшение секреции инсулина приводит к развитию сахарного диабета, основными симптомами которого являются гипергликемия, глюкозурия, полиурия (до 10 л в сутки), полифагия (усиленный аппетит), полидиспепсия (повышенная жажда).
Увеличение сахара в крови у больных сахарным диабетом является результатом потери способности печени синтезировать гликоген из глюкозы, а клеток – утилизировать глюкозу. В мышцах также замедляется процесс образования и отложения гликогена.
У больных сахарным диабетом нарушаются все виды обмена.
Источник